题目内容
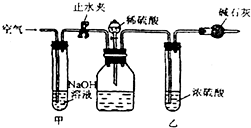
工业生产的纯碱中常有少量的NaCl等杂质.下图是测定产品中Na2CO3质量分数的实验装置.实验的步骤是:
A.检验装置的气密性
B.取ng样品装入广口瓶中
C.打开止水夹
D.缓缓鼓入空气数分钟
E.关闭止水夹
F.在干燥管内填满碱石灰,总质量为mg
G.缓缓加入稀硫酸至不再产生气体为止
H.打开止水夹
I.缓缓鼓入空气数分钟,再称干燥管总质量为Wg
请回答以下问题:
(1)操作步骤I中,要缓缓鼓入空气数分钟,鼓入空气的作用是 ;
装置甲的作用是 ;
装置乙的作用是 .
(2)计算溶液中Na2CO3质量分数的计算式为 .
(3)若去掉装置甲,测定结果会 ;若去掉装置乙,测定结果会 (填“偏大”“偏小”或“无影响”).

A.检验装置的气密性
B.取ng样品装入广口瓶中
C.打开止水夹
D.缓缓鼓入空气数分钟
E.关闭止水夹
F.在干燥管内填满碱石灰,总质量为mg
G.缓缓加入稀硫酸至不再产生气体为止
H.打开止水夹
I.缓缓鼓入空气数分钟,再称干燥管总质量为Wg
请回答以下问题:
(1)操作步骤I中,要缓缓鼓入空气数分钟,鼓入空气的作用是
装置甲的作用是
装置乙的作用是
(2)计算溶液中Na2CO3质量分数的计算式为
(3)若去掉装置甲,测定结果会
考点:探究物质的组成或测量物质的含量,钠的重要化合物
专题:实验探究和数据处理题
分析:(1)装置中残留生成的二氧化碳,不将二氧化碳排尽,会影响测定的二氧化碳的质量,从装置中产生导出的气体中含有水,如果不除去气体中的水,会使碱石灰增重偏多,二氧化碳的质量增大;
(2)由实验目的可知,反应生成的二氧化碳的质量为(W-m)g,计算二氧化碳的物质的量,根据碳元素守恒二氧化碳的物质的量等于样品中碳酸钠的物质的量,计算样品中碳酸钠的质量,再利用质量分数的定义进行求解;
(3)装置甲中装有氢氧化钠,氢氧化钠吸收二氧化碳,可除掉空气中的二氧化碳;如果不除去气体中的二氧化碳,会使干燥管中测定的二氧化碳的质量增大;从广口瓶中产生导出的气体中含有水,如果不除去气体中的水,会使干燥管中测定的二氧化碳的质量增大.
(2)由实验目的可知,反应生成的二氧化碳的质量为(W-m)g,计算二氧化碳的物质的量,根据碳元素守恒二氧化碳的物质的量等于样品中碳酸钠的物质的量,计算样品中碳酸钠的质量,再利用质量分数的定义进行求解;
(3)装置甲中装有氢氧化钠,氢氧化钠吸收二氧化碳,可除掉空气中的二氧化碳;如果不除去气体中的二氧化碳,会使干燥管中测定的二氧化碳的质量增大;从广口瓶中产生导出的气体中含有水,如果不除去气体中的水,会使干燥管中测定的二氧化碳的质量增大.
解答:
解:(1)稀硫酸和碳酸钠反应生成二氧化碳和硫酸钠和水,测定产品中Na2CO3质量分数,是通过测定稀硫酸和碳酸钠生成物中的二氧化碳的量,根据碳元素守恒,测定样品中碳酸钠质量分数,操作步骤I中,要缓缓鼓入空气数分钟,使广口瓶中的产生的二氧化碳气体全部排出;装置甲中装有氢氧化钠,氢氧化钠吸收二氧化碳,除掉空气中的二氧化碳;装置乙中装有浓硫酸,浓硫酸具有吸水性,能吸收二氧化碳中的水蒸气,
故答案为:使广口瓶中的产生的二氧化碳气体全部排出;吸收空气中的二氧化碳;吸收二氧化碳中的水蒸气;
(2)由题意可知,反应生成的二氧化碳的质量为(W-m)g,二氧化碳的物质的量n=
=
mol,根据碳元素守恒可知样品中碳酸钠的物质的量n=
mol,样品中碳酸钠的质量为m=n×M=
mol×106g/mol=
g,样品中碳酸钠质量分数为
×100%=
×100%,
故答案为:
×100%;
(3)装置甲中装有氢氧化钠,氢氧化钠吸收二氧化碳,可除掉空气中的二氧化碳,鼓入空气数分钟,使广口瓶中的产生的二氧化碳气体全部排出,若去掉装置甲,空气中的二氧化碳未除去,装置中二氧化碳的质量增大,会使干燥管中测定的二氧化碳的质量增大,导致测定的样品中碳酸钠的质量增大;从广口瓶中产生导出的气体中含有水,如果不除去气体中的水,会使干燥管中测定的二氧化碳的质量增大,计算样品中碳酸钠的质量是根据碳元素守恒二氧化碳的物质的量等于样品中碳酸钠的物质的量进行计算的,所以会导致测定的样品中碳酸钠的质量增大,测定的碳酸钠质量分数偏大,
故答案为:偏大;偏大.
故答案为:使广口瓶中的产生的二氧化碳气体全部排出;吸收空气中的二氧化碳;吸收二氧化碳中的水蒸气;
(2)由题意可知,反应生成的二氧化碳的质量为(W-m)g,二氧化碳的物质的量n=
| (W-m)g |
| 44g/mol |
| W-m |
| 44 |
| W-m |
| 44 |
| W-m |
| 44 |
| 53(W-m) |
| 22 |
| ||
| n |
| 53(W-m) |
| 22n |
故答案为:
| 53(W-m) |
| 22n |
(3)装置甲中装有氢氧化钠,氢氧化钠吸收二氧化碳,可除掉空气中的二氧化碳,鼓入空气数分钟,使广口瓶中的产生的二氧化碳气体全部排出,若去掉装置甲,空气中的二氧化碳未除去,装置中二氧化碳的质量增大,会使干燥管中测定的二氧化碳的质量增大,导致测定的样品中碳酸钠的质量增大;从广口瓶中产生导出的气体中含有水,如果不除去气体中的水,会使干燥管中测定的二氧化碳的质量增大,计算样品中碳酸钠的质量是根据碳元素守恒二氧化碳的物质的量等于样品中碳酸钠的物质的量进行计算的,所以会导致测定的样品中碳酸钠的质量增大,测定的碳酸钠质量分数偏大,
故答案为:偏大;偏大.
点评:本题考查了物质含量的测定,解答须理解实验原理、理解装置设计用途、实验目的,结合相关物质的化学性质进行解答,题目难度中等.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
在(NH4)2Fe(SO4)2?6H2O晶体溶于水后的溶液中,加入下列物质不能发生反应的是( )
| A、HNO3 |
| B、HCl |
| C、NaOH |
| D、Cl2 |
为了检验某FeCl2溶液是否变质,可向溶液中加入( )
| A、NaOH | B、铁片 |
| C、KSCN溶液 | D、石蕊溶液 |
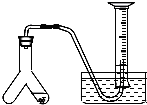 在室温和大气压强下,用图示的装置进行实验,测得a g含CaC2 90%的样品与水完全反应产生的气体体积为b L.现欲在相同条件下,测定某电石试样中CaC2的质量分数,请回答下列问题:
在室温和大气压强下,用图示的装置进行实验,测得a g含CaC2 90%的样品与水完全反应产生的气体体积为b L.现欲在相同条件下,测定某电石试样中CaC2的质量分数,请回答下列问题: