题目内容
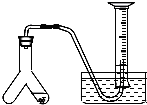 在室温和大气压强下,用图示的装置进行实验,测得a g含CaC2 90%的样品与水完全反应产生的气体体积为b L.现欲在相同条件下,测定某电石试样中CaC2的质量分数,请回答下列问题:
在室温和大气压强下,用图示的装置进行实验,测得a g含CaC2 90%的样品与水完全反应产生的气体体积为b L.现欲在相同条件下,测定某电石试样中CaC2的质量分数,请回答下列问题:(1)CaC2的电子式:
(2)CaC2和水反应的化学方程式是
(3)若反应刚结束时,观察到的实验现象如图所示,这时不能立即取出导气管,理由
(4)本实验中测量气体体积时应注意的事项是
(5)实验时防止乙炔泄漏,试剂添加和使反应开始进行应该如何操作?
(6)如果电石试样质量为c g,测得气体体积为d L,则电石试样中CaC2的质量分数计算式w(CaC2)=
考点:探究物质的组成或测量物质的含量
专题:阿伏加德罗常数和阿伏加德罗定律
分析:(1)碳化钙是钙离子和C22-离子构成的离子化合物,结合阴阳离子结构书写电子式;
(2)碳化钙和水反应生成氢氧化钙和乙炔;
(3)反应是放热反应,气体温度过高气体压强和外界大气压不同,读取气体体积产生误差;
(4)测量气体体积时应注意的事项守恒温度 在常温下,调节量筒使其内外液面持平,保证读取气体体积的准确性;
(5)实验时防止乙炔泄漏,试剂添加和使反应开始进行的操作是:检查装置气密性,加试剂时先将叉形管向一侧倾斜把电石滑入管低,再将叉形管向另一侧倾斜沿管壁加入蒸馏水;要使反应开始先将橡皮塞及导管提高,与叉形管连接,再将叉形管向有电石一侧倾斜,反应即可发生;
(6)依据产生C2H2的体积在相同条件下,与纯CaC2的质量成正比计算得到;
(2)碳化钙和水反应生成氢氧化钙和乙炔;
(3)反应是放热反应,气体温度过高气体压强和外界大气压不同,读取气体体积产生误差;
(4)测量气体体积时应注意的事项守恒温度 在常温下,调节量筒使其内外液面持平,保证读取气体体积的准确性;
(5)实验时防止乙炔泄漏,试剂添加和使反应开始进行的操作是:检查装置气密性,加试剂时先将叉形管向一侧倾斜把电石滑入管低,再将叉形管向另一侧倾斜沿管壁加入蒸馏水;要使反应开始先将橡皮塞及导管提高,与叉形管连接,再将叉形管向有电石一侧倾斜,反应即可发生;
(6)依据产生C2H2的体积在相同条件下,与纯CaC2的质量成正比计算得到;
解答:
解:(1)碳化钙是钙离子和C22-离子构成的离子化合物,结合阴阳离子结构书写电子式为
故答案为: ;
;
(2)碳化钙和水反应生成氢氧化钙和乙炔,反应的化学方程式为:CaC2+2H2O→Ca(OH)2+C2H2↑;
故答案为:CaC2+2H2O→Ca(OH)2+C2H2↑;
(3)由于CaC2与H2O的反应CaC2+2H2O→Ca(OH)2+C2H2↑为剧烈的放热反应,故在没有恢复到室温时,内部气体压强不等于大气压,故不能取出导气管;
故答案为:因为装置内气体的温度没有恢复到室温,气体压强不等于大气压强;
(4)反应是放热反应,装置中温度冷却后再取出导管,即使在恢复到室温后,也应调节量筒使其内外液面持平时才能读数;
故答案为:待装置内气体的温度恢复到室温后,调节量筒使其内外液面持平;
(5)实验时防止乙炔泄漏,试剂添加和使反应开始进行的操作是:检查装置气密性,加试剂时先将叉形管向一侧倾斜把电石滑入管低,再将叉形管向另一侧倾斜沿管壁加入蒸馏水;要使反应开始先将橡皮塞及导管提高,与叉形管连接,再将叉形管向有电石一侧倾斜,反应即可发生;
故答案为:检查装置气密性,加试剂时先将叉形管向一侧倾斜把电石滑入管低,再将叉形管向另一侧倾斜沿管壁加入蒸馏水;要使反应开始先将橡皮塞及导管提高,与叉形管连接,再将叉形管向有电石一侧倾斜,反应即可发生;
(6)由于产生C2H2的体积在相同条件下,与纯CaC2的质量成正比,所以有:ag×90%:c g×w(CaC2)=bL:d L,即w(CaC2)=
×90%;
故答案为:
×90%;

故答案为:
 ;
;(2)碳化钙和水反应生成氢氧化钙和乙炔,反应的化学方程式为:CaC2+2H2O→Ca(OH)2+C2H2↑;
故答案为:CaC2+2H2O→Ca(OH)2+C2H2↑;
(3)由于CaC2与H2O的反应CaC2+2H2O→Ca(OH)2+C2H2↑为剧烈的放热反应,故在没有恢复到室温时,内部气体压强不等于大气压,故不能取出导气管;
故答案为:因为装置内气体的温度没有恢复到室温,气体压强不等于大气压强;
(4)反应是放热反应,装置中温度冷却后再取出导管,即使在恢复到室温后,也应调节量筒使其内外液面持平时才能读数;
故答案为:待装置内气体的温度恢复到室温后,调节量筒使其内外液面持平;
(5)实验时防止乙炔泄漏,试剂添加和使反应开始进行的操作是:检查装置气密性,加试剂时先将叉形管向一侧倾斜把电石滑入管低,再将叉形管向另一侧倾斜沿管壁加入蒸馏水;要使反应开始先将橡皮塞及导管提高,与叉形管连接,再将叉形管向有电石一侧倾斜,反应即可发生;
故答案为:检查装置气密性,加试剂时先将叉形管向一侧倾斜把电石滑入管低,再将叉形管向另一侧倾斜沿管壁加入蒸馏水;要使反应开始先将橡皮塞及导管提高,与叉形管连接,再将叉形管向有电石一侧倾斜,反应即可发生;
(6)由于产生C2H2的体积在相同条件下,与纯CaC2的质量成正比,所以有:ag×90%:c g×w(CaC2)=bL:d L,即w(CaC2)=
| ad |
| bc |
故答案为:
| ad |
| bc |
点评:本题主要考查简单的实验操作与简单的计算,实验过程分析和注意问题,主要是气体体积测定方法的理解应用,题目难度中等.

练习册系列答案
相关题目
常温下,有甲、乙两份体积均为1L,浓度均为0.1mol/L的氨水,其pH为11.
①甲用蒸馏水稀释100倍后,溶液的pH将为a;
②乙与等体积、浓度为0.1mol/L的HCl混合,在混合液中:n(NH4+)+n(H+)-n(OH-)=bmol
则a、b正确的答案组合是( )
①甲用蒸馏水稀释100倍后,溶液的pH将为a;
②乙与等体积、浓度为0.1mol/L的HCl混合,在混合液中:n(NH4+)+n(H+)-n(OH-)=bmol
则a、b正确的答案组合是( )
| A、9~11之间;0.1 |
| B、9~11之间;0.05 |
| C、12~13之间;0.2 |
| D、13;0.1 |
用一种试剂就可以将NaOH、NH4SCN、AgNO3、Na2SO4四种无色溶液一一鉴别出来,这种试剂是( )
| A、盐酸 |
| B、FeCl3 |
| C、Fe(NO3)3 |
| D、BaCl2 |
 (R代表烃基,下同.)
(R代表烃基,下同.)



 (R,R′可以是相同的烃基,也可能是不同的烃基)现用乙烯和适当的无机物合成乙酸异丁酯
(R,R′可以是相同的烃基,也可能是不同的烃基)现用乙烯和适当的无机物合成乙酸异丁酯 的过程如图(反应条件和部分产物没有列出):
的过程如图(反应条件和部分产物没有列出):