题目内容
7.设NA为阿伏加德罗常数的值,下列叙述正确的是( )| A. | 25℃,pH=12的Na2CO3溶液中含有OH-的数目为0.01NA | |
| B. | 1 mol苯乙烯( )中含有的碳碳双键数为4NA )中含有的碳碳双键数为4NA | |
| C. | 加热条件下,4.6g金属Na与足量O2反应的产物中阳离子和阴离子总数为0.3NA | |
| D. | 常温时,1 L0.1 mol•L-1的硝酸铵溶液中,NH4+和H+总数为0.1NA |
分析 A.溶液体积未知;
B.苯环中不含有碳碳双键;
C.依据2Na~Na2O2,结合过氧化钠中阴离子为过氧根离子解答;
D.依据溶液中电荷守恒:[NH4+]+[H+]=[NO3-]+[OH-]判断.
解答 解:A.依据n=cv可知,溶液体积未知,无法计算氢氧根离子个数,故A错误;
B.1 mol苯乙烯( )中含有的碳碳双键数为NA,故B错误;
)中含有的碳碳双键数为NA,故B错误;
C.加热条件下,4.6g金属Na与足量O2反应生成过氧化钠0.1mol,含有0.2mol钠离子和0.1mol过氧根离子,共含有阳离子和阴离子总数为0.3NA,故C正确;
D.常温时,1 L0.1 mol•L-1的硝酸铵溶液中,硝酸根离子物质的量为0.1mol,依据溶液中电荷守恒:[NH4+]+[H+]=[NO3-]+[OH-],可知NH4+和H+总数大于0.1NA,故D错误;
故选:C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,注意苯环中不含有碳碳双键,注意过氧化钠的结构,注意溶液中电荷守恒的应用,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.设NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A. | 7.8g Na2S与Na2O2的混合物中阴离子数大于0.1NA | |
| B. | 标准状况下,22.4L NO和11.2L O2混合后气体的分子总数为2NA | |
| C. | T℃时,1L pH=6的某水溶液中,含1×10-8NA个OH- | |
| D. | 84g由碳酸镁和碳酸氢钠组成的混合物与足量盐酸反应生成CO2的体积为22.4L(标准状况下) |
18.工业上将Na2CO3和Na2S以1:2的物质的量之比配成溶液,再通入SO2,可制取Na2S2O3,同时放出CO2.在该反应中( )
| A. | 硫元素既被氧化又被还原 | |
| B. | 氧化剂与还原剂的物质的量之比为1:2 | |
| C. | 每生成1molNa2S2O3,转移4mol电子 | |
| D. | 该化学离子方程式:CO32-+2S2-+4SO2═3S2O32-+CO2 |
15.下列实验能达到预期目的是( )
| A. | 检验溶液中是否含有I-:加入CCl4,CCl4层显紫色 | |
| B. | 检验溶液中是否含有SO42-:先滴加稀硝酸,再滴加BaCl2溶液 | |
| C. | 检验溶液中是否含有CO32-:滴加稀盐酸,将产生的气体通入澄清石灰水 | |
| D. | 检验溶液中是否含有S2-:滴加硫酸铜溶液,出现黑色沉淀 |
2.东汉著名的炼丹理论家魏伯阳所著的《周易参同契》提出:“胡粉投火中,色坏还为铅”,已知胡粉主要成分是2PbCO3•Pb(OH)2.下列有关说法正确的是( )
| A. | 胡粉中的Pb显+4价 | |
| B. | 这里的“火”中含有炭 | |
| C. | 此过程中可能发生了化合反应 | |
| D. | 在元素周期表中铅与炭都位于第ⅥA族 |
12.以下实验:①为检验RX是碘代烷,将RX与NaOH水溶液混合后再加入AgNO3溶液;②实验室里用无水乙醇和浓硫酸共热至140℃制乙烯;③用锌与稀硝酸反应制取氢气,并用排水法收集氢气;④在试管中加入2mL 10%的CuSO4溶液,滴入2%的NaOH溶液4~6滴,振荡后加入乙醛溶液0.5mL,加热至沸腾;⑤为检验淀粉已水解,将淀粉与少量稀硫酸加热一段时间后再加入银氨溶液,水浴加热;其中可能失败的实验是( )
| A. | ①②③④⑤ | B. | ①②④⑤ | C. | ②③④⑤ | D. | ②③⑤ |
19.用一种试剂除去下列各组物质中所含有的少量杂质(括号内为杂质),其中除杂方法正确的是( )
| A. | CO2(SO2):通过饱和Na2CO3溶液,洗气 | |
| B. | Cl2(HCl):通过NaOH固体,吸收 | |
| C. | BaCl2溶液(HCl):加入足量BaCO3,过滤 | |
| D. | FeCl3溶液(CuCl2):通入足量Fe,过滤 |
16.下列说法正确的是( )
| A. | 18gD2O中含有的中子数为10 NA(设NA为阿伏加德罗常数的数值) | |
| B. | 电解精炼铜时,每转移1mol电子,阳极溶解铜的质量为32g | |
| C. | 恒温恒容下,某可逆反应X(g)+Y(g)?Z(g)+W(s)△H>0达平衡后再加入X,该反应的△H增大 | |
| D. | 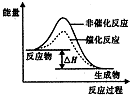 如图表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
17.在一个密闭容器中发生如下反应:2SO2(g)+O2(g)?2SO3(g),反应过程中某一时刻测得SO2、O2、SO3的浓度分别为:0.2mol•L-1、0.2mol•L-1、0.2mol•L-1,当反应达到平衡时,可能出现的数据是( )
| A. | c(SO3)=0.4 mol•L-1 | B. | c(SO2)=c(SO3)=0.15 mol•L-1 | ||
| C. | c(SO2)=0.25 mol•L-1 | D. | c(SO2)+c(SO3)=0.5 mol•L-1 |