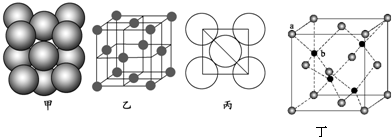
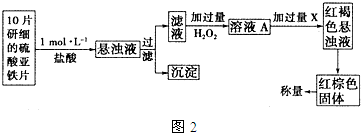
��Ŀ����
15�������º��� ��CH3COOH �ڣ�HCl �ۣ�H2SO4������Һ����1�������ǵ�pH��ͬʱ�������ʵ���Ũ�ȵĹ�ϵ�ǣ��٣��ڣ��� �������ֱ�ţ�
��2�������ǵ����ʵ���Ũ����ͬʱ����pH��ϵ�Ǣ٣��ڣ���
��3���к�ͬһ�ռ���Һ����ͬŨ�ȵ�������Һ�������ϵ�Ǣ�=�ڣ���
��4�������Ũ����ͬ�Ģ١��ڡ�������Һ���ֱ���ͬŨ�ȵ�NaOH��Һ��ӦʹpH����7������NaOH��Һ�������ϵ�Ǣ٣���=$\frac{1}{2}$��
��5��ij�¶��£���ˮ�е�c��H+��=2.0x10-7mol/L�����ʱ��Һ�е�c��OH-��Ϊ2��10-7mol/L
���¶Ȳ��䣬����ϡ����ʹc��H+��=5.0x10-6mol/L����c��OH-��Ϊ8��10-9mol/L��
���� ��1������Ϊ���ᣬ����ΪһԪǿ�ᣬ����Ϊ��Ԫǿ�ᣬ��pHʱ������Ũ�����
��2�����ʵ���Ũ����ͬʱ������������Ũ����࣬����������Ũ����С��
��3���к�ʱ����Ũ�ȵ������ᣬ�����������к�������ͬ��
��4�������Ũ����ͬ�Ģ١��ڡ�������Һ�������ʵ�����ȣ��ֱ���ͬŨ�ȵ��ռ���Һǡ����ȫ��Ӧ�������ռ���Һ����������Ԫ���ɷ��ȣ�
��5����ˮ�е�c��H+��=c��OH-����ij�¶��£���ˮ�е�c��H+��=2.0��10-7mol/L����Kw=4.0��10-14�����Kw���㣮
��� �⣺��1��pH��ͬ��Һ��������Ũ����ͬ��������һԪ���ᣬ�����Ƕ�Ԫǿ�ᡢ������һԪǿ�ᣬ����������Ũ��Ϊ1mol/L�������Ũ�ȴ���1mol/L������Ũ����1mol/L������Ũ����0.5mol/L�����������ʵ���Ũ�ȵ��ɴ�С������ �٣��ڣ��ۣ��ʴ�Ϊ���٣��ڣ��ۣ�
��2�������ǵ����ʵ���Ũ����ͬʱ�����趼��1mol/L��������������Ũ��С��1mol/L��������������Ũ����2mol/L��������������Ũ����1mol/L��������Ũ��Խ��pHԽС��������pH���ɴ�С�����Ǣ٣��ڣ��ۣ��ʴ�Ϊ���٣��ڣ��ۣ�
��3���к͵����������ƣ���ʧͬŨ�������������������������ӵ�Ũ�ȳɷ��ȣ�������ҺŨ����ȣ������Ƕ�Ԫ�ᡢ��������ᶼ��һԪ�ᣬ�������յ���������ӵ�Ũ���������=���ᣬ��������������������С˳���Ǣ�=�ڣ��ۣ��ʴ�Ϊ����=�ڣ��ۣ�
��4�������Ũ����ͬ�Ģ١��ڡ�������Һ�������ʵ�����ȣ��ֱ���ͬŨ�ȵ��ռ���Һǡ����ȫ��Ӧ�������ռ���Һ����������Ԫ���ɷ��ȣ������Ƕ�Ԫ�ᡢ��������ᶼ��һԪ�ᣬ������Ҫ�ռ���Һ�����ϵΪ �٣���=$\frac{1}{2}$�ۣ��ʴ�Ϊ���٣���=$\frac{1}{2}$�ۣ�
��5����ˮ�е�c��H+��=c��OH-����ij�¶��£���ˮ�е�c��H+��=2.0��10-7mol/L����Kw=4.0��10-14��
���¶Ȳ��䣬����ϡ����ʹc��H+��=5.0x10-6mol/L����c��OH-��=$\frac{4��1{0}^{-14}}{5��1{0}^{-6}}$mol/L=8��10-9 mol/L��
�ʴ�Ϊ��2��10-7��8��10-9��
���� ���⿼���������Һ�����жϣ����ؿ���ѧ���������ƶ���������ȷһԪ�ᡢ��Ԫ��ͼ�Ķ�����ϵ�ǽⱾ��ؼ�����Ŀ�Ѷ��еȣ�

�ڲ���������������������ʽ����ʱ��Һ��pH����������������Ũ��Ϊ��0.01mol/L��
| ������ | Fe��OH��3 | Fe��OH��2 | Co��OH��2 | Al��OH��3 | Mn��OH��2 |
| ��ʼ���� | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| ��ȫ���� | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
��1��ˮ�ܿ����Ԥ����ʱ����Na2SO3����Ҫ�����ǽ�Fe3+��Co3+��ԭ��
��2��д��NaClO3�ڽ���Һ�з�����Ҫ��Ӧ�����ӷ���ʽClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O������������Һ���мӹ���NaClO3ʱ�����ܻ������ж����壬д�����ɸ��ж���������ӷ���ʽClO3-+5Cl-+6H+=3Cl2��+3H2O��
��3������Na2CO3��pH��a����a��ȡֵ��Χ��5.2��a��7.6���������õ��ij����ɷ�ΪFe��OH��3��Al��OH��3��
��4��������1���а���3������ʵ���������������������Ũ������ȴ�ᾧ���ˣ��Ƶõ�CoCl2•6H2O�ں��ʱ���ѹ��ɵ�ԭ���ǽ��ͺ���¶ȣ���ֹ��Ʒ�ֽ⣮
��5����ȡ���Խ������ӵ���ȡ����pH�Ĺ�ϵ��ͼ2������Һ���м�����ȡ����Ŀ���dz�ȥ��Һ�е�Mn2+����ʹ�õ����pH��Χ��B��
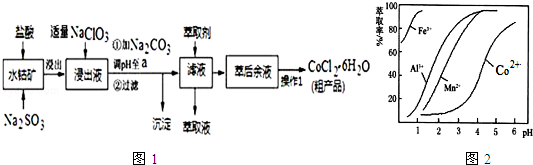
A��2.0��2.5 B��3.0��3.5 C��4.0��4.5 D��5.0��5.5
��6��Ϊ�ⶨ�ֲ�Ʒ��CoCl2•6H2O�ĺ�������ȡ16.4g�Ĵֲ�Ʒ����ˮ���100.0mL��Һ������ȡ��25.0mL������AgNO3��Һ��ϣ����ˡ�ϴ�ӡ���������ɺ��������Ϊ4��.6g����ֲ�Ʒ��CoCl2•6H2O������������93%�����������С�����һλ���֣�
| A�� | ������ˮ�еμ�ϡH2SO4��c��H+����KW������ | |
| B�� | ��Na2Sϡ��Һ�У�c��OH-��+c��HS-��+2c��S2-���Tc��H+��+c��Na+�� | |
| C�� | NaCl��Һ��CH3COONH4��Һ�������ԣ�����Һ��ˮ�ĵ���̶���ͬ | |
| D�� | �����0.2mol/LHCl��Һ��0.05mol/LBa��OH��2��Һ��Ϻ���Һ��pH=1 |
�ٹ���
�ڼӹ�����NaOH
�ۼ���������
�ܼӹ���Na2CO3��Һ
�ݼӹ���BaCl2��Һ��
| A�� | �٢ܢڢݢ� | B�� | �ܢ٢ڢݢ� | C�� | �ܢڢݢ٢� | D�� | �ݢڢܢ٢� |
| A�� | 4 v��NH3��=5 v��O2�� | B�� | 5 v��O2��=6 v��H2O�� | C�� | 5 v��NO��=4 v��O2�� | D�� | 3 v��H2O��=2 v��NH3�� |
| A�� | SiH4��CH4�ȶ� | |
| B�� | O2-�뾶��F-��С | |
| C�� | Na��Cs���ڵڢ�A��Ԫ�أ�Csʧ����������Na��ǿ | |
| D�� | HClO4��H2SO4��H3PO4������������ǿ |
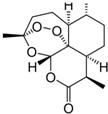 �ҹ�Ůҩѧ����������Ϊ��ű��ҩ�����صĵ�һ�������ٻ�2015��ŵ��������ѧ��ҽѧ���������صĽṹ��ͼ��ʾ�����й��������ص�˵��������ǣ�������
�ҹ�Ůҩѧ����������Ϊ��ű��ҩ�����صĵ�һ�������ٻ�2015��ŵ��������ѧ��ҽѧ���������صĽṹ��ͼ��ʾ�����й��������ص�˵��������ǣ�������| A�� | �����صĻ�ѧʽΪC15H22O5 | |
| B�� | �����ص�ͬ���칹������з����廯���� | |
| C�� | �����ؿ���NaOH��Һ����ˮ�ⷴӦ | |
| D�� | �����ؿ�������ˮ��ֲ����ȡ |