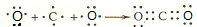题目内容
7.反应4NH3+5O2?4NO+6H2O均为气体,若化学反应速率分别用v(NH3),v(O2),v(NO),v(H2O)(单位:mol•L-1•s-1)表示,则关系正确的是( )| A. | 4 v(NH3)=5 v(O2) | B. | 5 v(O2)=6 v(H2O) | C. | 5 v(NO)=4 v(O2) | D. | 3 v(H2O)=2 v(NH3) |
分析 不同物质表示的速率之比等于化学计量数之比,据此计算判断.
解答 解:不同物质表示的速率之比等于其化学计量数之比,对于反应4NH3+5O2?4NO+6H2O,
A.v(NH3):v(O2)=4:5,则5 v(NH3)=4 v(O2),故A错误;
B.v(O2):v(H2O)=5:6,则6 v(O2)=5 v(H2O),故B错误;
C.v(NO):v(O2)=4:5,则5 v(NO)=4 v(O2),故C正确;
D.v(H2O):v(NH3)=6:4=3:2,则2 v(H2O)=3 v(NH3),故D错误.
故选:C.
点评 本题考查化学反应速率的有关计算,比较基础,注意速率计算常用方法有定义法与化学计量数法,同一反应不同的物质来表示化学反应速率,数值不同但意义相同,且化学反应速率之比等于化学计量数之比.

练习册系列答案
相关题目
2.下列有关叙述正确的是( )
| A. | 在中和滴定中,既可用标准溶液滴定待测溶液,也可用待测溶液滴定标准溶液 | |
| B. | 进行中和滴定操作中,眼睛要始终注视滴定管内溶液液面的变化 | |
| C. | 测定中和热时,两烧杯间填满碎纸的作用是固定小烧杯 | |
| D. | 若用50mL 0.55mo1•L-1的氢氧化钠溶液,分别与50mL 0.50mo1•L-1的盐酸和50mL 0.50mo1•L-1的硫酸充分反应,两反应的中和热不相等 |
2.下列化合物中,既存在离子键又存在共价键的是( )
| A. | 碳酸钠 | B. | 乙醇 | C. | 氯化钾 | D. | 一氧化碳 |
19.元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用.下表列出了①~⑨九种元素在周期表中的位置.
请回答:(1)这九种元素中化学性质最不活泼的是Ar(填元素符号).
(2)在①、②、③三种元素的最高价氧化物的水化物中,碱性最强的是KOH(填化学式).
(3)①、②、③三种元素按原子半径由大到小的顺序依次为K>Na>Mg(填元素符号).
(4)①、③、④、⑥四种元素的离子半径由大到小的顺序依次为Al3+(填离子符号).
(5)⑦、⑧两元素的最高价氧化物对应的水化物中,酸性最强的是HClO4(填化学式).
(6)⑥的氢化物与⑦的单质反应的离子方程式为Cl2+H2O?H++Cl-+HClO.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ④ | ⑦ | ⑨ | |||
| 4 | ② | ⑧ |
(2)在①、②、③三种元素的最高价氧化物的水化物中,碱性最强的是KOH(填化学式).
(3)①、②、③三种元素按原子半径由大到小的顺序依次为K>Na>Mg(填元素符号).
(4)①、③、④、⑥四种元素的离子半径由大到小的顺序依次为Al3+(填离子符号).
(5)⑦、⑧两元素的最高价氧化物对应的水化物中,酸性最强的是HClO4(填化学式).
(6)⑥的氢化物与⑦的单质反应的离子方程式为Cl2+H2O?H++Cl-+HClO.
17.氨气是生产化肥、硝酸等的重要原料,围绕合成氨人们进行了一系列的研究
(1)三氯化氮水解可生成氨气和物质X,X的电子式为 .
.
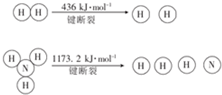
(2)已知:N2(g)+3H2 (g)?2NH3(g)△H=-92.4kJ•mol-1,断裂1molN≡N键需要的能量为946kJ.
(3)常温下,向amol•L-1的氨水中加入等体积bmol•L-1的盐酸,混合后溶液呈中性,则该温度下氨水的电离平衡常数为$\frac{b×1{0}^{-7}}{a-b}$(用含a和b的代数式表示).
(4)在相同温度下,向甲、乙、丙三个容积相同的恒容密闭容器中按照下列三种方式分别投料,发生反应:N2(g)+3H2 (g)?2NH3(g),测得甲容器中H2的平衡转化率为40%.
①乙容器中起始反应逆向(填“正向”“逆向”或“不”)移动.
②达到平衡时,甲、乙、丙三个容器中NH3的体积分数由大到小顺序为丙>甲=乙.
(5)现分别在150℃、300℃、500℃时向反应器中按n(N2):n(H2)=1:3投料发生反应:N2(g)+3H2 (g)?2NH3(g),该反应达到平衡时,体系中NH3的物质的量分数随压强的变化曲线如图所示.
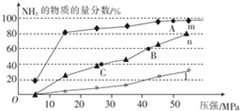
①150℃时发生的反应可用曲线m(填“m”“n”或“l”)表示.
②上图中A、B、C三点的平衡常数K的大小关系是K(A)>K(B)=K(C).
③若B点时c(NH3)=0.6mol•L-1,则此时反应的化学平衡常数K=$\frac{400}{3}$.
(1)三氯化氮水解可生成氨气和物质X,X的电子式为
 .
.(2)已知:N2(g)+3H2 (g)?2NH3(g)△H=-92.4kJ•mol-1,断裂1molN≡N键需要的能量为946kJ.

(3)常温下,向amol•L-1的氨水中加入等体积bmol•L-1的盐酸,混合后溶液呈中性,则该温度下氨水的电离平衡常数为$\frac{b×1{0}^{-7}}{a-b}$(用含a和b的代数式表示).
(4)在相同温度下,向甲、乙、丙三个容积相同的恒容密闭容器中按照下列三种方式分别投料,发生反应:N2(g)+3H2 (g)?2NH3(g),测得甲容器中H2的平衡转化率为40%.
| n(N2)/mol | N(H2)/mol | N(NH3)/mol | |
| 甲 | 1 | 3 | 0 |
| 乙 | 0.5 | 1.5 | 1 |
| 丙 | 0 | 0 | 4 |
②达到平衡时,甲、乙、丙三个容器中NH3的体积分数由大到小顺序为丙>甲=乙.
(5)现分别在150℃、300℃、500℃时向反应器中按n(N2):n(H2)=1:3投料发生反应:N2(g)+3H2 (g)?2NH3(g),该反应达到平衡时,体系中NH3的物质的量分数随压强的变化曲线如图所示.

①150℃时发生的反应可用曲线m(填“m”“n”或“l”)表示.
②上图中A、B、C三点的平衡常数K的大小关系是K(A)>K(B)=K(C).
③若B点时c(NH3)=0.6mol•L-1,则此时反应的化学平衡常数K=$\frac{400}{3}$.
 短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示,其中A为地壳中含量最高的金属元素.
短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示,其中A为地壳中含量最高的金属元素.