题目内容
15.下列各组中,含有离子晶体、分子晶体、原子晶体各一种的是( )| A. | KCl、HCl、S | B. | 金刚石、Na3PO4、MgO | ||
| C. | HF、SiC、Ar | D. | H2O、SiO2、K2CO3 |
分析 由离子键结合的物质为离子晶体,由分子构成的物质为分子晶体,由原子构成的物质且以共价键形成空间网状结构的物质为原子晶体,以此来解答.
解答 解:A、KCl为离子晶体,HCl、S为分子晶体,故A不选;
B、金刚石为原子晶体,Na3PO4、MgO为离子晶体,故B不选;
C、HF、Ar为分子晶体,SiC为原子晶体,故C不选;
D、H2O为分子晶体,SiO2为原子晶体,K2CO3为离子晶体,故D选;
故选D.
点评 本题考查晶体的判断,明确不同类型晶体的构成微粒及作用力即可解答,难度不大.

练习册系列答案
相关题目
5.最近美国宇航局(NASA)马里诺娃博士找到了一种比CO2有效104倍的“超级温室气体”--全氟丙烷(C3F8),并提出用其“温室化火星”,使火星成为第二个地球的计划.有关全氟丙烷的说法正确的是( )
| A. | 分子中三个碳原子可能处于同一直线上 | |
| B. | 全氟丙烷的结构式为 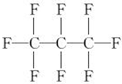 | |
| C. | 相同压强下,沸点:C3F8<C3H8 | |
| D. | 全氟丙烷分子中只有极性键 |
6.对于达到平衡状态的可逆反应:N2+3H2?2NH3,下列有关叙述正确的是( )
| A. | N2和NH3的质量分数相等 | |
| B. | N2、H2、NH3的浓度之比为1:3:2 | |
| C. | 当断开1mol氮氮三键的同时,断开3mol氢氢键 | |
| D. | 氮气的体积分数保持不变 |
3.W是由短周期元素X、Y、Z组成的盐.X、Y、Z原子的最外层电子数依次增大,Z原子最外层电子数是内层电子数的3倍;X、Y原子最外层电子数之和等于Z原子的最外层电子数;Y、Z同周期且相邻,但与X不同周期.下列说法一定正确的是( )
| A. | 三种元素的最高正化合价中,Z的最大 | |
| B. | W晶体中只存在有共价键 | |
| C. | 原子半径:X>Y>Z | |
| D. | Y的最高价氧化物对应的水化物是强酸 |
10.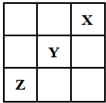 短周期元素X、Y、Z在周期表中的位置关系如图所示,已知X最外层电子数为2,则下列叙述中正确的是( )
短周期元素X、Y、Z在周期表中的位置关系如图所示,已知X最外层电子数为2,则下列叙述中正确的是( )
 短周期元素X、Y、Z在周期表中的位置关系如图所示,已知X最外层电子数为2,则下列叙述中正确的是( )
短周期元素X、Y、Z在周期表中的位置关系如图所示,已知X最外层电子数为2,则下列叙述中正确的是( )| A. | Y的氢化物稳定性大于Z的氢化物稳定性 | |
| B. | Z一定是活泼的金属元素 | |
| C. | Y的最高价氧化物的水化物是一种强酸 | |
| D. | 1molX的单质可以跟足量水反应,转移的电子为2mol |
20.2007年诺贝尔化学奖得主 Gerhard Ertl 对金属Pt表面催化CO氧化反应的模型进行了深入研究.下列关于${\;}_{78}^{202}$Pt和${\;}_{78}^{198}$Pt的说法正确的是( )
| A. | ${\;}_{78}^{202}$ Pt和${\;}_{78}^{198}$Pt的中子数相同,互称为同位素 | |
| B. | ${\;}_{78}^{202}$ Pt和${\;}_{78}^{198}$Pt的质子数相同,互称为同位素 | |
| C. | ${\;}_{78}^{202}$ Pt和${\;}_{78}^{198}$Pt不能互称为同位素 | |
| D. | ${\;}_{78}^{202}$Pt和${\;}_{78}^{198}$Pt是同一种核素 |
7.某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值,体积已换算成标准状态):
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5min)反应速率最大2~3 min
(2)哪一段时段的反应速率最小4~5 min.
(3)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变)0.1mol/(L.min).
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,可以在盐酸中分别加入等体积的下列溶液:
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4溶液
你认为可行的是(填编号)AB.
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
(2)哪一段时段的反应速率最小4~5 min.
(3)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变)0.1mol/(L.min).
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,可以在盐酸中分别加入等体积的下列溶液:
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4溶液
你认为可行的是(填编号)AB.
4.设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 标准状况下,33.6 L SO3分子含有的硫原子数为1.5NA | |
| B. | 1 mol/L KI溶液中I-数目为NA | |
| C. | 0.1 mol Na+离子中所含的电子数为3.4 NA | |
| D. | 56g铁与足量的Cl2或S反应时转移电子数均为3 NA |