题目内容
15.下列物质不能由单质直接化合得到的是( )| A. | NO | B. | Cu2S | C. | FeCl3 | D. | FeCl2 |
分析 A.氮气和氧气化合生成NO;
B.硫具有弱氧化性,Cu与S加热反应生成的是Cu2S;
C.氯气具有强氧化性,Fe与Cl2反应生成产物为氯化铁;
D.Fe化学性质比较活泼,氯气具有强氧化性,不会生成氯化亚铁.
解答 解:A.氮气和氧气在放电的条件下生成NO,反应为N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO,即可以由N2与O2直接化合得到NO,故A不选;
B.硫具有弱氧化性,与变价金属反应生成低价金属硫化物,所以铜与硫单质反应的化学方程式为:2Cu+S$\frac{\underline{\;\;△\;\;}}{\;}$Cu2S,即可以由Cu与S直接化合得到Cu2S,故B不选;
C.氯气具有强氧化性,氯气与变价金属反应生成最高价金属氯化物,铁与氯气反应的化学方程式为:2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3,即可以由Fe与Cl2直接化合得到FeCl3,故C不选;
D.氯气具有强氧化性,铁与氯气反应不会生成FeCl2,不能由单质直接化合得到FeCl2,故D选;
故选D.
点评 本题考查了常见单质的化学性质,题目难度不大,明确氯气具有强氧化性、硫具有弱氧化性,氯气与变价金属反应生成最高价金属氯化物、硫与变价金属反应生成低价金属硫化物是解答本题的关键,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
6.已知生产一个暖瓶胆需0.54gAg,现有0.05mo1乙醛溶液与足量的银氨溶液共热,最多可以制得暖瓶胆( )
| A. | 10个 | B. | 20个 | C. | 40个 | D. | 80 |
3.在标准状况下,11.2L H2的物质的量为( )
| A. | 1mol | B. | 2mol | C. | 0.5mol | D. | 1.5mol |
7.如图中所示的实验方法、装置或操作完全正确的是( )
| A. | 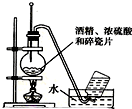 实验室制乙烯 | B. | 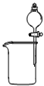 分离苯酚和水 | ||
| C. |  石油的蒸馏 | D. | 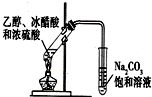 实验室制乙酸乙酯 |
4.把质量为 m g的Cu丝灼烧变黑,立即放入下列物质中,使Cu丝变红,而且质量仍为 m g的是( )
| A. | 稀H2SO4 | B. | C2H5OH | C. | 稀HNO3 | D. | CH 3COOH(aq) |
2.等浓度的下列溶液:①碳酸钠,②碳酸氢钠,③苯酚钠.溶液pH由小到大排列的是( )
| A. | ①②③ | B. | ②①③ | C. | ③①② | D. | ②③① |
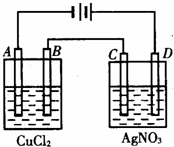 如图为以惰性电极进行电解:
如图为以惰性电极进行电解: