题目内容
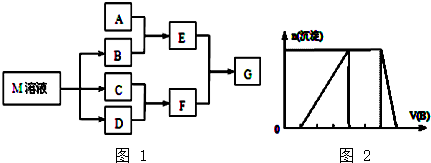
17.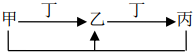 甲、乙、丙、丁四种物质中,甲、乙、丙含有相同的某种元素,它们之间有如下转化关系,则下列有关物质的推断错误的是( )
甲、乙、丙、丁四种物质中,甲、乙、丙含有相同的某种元素,它们之间有如下转化关系,则下列有关物质的推断错误的是( )| A. | 若甲为焦炭,则丁可能是O2 | |
| B. | 若甲为NaOH溶液,则丁可能是CO2 | |
| C. | 若甲为铝盐溶液,则丁可能是NaOH溶液 | |
| D. | 若甲为Fe,则丁可能是氯气 |
分析 A.甲为焦炭,则丁可能是O2,则乙为CO,丙为CO2;
B.甲为NaOH溶液,则丁可能是CO2,乙为Na2CO3,丙为NaHCO3;
C.若甲为AlCl3溶液,丁是NaOH溶液,则乙为氢氧化铝、丙为偏铝酸钠;
D.若甲为Fe,则丁可能是氯气,则乙为氯化铁,而氯化铁与氯气不反应.
解答 解:A.甲为焦炭,则丁可能是O2,则乙为CO,丙为CO2,二氧化碳与C反应得到CO,符合转化关系,故A正确;
B.甲为NaOH溶液,则丁可能是CO2,乙为Na2CO3,丙为NaHCO3,碳酸氢钠与氢氧化钠反应得到碳酸钠,符合转化关系,故B正确;
C.若甲为AlCl3溶液,丁是NaOH溶液,则乙为氢氧化铝、丙为偏铝酸钠,氯化铝与偏铝酸钠发生水解反应得到氢氧化铝,符合转化关系,故C正确;
D.若甲为Fe,则丁可能是氯气,则乙为氯化铁,而氯化铁与氯气不反应,所以不符合转化关系,故D错误;
故选D.
点评 本题考查无机物的推断,综合考查元素化合物性质,关键是掌握物质之间的相互转化,题目难度中等.

练习册系列答案
相关题目
8.油炸虾条、薯片等容易挤碎的食品,不宜选用真空袋装,而应采用充气袋装.下列气体中最不应该充入的是( )
| A. | 氮气 | B. | 二氧化碳 | C. | 氧气 | D. | 氦气 |
5.在1L某一元弱酸HR的溶液中,H+与HR的个数之比为m:n,则此时HR的电离平衡常数为( )
| A. | $\frac{{m}^{2}}{n}$ | B. | $\frac{{m}^{2}}{m+n}$ | C. | $\frac{{m}^{2}}{n-m}$ | D. | $\frac{{n}^{2}}{{m}^{3}}$ |
2.下列说法正确的是( )
| A. | 萃取溴水中的溴,将四氯化碳和溴水混合后,振荡并打开分液漏斗瓶塞,使漏斗内气体放出 | |
| B. | 在蔗糖中加入浓硫酸时,蔗糖变黑,证明浓硫酸具有脱水性 | |
| C. | 向Ba(NO3)2溶液中通入SO2气体,产生白色沉淀,可推测SO2与可溶性钡盐均能反应产生白色沉淀 | |
| D. | 若要检验铜和浓硫酸反应后产物硫酸铜,可向反应后的试管中加入少量水,观察溶液是否变蓝,若变蓝则证明有硫酸铜生成 |
9.下列离子方程式中不正确的是( )
| A. | Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| B. | 硫代硫酸钠与稀硫酸反应的离子方程式为S2O32-+2H+═SO42-+S↓+H2O | |
| C. | 利用水解原理制备纳米材料TiCl4+(2+n)H2O?4HCl+TiO2?nH2O↓ | |
| D. | 向明矾溶液中滴加Ba(OH)2至SO42-恰好完全沉淀时Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O |
6.对于常温pH=2的醋酸溶液,下列叙述不正确的是( )
| A. | c(H+)=c(CH3CO0-) | |
| B. | 加水稀释时$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$增大 | |
| C. | 与pH=12的NaOH溶液等体积混合后,溶液呈酸性 | |
| D. | 加入醋酸钠固体可抑制醋酸的电离,但电离常数Ka不变 |
14.某消毒液的主要成分为NaClO,还含有一定量的NaOH,下列说法不正确的是( )
| A. | 为测定该消毒液的pH,用玻璃棒蘸取液体滴在pH试纸上与标准比色卡对照即可 | |
| B. | 该消毒液可用NaOH溶液吸收Cl2制备:Cl2+2OH-═Cl-+ClO-+H2O | |
| C. | 该消毒液与洁厕灵(主要成分为HCl)混用,产生有毒Cl2:2H++Cl-+ClO-═Cl2↑+H2O | |
| D. | 该消毒液加白醋生成HClO,可增强漂白作用:CH3COOH+ClO-═HClO+CH3COO- |