题目内容
6.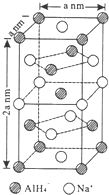 氢化铝钠(NaAlH4)是一种新型轻质储氢材料,掺入少量Ti的NaAlH4在150℃时释氢,在170℃、15.2MPa条件下又重复吸氢.NaAlH4可由AlCl3和NaH在适当条件下合成.NaAlH4的晶胞结构如图所示.
氢化铝钠(NaAlH4)是一种新型轻质储氢材料,掺入少量Ti的NaAlH4在150℃时释氢,在170℃、15.2MPa条件下又重复吸氢.NaAlH4可由AlCl3和NaH在适当条件下合成.NaAlH4的晶胞结构如图所示. (1)基态Ti原子的价电子轨道表示式为
 .
. (2)NaH的熔点为800℃,不溶于有机溶剂.NaH属于离子晶体,其电子式为
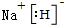 .
. (3)AlCl3在178℃时升华,其蒸气的相对分子质量约为267,蒸气分子的结构式为
 (标明配位键).
(标明配位键).(4)AlH4-中,Al的轨道杂化方式为sp3杂化;例举与AlH4-空间构型相同的两种离子NH4+、SO42-等(填化学式).
(5)NaAlH4晶体中,与Na+紧邻且等距的AlH4-有8个;NaAlH4晶体的密度为$\frac{108×1{0}^{21}}{{{N}_{A}a}^{3}}$g•cm-3(用含a的代数式表示).若NaAlH4晶胞底心处的Na+被Li+取代,得到的晶体为Na3Li[AlH4]4(填化学式).
(6)NaAlH4的释氢机理为:每3个AlH4-中,有2个分别释放出3个H原子和1个Al原子,同时与该Al原子最近邻的Na原子转移到被释放的Al原子留下的空位,形成新的结构.这种结构变化由表面层扩展到整个晶体,从而释放出氢气.该释氢过程可用化学方程式表示为3NaAlH4=Na3AlH6+2Al+3H2↑.
分析 (1)Ti原子核外电子数为22,价电子排布式为3d24s2,结合泡利原理、洪特规则画出价电子排布图;
(2)NaH的熔点为800℃,不溶于有机溶剂,应属于离子晶体,用钠离子与氢负离子构成;
(3)氯化铝在178℃时升华,熔沸点较低,属于分子晶体,蒸气的相对分子质量约为267,蒸气分子的分子式为Al2Cl6,铝原子最外层电子只有3个电子,形成3个共价键,每个铝原子和四个氯原子形成共价键,且其中一个共用电子对是氯原子提供形成的配位键;
(4)AlH4-中,Al的轨道杂化数目为4+$\frac{3+1-1×4}{2}$=4,Al采取sp3杂化,为正四面体构型;
(5)以体心的AlH4-研究,与之紧邻且等距的Na+位于晶胞棱之间、晶胞中上面立方体左右侧面面心、晶胞中下面立方体前后面的面心,与AlH4-紧邻且等距的Na+有8个,根据均摊法可知,晶胞中AlH4-数目为1+8×$\frac{1}{8}$+4×$\frac{1}{2}$=4,Na+数目为6×$\frac{1}{2}$+4×$\frac{1}{4}$=4,则二者配位数相等;
结合晶胞中AlH4-、Na+数目,表示出晶胞质量,再根据ρ=$\frac{m}{V}$计算密度;
若NaAlH4晶胞底心处的Na+被Li+取代,可知晶胞中Li+为1,再计算Na+数目,而晶胞中AlH4-数目不变,可得化学式;
(6)NaAlH4的释氢机理为:每3个AlH4-中,有2个分别释放出3个H原子和1个Al原子,同时与该Al原子最近邻的Na原子转移到被释放的Al原子留下的空位,根据原子守恒可知:3NaAlH4→Na3AlH6+2Al+3H2↑.
解答 解:(1)Ti原子核外电子数为22,价电子排布式为3d24s2,价电子排布图为 ,
,
故答案为: ;
;
(2)NaH的熔点为800℃,不溶于有机溶剂,应属于离子晶体,用钠离子与氢负离子构成,电子式为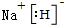 ,
,
故答案为: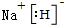 ;
;
(3)氯化铝在178℃时升华,熔沸点较低,属于分子晶体,蒸气的相对分子质量约为267,蒸气分子的分子式为Al2Cl6,铝原子最外层电子只有3个电子,形成3个共价键,每个铝原子和四个氯原子形成共价键,且其中一个共用电子对是氯原子提供形成的配位键,结构式如图 ,
,
故答案为: ;
;
(4)AlH4-中Al的轨道杂化数目为4+$\frac{3+1-1×4}{2}$=4,Al采取sp3杂化,为正四面体构型,与AlH4-空间构型相同的两种离子为NH4+、SO42-等,
故答案为:sp3杂化;NH4+、SO42-等;
(5)根据均摊法可知,晶胞中AlH4-数目为1+8×$\frac{1}{8}$+4×$\frac{1}{2}$=4,Na+数目为6×$\frac{1}{2}$+4×$\frac{1}{4}$=4,则二者配位数为1:1,以体心的AlH4-研究,与之紧邻且等距的Na+位于晶胞棱之间、晶胞中上面立方体左右侧面面心、晶胞中下面立方体前后面的面心,与AlH4-紧邻且等距的Na+有8个,则与Na+紧邻且等距的AlH4-有8个;
晶胞质量为4×$\frac{54}{{N}_{A}}$g,晶胞密度为4×$\frac{54}{{N}_{A}}$g÷[(a×10-7 cm)2×2a×10-7 cm]=$\frac{108×1{0}^{21}}{{{N}_{A}a}^{3}}$g•cm-3,
若NaAlH4晶胞底心处的Na+被Li+取代,可知晶胞中Li+为1,Na+数目为3,而晶胞中AlH4-数目不变,可得化学式Na3Li[AlH4]4,
故答案为:8;$\frac{108×1{0}^{21}}{{{N}_{A}a}^{3}}$;Na3Li[AlH4]4;
(6)NaAlH4的释氢机理为:每3个AlH4-中,有2个分别释放出3个H原子和1个Al原子,同时与该Al原子最近邻的Na原子转移到被释放的Al原子留下的空位,根据原子守恒可知:3NaAlH4→Na3AlH6+2Al+3H2,反应方程式为:3NaAlH4=Na3AlH6+2Al+3H2↑,
故答案为:3NaAlH4=Na3AlH6+2Al+3H2↑.
点评 本题是对物质结构与性质的考查,涉及核外电子排布、晶体类型与性质、杂化方式与空间构型、晶胞结构与计算等,题目素材中学基本不接触,容易是学生产生畏惧感,侧重考查学生对知识的迁移由于,(6)中注意利用原子守恒进行晶胞,避免考虑结构问题.

| A. | 4种 | B. | 8种 | C. | 10种 | D. | 12种 |
| A. | 1molCl2与足量的铁粉反应,反应转移电子的数目为3NA | |
| B. | 室温时,足量Zn与浓硫酸反应共产生2mol气体,转移电子数为4NA | |
| C. | 7.8gNa2O2与足量水反应时转移电子数目为0.2NA | |
| D. | 1mol二氧化氮气体久置后在标准状况下的体积为22.4L |
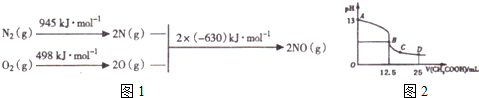
(1)汽车发动机工作时会引发N2和O2反应,其能量变化示意图如图1如下:
写出该反应的热化学方程式N2(g)+O2(g)=2NO(g)△H=+183KJ/mol
(2)在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NOx.碳氢化合 物)进行相互反应,生成无毒物质,在某温度时,探究某种催化剂作用下反应 2NO+2CO?N2+2CO2△H<0的反应速率.用气体传感器测得不同时间的 NO和C0浓度如下表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO) (×lO-4mol•L-1) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(CO) (×lO-3mol•L-1) | 2.70 | 2.15 | 1.95 | 1.85 | 1.80 | 1.80 |
①计算以v(CO)表示0-3s内的反应速率2.83×10-4mol•L-1•s-1在该温度下反应的平衡常数K=11250L•mol-1
②对于该可逆反应,通过综合分析以上信息,至少可以说明BC(填宇母)
A.该反应使用催化意义不大
B.该反应一旦发生将在很短的时间内完成
C.该反应体系达到平时至少有一种反应物的百分含量减小
(3)C0分析仪的传感器可测定汽车尾气是否符合排放标准.该分析仪的工作原理类似于燃料电池,其中电解质是氧化钇(Y2A3)和氧化锆(ZrO2)晶体.能传导02-则负极的电极反应式为CO+O2--2e-═CO2,以该电池为电源.以石墨为电极,电解2LO.1mol•L-1KCl溶液,写出电解反应的离子方程式2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑,电解一段时间后.取25mL上述电解后的溶液.滴加0.21mol•L-1醋酸得到如图2曲线 (不考虑能量损失和气体溶于水,溶液体积变化忽略不计).根据图计算,上述电解过程中消耗一氧化碳的质量为2.8g.
| A. | 1 | B. | l-a | C. | 2-lga | D. | 3-lga |
| A. | 50mL18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA | |
| B. | 某密闭容器盛有0.1mol N2和0.3mol H2,在一定条件下充分反应,转移电子的数目为0 6NA | |
| C. | 若由CO2和O2组成的混合物中共有NA个分子,则其中的氧原子数为2 NA | |
| D. | 常温下,1L 0. 1 mol/L NH4NO3溶液中的氢原子数为0.4 NA |
| A. | 有气泡产生,该气体能使带火星的火柴梗复燃 | |
| B. | 反应后溶液中有晶体析出 | |
| C. | 反应前后溶液中钠离子的浓度不变 | |
| D. | 反应前后溶液中钠离子的质量不变 |
