3.在一个密闭容器中放入M、N、P、Q四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应认识不正确的( )
| 物质 | M | N | P | Q |
| 反应前质量/g | 18 | 1 | 2 | 32 |
| 反应后质量/g | X | 26 | 2 | 12 |
| A. | 该反应是化合反应 | B. | 反应后物质M的质量为13g | ||
| C. | 反应中 N、P的质量之比为5:4 | D. | 物质M、P的相对分子质量比为1:4 |
2.除去下列物质中混有的杂质,所选用的试剂及操作方法均正确的是( )
| 物质 | 杂质 | 除杂质应选用的试剂和操作方法 | |
| A | CO2 | CO | 通入O2,点燃 |
| B | NaOH固体 | Na2CO3固体 | 加入过量盐酸,蒸发 |
| C | Cu(NO3)2溶液 | AgNO3溶液 | 加入过量的铜粉,过滤 |
| D | CuO固体 | Cu固体 | 加入适量的稀硫酸溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
1.要验证镁、铁、铜三种金属的活动顺序,通过下列试剂可达到实验目的是( )
| A. | 铁、铜、氯化镁溶液 | B. | 镁、铁、氯化铜溶液 | ||
| C. | 铁、氯化铜溶液、氯化镁溶液 | D. | 镁、氯化铜溶液、氯化亚铁溶液 |
20.正确的实验操作对实验结果、人身安全都非常重要.下列实验操作不正确的是( )
| A. |  滴加少量液体 | B. | 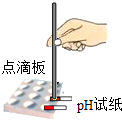 测定溶液pH | C. |  称量固体 | D. |  液体过滤 |
19.2011年为国际化学年,旨在“增进公众对化学重要性的认识,鼓励青年人热爱化学,憧憬化学的美好未来”.学习化学可以帮助人类认识改造周围的世界,促进社会发展.下列说法中,错误的是( )
| A. | 熟石灰能和酸发生反应,可用于改良酸性土壤 | |
| B. | “洗洁精”有乳化功能,可用于洗涤餐具上的油污 | |
| C. | 甲醛能使蛋白质变性,起到防腐作用,可用来浸泡水产品 | |
| D. | 限制使用塑料袋有利于减轻“白色污染” |
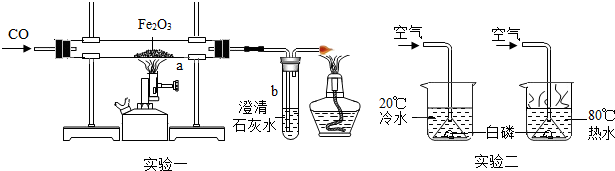
18.在小组活动中,老师讲烘干的碳酸镁与锌粉按照一定比例研细混匀,按照图1进行实验.
【提出问题】碳酸镁与锌粉反应的产物是什么?
【查阅资料】①氧化镁、氧化锌:均为白色固体,均与盐酸反应,生成无色盐溶液.
②碳酸镁、碳酸锌:均为白色固体,均与盐酸反应,生成无色盐溶液和二氧化碳气体.
【实验探究】
(1)实验一:碳酸镁与锌粉反应的气体产物是什么?
结论:碳酸镁与锌粉反应的气体燃烧的化学方程式为2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.
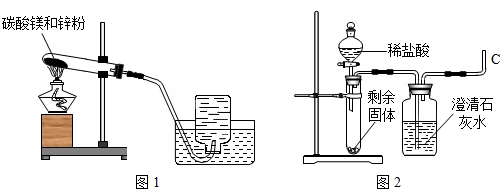
2)实验二:碳酸镁与锌粉反应的固体产物是什么?
老师将加热后的剩余固体分成两份,由甲、乙两组同学进行探究.
甲组同学将剩余固体直接按照图2进行实验,观察到A中有大量气泡生成,B中的澄清石灰水变浑浊,将产生的气体在C处验纯后点燃,观察到淡蓝色火焰.C处点燃的气体是H2(填化学式).甲组同学获得结论:该反应的固体产物是碳酸锌和镁.
乙组同学提出了质疑,他们先将另一份剩余固体先进行了处理,然后也按照图2进行了实验,观察到A中固体溶解,生成无色溶液,B中没有明显变化.他们对剩余固体的处理操作是继续按图1方式加热,直至不再产生气体.乙组同学利用实验现象,分析碳酸镁与锌粉反应的化学方程式为MgCO3+Zn$\frac{\underline{\;\;△\;\;}}{\;}$MgO+ZnO+CO↑.甲组同学对实验过程再次进行了认真分析,确定他们放入试管A中的固体含有MgCO3、Zn、MgO、ZnO.
【实验反思】:通过以上实验说明,在研究反应后的产物时.要考虑反应物是否有剩余.
0 166950 166958 166964 166968 166974 166976 166980 166986 166988 166994 167000 167004 167006 167010 167016 167018 167024 167028 167030 167034 167036 167040 167042 167044 167045 167046 167048 167049 167050 167052 167054 167058 167060 167064 167066 167070 167076 167078 167084 167088 167090 167094 167100 167106 167108 167114 167118 167120 167126 167130 167136 167144 211419
【提出问题】碳酸镁与锌粉反应的产物是什么?
【查阅资料】①氧化镁、氧化锌:均为白色固体,均与盐酸反应,生成无色盐溶液.
②碳酸镁、碳酸锌:均为白色固体,均与盐酸反应,生成无色盐溶液和二氧化碳气体.
【实验探究】
(1)实验一:碳酸镁与锌粉反应的气体产物是什么?
| 序号 | 实验操作 | 实验现象 |
| ① | 收集两瓶气体,盖好玻璃片,停止加热,向其中一瓶迅速倒入少量澄清石灰水,盖好振荡. | 无明显现象. |
| ② | 将另一瓶气体点燃,待火焰熄灭后,迅速倒入少量澄清石灰水,盖好振荡. | 气体安静燃烧,火焰呈蓝色,澄清石灰水变浑浊. |

2)实验二:碳酸镁与锌粉反应的固体产物是什么?
老师将加热后的剩余固体分成两份,由甲、乙两组同学进行探究.
甲组同学将剩余固体直接按照图2进行实验,观察到A中有大量气泡生成,B中的澄清石灰水变浑浊,将产生的气体在C处验纯后点燃,观察到淡蓝色火焰.C处点燃的气体是H2(填化学式).甲组同学获得结论:该反应的固体产物是碳酸锌和镁.
乙组同学提出了质疑,他们先将另一份剩余固体先进行了处理,然后也按照图2进行了实验,观察到A中固体溶解,生成无色溶液,B中没有明显变化.他们对剩余固体的处理操作是继续按图1方式加热,直至不再产生气体.乙组同学利用实验现象,分析碳酸镁与锌粉反应的化学方程式为MgCO3+Zn$\frac{\underline{\;\;△\;\;}}{\;}$MgO+ZnO+CO↑.甲组同学对实验过程再次进行了认真分析,确定他们放入试管A中的固体含有MgCO3、Zn、MgO、ZnO.
【实验反思】:通过以上实验说明,在研究反应后的产物时.要考虑反应物是否有剩余.

 图中的A-G表示几种初中化学常见的纯净物,其中A用于改良酸性土壤,B、C是氧化物,E俗称小苏打,人的胃液中含有F、E、G分别与足量F反应的生成物相同,图中“-”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系,部分反应物或生成物已略去.
图中的A-G表示几种初中化学常见的纯净物,其中A用于改良酸性土壤,B、C是氧化物,E俗称小苏打,人的胃液中含有F、E、G分别与足量F反应的生成物相同,图中“-”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系,部分反应物或生成物已略去.