题目内容
20.正确的实验操作对实验结果、人身安全都非常重要.下列实验操作不正确的是( )| A. |  滴加少量液体 | B. | 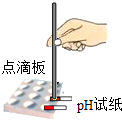 测定溶液pH | C. |  称量固体 | D. |  液体过滤 |
分析 A、根据使用胶头滴管滴加少量液体的方法进行分析判断;
B、根据测定溶液pH的注意事项分析;
C、根据托盘天平的使用分析;
D、根据液体的过滤分析.
解答 解:A、使用胶头滴管滴加少量液体的操作,注意胶头滴管的位置是否伸入到试管内或接触试管内壁.应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,图中所示操作错误;
B、测定溶液pH的操作正确;
C、托盘天平的使用正确;
D、液体过滤用玻璃棒引流,正确;
故选A
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
8.我国大部分地区深受酸雨的危害,煤燃烧产生的SO2是形成酸雨的主要污染物,SO2与水结合生成弱酸性亚硫酸(H2SO3).
已知:H2SO3易分解生成水和SO2,也易与空气中的氧气或稀硝酸反应生成H2SO4;H2SO3和SO2都能使红色的品红溶液褪色.
(1)酸雨是pH小于5.6的降雨.
(2)常用脱硫方法减少废气中的SO2和O2化合生成CaSO4,化学方程式为2CaO+2SO2+O2$\frac{\underline{\;高温\;}}{\;}$2CaSO4.
(3)实验室常用亚硫酸盐与HCl或H2SO4反应制备SO2,Na2SO3与盐酸反应的化学方程式为Na2SO3+2HCl═2NaCl+H2O+SO2↑.
(4)小鸿同学利用中和反应的原理,在空气中放置一段时间的酸雨(pH约为3)中加入足量的KOH,并就反应后混合溶液中盐的成分进行如下探究:
【提出猜想】反应后的混合溶液中盐的成分是什么?
猜想1:只有K2SO4
猜想2:只有K2SO3
猜想3:既有K2SO4,也有K2SO3
【实验探究】限选试剂:稀硫酸、稀盐酸、稀硝酸氯化钡溶液、澄清石灰水、红色品红溶液、紫色石蕊溶液.
已知:H2SO3易分解生成水和SO2,也易与空气中的氧气或稀硝酸反应生成H2SO4;H2SO3和SO2都能使红色的品红溶液褪色.
(1)酸雨是pH小于5.6的降雨.
(2)常用脱硫方法减少废气中的SO2和O2化合生成CaSO4,化学方程式为2CaO+2SO2+O2$\frac{\underline{\;高温\;}}{\;}$2CaSO4.
(3)实验室常用亚硫酸盐与HCl或H2SO4反应制备SO2,Na2SO3与盐酸反应的化学方程式为Na2SO3+2HCl═2NaCl+H2O+SO2↑.
(4)小鸿同学利用中和反应的原理,在空气中放置一段时间的酸雨(pH约为3)中加入足量的KOH,并就反应后混合溶液中盐的成分进行如下探究:
【提出猜想】反应后的混合溶液中盐的成分是什么?
猜想1:只有K2SO4
猜想2:只有K2SO3
猜想3:既有K2SO4,也有K2SO3
【实验探究】限选试剂:稀硫酸、稀盐酸、稀硝酸氯化钡溶液、澄清石灰水、红色品红溶液、紫色石蕊溶液.
| 步骤 | 实验操作 | 预期现象与结论 |
| 1 | 各取2mL反应后混合溶液分别加入A、B两支试管中 | / |
| 2 | 向A试管中滴加足量稀硫酸,随即滴加几滴红色品红溶液. | 有气泡产生,品红溶液褪色, 证明含有K2SO3. |
| 3 | 向B试管中,加入足量的氯化钡溶液,再加入足量稀盐酸. | 先有白色沉淀产生,后有气泡产生,沉淀部分溶解,证明含有K2SO4,则猜想3成立. |
5.下列物质中,属于有机物的是( )
①烧碱 ②淀粉 ③蔗糖 ④甲烷 ⑤蛋白质 ⑥草木灰.
①烧碱 ②淀粉 ③蔗糖 ④甲烷 ⑤蛋白质 ⑥草木灰.
| A. | ①②③④⑤⑥ | B. | ②③④⑤ | C. | ③④⑤⑥ | D. | ①③④⑤ |
 乙醚是人类很早就使用的有机麻醉剂,分子结构如图所示,其中短线表示原子间的连接(例如水分子的结构可表示为H-O-H).根据乙醚的结构式回答有关问题;
乙醚是人类很早就使用的有机麻醉剂,分子结构如图所示,其中短线表示原子间的连接(例如水分子的结构可表示为H-O-H).根据乙醚的结构式回答有关问题;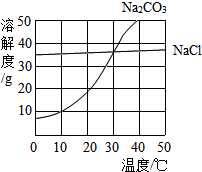 (1)30℃时,氯化钠的溶解度=碳酸钠的溶解度(填写“>”、“<”或“=”);
(1)30℃时,氯化钠的溶解度=碳酸钠的溶解度(填写“>”、“<”或“=”);
