11.已知一铜、锌合金粉末,加入到AgNO3溶液中,如果过滤后得到的固体中物质的种类为a,滤液中溶质的种类为b,则下列说法正确的是( )
| A. | 若a+b=3,则滤液中一定不含AgNO3 | |
| B. | 若a+b=4,则滤纸上一定有Ag和Cu,滤液中一定含有Zn(NO3)2和Cu(NO3)2 | |
| C. | 若溶液呈蓝色,则a=1 | |
| D. | 若向固体中滴加稀盐酸,有气泡产生,则a+b=4 |
10. 如图为某固体饱和溶液的浓度随温度变化的曲线.该固体从溶液中析出时不带结晶水.M、N两点分别表示该固体形成的两份溶液在不同温度时的浓度.当条件改变时,溶液新的状态在图中对应的点的位置可能也随之变化,其中判断错误的是( )
如图为某固体饱和溶液的浓度随温度变化的曲线.该固体从溶液中析出时不带结晶水.M、N两点分别表示该固体形成的两份溶液在不同温度时的浓度.当条件改变时,溶液新的状态在图中对应的点的位置可能也随之变化,其中判断错误的是( )
 如图为某固体饱和溶液的浓度随温度变化的曲线.该固体从溶液中析出时不带结晶水.M、N两点分别表示该固体形成的两份溶液在不同温度时的浓度.当条件改变时,溶液新的状态在图中对应的点的位置可能也随之变化,其中判断错误的是( )
如图为某固体饱和溶液的浓度随温度变化的曲线.该固体从溶液中析出时不带结晶水.M、N两点分别表示该固体形成的两份溶液在不同温度时的浓度.当条件改变时,溶液新的状态在图中对应的点的位置可能也随之变化,其中判断错误的是( )| A. | 保持温度不变,蒸发溶剂时,先是M点不动,N点向左平移至曲线;继续蒸发溶剂,M、N点都不动 | |
| B. | 都升温10℃后,M、N点均向右平移 | |
| C. | 都降温10℃后,M点沿曲线向左下移,N点向左平移 | |
| D. | 保持温度不变,加水稀释时,M、N点均向下移动 |
9.向盛有10% Ca(NO3)2溶液的烧杯中滴加10%的Na2CO3溶液,至Ca(NO3)2和Na2CO3恰好反应完全时生成沉淀10g,过滤,并将滤液蒸发掉90g水后,溶液中溶质的质量分数是( )
| A. | 16% | B. | 10% | C. | 9.2% | D. | 6.5% |
8.金属冶炼就是把化合态变成游离态的过程,为了得到金属单质,某兴趣小组成员设想利用H2把自然界中CuO和Fe2O3混合物中的Cu和Fe冶炼出来,取100克该混合物,其中氧的质量分数为16%,用H2充分反应后最多能得H2O的质量是( )
| A. | 16克 | B. | 9克 | C. | 36克 | D. | 18克 |
7.白酒、食醋、蔗糖、淀粉等均为家庭厨房中常用的物质,利用这些物质能完成的实验是( )
①检验自来水中是否含氯离子 ②鉴别食盐和小苏打③蛋壳能否溶于酸 ④白酒中是否含甲醇.
①检验自来水中是否含氯离子 ②鉴别食盐和小苏打③蛋壳能否溶于酸 ④白酒中是否含甲醇.
| A. | ①② | B. | ①④ | C. | ②③ | D. | ③④ |
6.下列实验操作正确的是( )
| A. | 将氢氧化钠固体放在滤纸上称量 | |
| B. | 用10mL量筒量取8.58mL蒸馏水 | |
| C. | 氯化钠、硝酸银、碳酸钠三种无色溶液可以用稀盐酸来鉴别 | |
| D. | 制取氧气时,用二氧化锰与过氧化氢溶液在常温下反应,并用向下排空气法收集 |
2.某同学测定硫酸铜晶体(CuSO4•5H2O)里结晶水的含量,请回答下列问题:
(1)实验步骤为:①研磨 ②称量空坩埚和装有试样的坩埚的质量 ③加热 ④冷却 ⑤称量 ⑥重复③至⑤的操作,直到连续两次称量的质量差不超过0.1g为止 ⑦根据实验数据计算硫酸铜结晶水的含量.现有坩埚、坩埚钳、三脚架、泥三角、研钵、玻璃棒、干燥器、药匙、酒精灯、火柴、硫酸铜晶体样品等实验用品,进行该实验时,缺少的实验用品是托盘天平.实验步骤⑥的目的是使硫酸铜晶体中的结晶水完全失去.
(2)细心的同学发现在加热硫酸铜晶体时,会闻到刺激性气味,那分解的产物是什么呢?
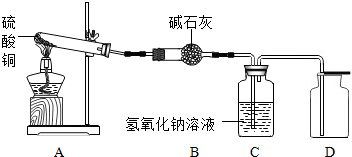
查阅资料发现:硫酸铜受热分解生成氧化铜和气体,气体是由SO2、SO3、O2中的一种或几种;SO2、SO3都能被碱石灰(氢氧化钠和氧化钙混合物)吸收,SO2、SO3都能被氢氧化钠溶液吸收.同学利用如图装置探究硫酸铜受热分解生成的气体的成分(假设加热硫酸铜粉末直至完全分解).实验结果发现:用带火星的木条伸入集气瓶D,发现木条能复燃,说明气体中含有O2.已知硫酸铜粉末质量为10.0克,完全分解后,各装置的质量变化关系如下表所示:
请通过计算,推断出该实验条件下硫酸铜分解的化学方程式是哪一个?B
A.3CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$3CuO+SO3↑+2SO2↑+O2↑ B.4CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$4CuO+2SO3↑+2SO2↑+O2↑
C.5CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$5CuO+SO3↑+4SO2↑+2O2↑ D.6CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$6CuO+4SO3↑+2SO2↑+O2↑
0 166648 166656 166662 166666 166672 166674 166678 166684 166686 166692 166698 166702 166704 166708 166714 166716 166722 166726 166728 166732 166734 166738 166740 166742 166743 166744 166746 166747 166748 166750 166752 166756 166758 166762 166764 166768 166774 166776 166782 166786 166788 166792 166798 166804 166806 166812 166816 166818 166824 166828 166834 166842 211419
(1)实验步骤为:①研磨 ②称量空坩埚和装有试样的坩埚的质量 ③加热 ④冷却 ⑤称量 ⑥重复③至⑤的操作,直到连续两次称量的质量差不超过0.1g为止 ⑦根据实验数据计算硫酸铜结晶水的含量.现有坩埚、坩埚钳、三脚架、泥三角、研钵、玻璃棒、干燥器、药匙、酒精灯、火柴、硫酸铜晶体样品等实验用品,进行该实验时,缺少的实验用品是托盘天平.实验步骤⑥的目的是使硫酸铜晶体中的结晶水完全失去.
(2)细心的同学发现在加热硫酸铜晶体时,会闻到刺激性气味,那分解的产物是什么呢?
查阅资料发现:硫酸铜受热分解生成氧化铜和气体,气体是由SO2、SO3、O2中的一种或几种;SO2、SO3都能被碱石灰(氢氧化钠和氧化钙混合物)吸收,SO2、SO3都能被氢氧化钠溶液吸收.同学利用如图装置探究硫酸铜受热分解生成的气体的成分(假设加热硫酸铜粉末直至完全分解).实验结果发现:用带火星的木条伸入集气瓶D,发现木条能复燃,说明气体中含有O2.已知硫酸铜粉末质量为10.0克,完全分解后,各装置的质量变化关系如下表所示:

| 装置 | A(试管+粉末) | B | C |
| 反应前 | 42.0克 | 75.0克 | 140.0克 |
| 反应后 | 37.0克 | 79.5克 | 140.0克 |
A.3CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$3CuO+SO3↑+2SO2↑+O2↑ B.4CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$4CuO+2SO3↑+2SO2↑+O2↑
C.5CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$5CuO+SO3↑+4SO2↑+2O2↑ D.6CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$6CuO+4SO3↑+2SO2↑+O2↑