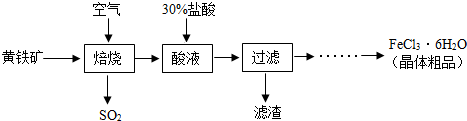
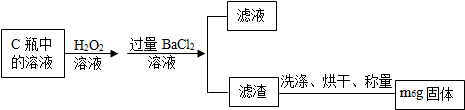
3.工业铁红的主要成分是Fe2O3,还含有少量的FeO、Fe3O4.为了测定铁红中铁的质量分数,兴趣小组的同学进行了如下实验,请你参与过程分析.
【资料1】草酸晶体(H2C2O4•3H2O)在浓H2SO4作用下受热分解,化学方程式为:
H2C2O4•3H2O$→_{△}^{浓H_{2}SO_{4}}$ CO2↑+CO↑+4H2O
(1)下列可用作草酸分解制取气体的装置是d(填字母编号).

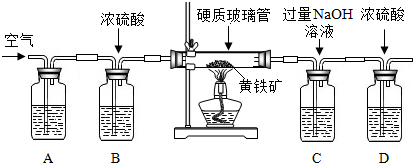
【问题讨论】用图所示装置进行实验:

(2)实验前应先检查装置的气密性.
(3)进入D中的气体是纯净、干燥的CO,则A、C中的试剂依次是c、a(填字母编号).
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
(4)B装置的作用是验证二氧化碳已除尽.
(5)对D装置加热前和停止加热后,都要通入过量的CO,其作用分别是:
①加热前将装置中的空气排出,防止发生爆炸. ②停止加热后驱赶装置中滞留的二氧化碳,使其全部被E装置中碱石灰全部吸收.
(6)写出D装置中所发生反应的一个化学方程式3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
【数据分析与计算】
【资料2】
铁的常见氧化物中铁的质量分数:
(7)称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数.
①D中充分反应后得到Fe粉的质量为m g,则7.0<m<7.78.
②实验前后称得E装置增重6.6g,则此铁红中铁的质量分数是76.0%.
【实验评价】
反思1:本实验中如果缺少C装置(不考虑其它因素),则测得样品中铁的质量分数会偏小(填“偏小”、“不变”或“偏大”).
反思2:请指出问题讨论】中实验装置的一个明显缺陷缺少尾气处理装置.
【资料1】草酸晶体(H2C2O4•3H2O)在浓H2SO4作用下受热分解,化学方程式为:
H2C2O4•3H2O$→_{△}^{浓H_{2}SO_{4}}$ CO2↑+CO↑+4H2O
(1)下列可用作草酸分解制取气体的装置是d(填字母编号).

【问题讨论】用图所示装置进行实验:

(2)实验前应先检查装置的气密性.
(3)进入D中的气体是纯净、干燥的CO,则A、C中的试剂依次是c、a(填字母编号).
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
(4)B装置的作用是验证二氧化碳已除尽.
(5)对D装置加热前和停止加热后,都要通入过量的CO,其作用分别是:
①加热前将装置中的空气排出,防止发生爆炸. ②停止加热后驱赶装置中滞留的二氧化碳,使其全部被E装置中碱石灰全部吸收.
(6)写出D装置中所发生反应的一个化学方程式3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
【数据分析与计算】
【资料2】
铁的常见氧化物中铁的质量分数:
| 铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 铁的质量分数 | 77.8% | 70.0% | 72.4% |
①D中充分反应后得到Fe粉的质量为m g,则7.0<m<7.78.
②实验前后称得E装置增重6.6g,则此铁红中铁的质量分数是76.0%.
【实验评价】
反思1:本实验中如果缺少C装置(不考虑其它因素),则测得样品中铁的质量分数会偏小(填“偏小”、“不变”或“偏大”).
反思2:请指出问题讨论】中实验装置的一个明显缺陷缺少尾气处理装置.
2.如图为某化工企业生产流程示意图:
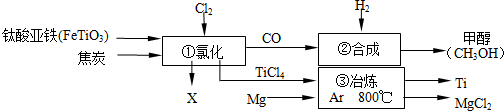
下列说法不正确的是( )

下列说法不正确的是( )
| A. | 钛酸亚铁(FeTiO3)中钛元素为+4价 | |
| B. | ①中反应为:2FeTiO3+6C+7Cl2═2X+2TiCl4+6CO,则X为FeCl3 | |
| C. | ③中氩气(Ar)作保护气,反应类型为置换反应 | |
| D. | ②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为1:2 |
18.区分下列物质的方法不正确的是( )
| A. | 用熟石灰区分氯化铵和氯化钾 | |
| B. | 用水区分硝酸铵和蔗糖固体 | |
| C. | 用稀硫酸溶液区分黄铜(Cu、Zn)和黄金 | |
| D. | 用硝酸钡区分稀硫酸和硫酸钠溶液 |
17.下列关于氧气的说法中错误的是( )
| A. | 氧气约占空气总体积的$\frac{1}{5}$ | |
| B. | 氧气供给呼吸,它和体内物质反应,释放能量,维持生命活动的需要 | |
| C. | 氧气可以支持燃烧,说明氧气具有可燃性 | |
| D. | 夏天鱼池内需要增氧,是因为温度升高,氧气在水中的溶解度减小 |
16.根据物质分类的知识判断,下列生活中的物质属于单质的是( )
| A. | 用作食品保护的氮气 | B. | 加碘盐 | ||
| C. | 食醋 | D. | 发酵粉 |
15.松花蛋,又称皮蛋、卞蛋.其中一种加工工艺的主要原料配方为:鸭蛋10Kg,水10Kg,生石灰1.2Kg,纯碱0.53Kg,食盐0.35Kg.加工时,将纯碱、食盐加入容器中,加沸水溶解,再慢慢加入生石灰充分反应,冷却后得到料液,再加入鸭蛋浸渍.
请回答下列问题:
(1)鸭蛋中富含的营养素有水和蛋白质.
(2)生石灰加入沸水中,水能持续保持沸腾,其原因是氧化钙与水反应能放出大量的热.
(3)静置后,取少量的上层料液,稀释后滴加无色酚酞试液,料液应变为红色
(4)同学们对上层料液的成分产生了兴趣,请你一起参加他们的探究活动.
【提出问题】料液中含有哪些溶质?
【交流讨论】①一定含有NaOH、NaCl
②可能还含有其它溶质:甲同学推断只有Ca(OH)2,乙同学推断只有Na2CO3,丙同学推断有Ca(OH)2、也有Na2CO3
通过进一步讨论,大家一致认为丙同学的推断是错误的,理由是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH(用化学方程式表示).
【实验探究】
【探究结论】甲同学的推断是正确的.
【知识应用】①皮蛋食用时加入一些食醋,可以去除氨味和涩感,原因是酸碱起中和反应.
②料液中起主要作用的是烧碱.现行配方中,直接用烧碱代替石灰和纯碱作用生成的烧碱.若加工10Kg的鸭蛋,需要烧碱的质量是多少千克?(请写出计算过程)
请回答下列问题:
(1)鸭蛋中富含的营养素有水和蛋白质.
(2)生石灰加入沸水中,水能持续保持沸腾,其原因是氧化钙与水反应能放出大量的热.
(3)静置后,取少量的上层料液,稀释后滴加无色酚酞试液,料液应变为红色
(4)同学们对上层料液的成分产生了兴趣,请你一起参加他们的探究活动.
【提出问题】料液中含有哪些溶质?
【交流讨论】①一定含有NaOH、NaCl
②可能还含有其它溶质:甲同学推断只有Ca(OH)2,乙同学推断只有Na2CO3,丙同学推断有Ca(OH)2、也有Na2CO3
通过进一步讨论,大家一致认为丙同学的推断是错误的,理由是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH(用化学方程式表示).
【实验探究】
| 实验步骤 | 实验现象 |
| 取少量上层料液,滴加稀盐酸 | 无明显现象 |
| 另取少量上层料液,滴加碳酸钠溶液 | 产生白色沉淀 |
【知识应用】①皮蛋食用时加入一些食醋,可以去除氨味和涩感,原因是酸碱起中和反应.
②料液中起主要作用的是烧碱.现行配方中,直接用烧碱代替石灰和纯碱作用生成的烧碱.若加工10Kg的鸭蛋,需要烧碱的质量是多少千克?(请写出计算过程)
14.氧化铁和氧化铜的固体混合粉末X克,高温下用足量的CO还原,得到金属混合物2.4克,将生成的CO2气体用足量的澄清石灰水吸收后,产生5克白色沉淀,则原固体混合粉末中氧化铁与氧化铜的质量比为( )
0 166310 166318 166324 166328 166334 166336 166340 166346 166348 166354 166360 166364 166366 166370 166376 166378 166384 166388 166390 166394 166396 166400 166402 166404 166405 166406 166408 166409 166410 166412 166414 166418 166420 166424 166426 166430 166436 166438 166444 166448 166450 166454 166460 166466 166468 166474 166478 166480 166486 166490 166496 166504 211419
| A. | 4:1 | B. | 2:3 | C. | 1:2 | D. | 1:1 |