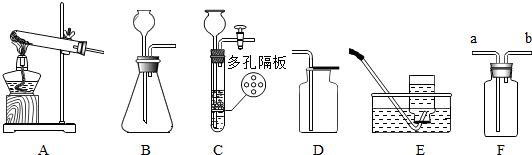
5.除去下列物质中混有的少量杂质,所选用的试剂及操作方法正确的是( )
| 序号 | 物质 | 杂质(少量) | 除去杂质的方法 |
| A | O2 | 水蒸气 | 通过NaOH溶液 |
| B | 铁粉 | 硫酸铜 | 溶解,过滤,洗涤、干燥 |
| C | NaCl溶液 | Na2CO3 | 加入适量的稀HCl |
| D | CO2 | CH4 | 通入O2点燃后,再经过浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |
4.下列实验现象的描述正确的是( )
| A. | 用玻璃尖嘴导管点燃H2,火焰呈淡蓝色,放出大量的热 | |
| B. | 光亮的铁丝插入到硫酸铜溶液中,铁丝表面有红色固体出现 | |
| C. | 二氧化碳通入氯化钙溶液中,溶液会变浑浊 | |
| D. | 将红色的石蕊试纸与氨气接触会变成蓝色 |
3.某研究小组设立研究课题:选用大理石与稀硫酸反应制取二氧化碳,选择合适浓度的硫酸和适当的反应温度进行制取.
Ⅰ.选择合适浓度的硫酸.在28℃时,采用控制变量法进行实验,记录15分钟内生成气体的体积,如下表:
Ⅱ.选择合适的反应温度.在合适的硫酸浓度下采用控制变量法进行实验,观察反应的情况,记录如下表:
分析以上数据,回答问题:
(1)在28℃时,选用硫酸的浓度最合适为25%,因为浓度小于或大于合适浓度对反应的影响是生成气体体积较少.
(2)在合适的硫酸浓度下,应选择最合适的反应温度为70℃,理由是温度过低反应过慢,温度过高反应剧烈,不利于收集气体.
(3)在最合适反应条件时,硫酸与大理石反应的化学方程式为CaCO3+H2SO4═CaSO4+CO2↑+H2O.
(4)除选用适当的温度和合适浓度的硫酸之外,在反应过程中,为防止硫酸钙覆盖在大理石上,应增加摇动试管(或摇动装置)操作,更有利于气体的制备.
Ⅰ.选择合适浓度的硫酸.在28℃时,采用控制变量法进行实验,记录15分钟内生成气体的体积,如下表:
| 试管编号 | 1 | 2 | 3 | 4 | 5 |
| 硫酸浓度(%) | 15 | 20 | 25 | 30 | 35 |
| 气体体积(mL) | 35 | 47 | 55 | 51 | 42 |
| 试管编号 | A | B | C | D | E |
| 温度(℃) | 40 | 50 | 60 | 70 | 80 |
| 现象和比较 | 有少量气泡 | 气泡比A号试管多 | 气泡明显比B号试管多 | 大量气泡产生,与常温盐酸反应相似 | 反应剧烈,迅速产生较多气体 |
(1)在28℃时,选用硫酸的浓度最合适为25%,因为浓度小于或大于合适浓度对反应的影响是生成气体体积较少.
(2)在合适的硫酸浓度下,应选择最合适的反应温度为70℃,理由是温度过低反应过慢,温度过高反应剧烈,不利于收集气体.
(3)在最合适反应条件时,硫酸与大理石反应的化学方程式为CaCO3+H2SO4═CaSO4+CO2↑+H2O.
(4)除选用适当的温度和合适浓度的硫酸之外,在反应过程中,为防止硫酸钙覆盖在大理石上,应增加摇动试管(或摇动装置)操作,更有利于气体的制备.
1.下列实验操作中错误的是( )
| A. |  闻气味方法 | B. | 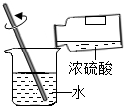 稀释浓硫酸 | ||
| C. | 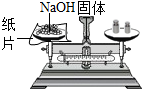 称量氢氧化钠质量 | D. | 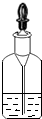 滴管用后不洗涤直接放回原瓶 |
20.2015年5月12日15时05分在尼泊尔发生7.5级地震,在地震灾区为防止疟疾传染,河水需处理后方可饮用.常用的处理方法有:①加热煮沸,②过滤,③投药消毒,④自然沉降.较合理的顺序为( )
0 164576 164584 164590 164594 164600 164602 164606 164612 164614 164620 164626 164630 164632 164636 164642 164644 164650 164654 164656 164660 164662 164666 164668 164670 164671 164672 164674 164675 164676 164678 164680 164684 164686 164690 164692 164696 164702 164704 164710 164714 164716 164720 164726 164732 164734 164740 164744 164746 164752 164756 164762 164770 211419
| A. | ③②④① | B. | ③①④② | C. | ④②③① | D. | ④①③② |