题目内容
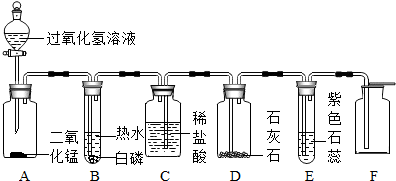
2.请根据图1回答问题:
(1)标号①②的仪器名称:①铁架台,铁架台,②长颈漏斗.
(2)实验室选用A、D装置制取O2,写出用该装置的化学方程式2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑气体收集完毕时,应先从水中取出导气管.
(3)选择发生装置B和收集装置C(选填序号)可以用于实验室制取CO2,若将发生装置由B改为F,其优点是控制反应的发生或停止.
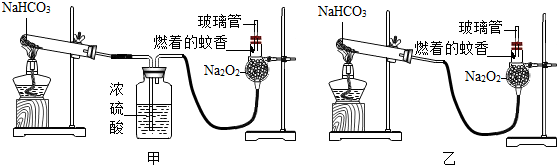
(4)为了得到纯净、干燥的CO2,除杂、干燥装置(如图2)的导管按气流方向连接顺序是_4→3→1→2(选填序号).
分析 (1)认识常用的化学仪器;
(2)根据制取装置来确定制取原理,根据制备和收集氧气的注意事项来分析;
(3)根据二氧化碳的性质以及实验装置的特点来分析;
(4)在除去水和HCl的时候,要先除去HCl,再除水,据此解答即可.
解答 解:(1)①是铁架台,②是长颈漏斗;故填:铁架台;长颈漏斗;
(2)A是加热固体制取氧气,试管口没棉花团,则是加热氯酸钾和二氧化锰的混合物,因为加热高锰酸钾制取氧气需要在试管口放置一棉花团,以防高锰酸钾颗粒进入导管;排水法收集氧气完毕后,应先将导管从水槽中取出,再熄灭酒精灯,以免冷水倒吸炸裂试管;故填:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑;从水中取出导气管;
(3)二氧化碳能溶于水,密度比空气大,所以只能用向上排空气法来收集,若将发生装置由B改为F,其优点是随时控制反应的发生和停止(或随开随用,随关随停).故填:C;控制反应的发生或停止;
(4)实验室制取二氧化碳使用的是碳酸钙与稀盐酸反应,能生成氯化钙、水和二氧化碳,要先除去HCl再除水,故先通过G再通过F,需要从长管进,短管出,故填:4→3→1→2.
点评 本题考查了实验室气体的制取,完成此题,可以依据已有的知识进行.要求同学们熟练掌握气体发生装置的选择以及收集装置的选择依据,以便灵活应用.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
20.在铁制品上连接比铁活泼的金属是防止铁生锈的方法之一,下列金属可行的是( )
| A. | Ag | B. | Pb(铅) | C. | Cu | D. | Zn |
13.溶液与我们的生活息息相关.下列说法不正确的是( )
| A. | 配制5%的硫酸溶液的一般步骤是计算、量取和稀释 | |
| B. | 氢氧化钠溶液能导电是由于溶液中含有钠离子和氢氧根离子 | |
| C. | 20℃时NaCl饱和溶液的溶质质量分数为26.5%,则该温度下NaCl的溶解度为36.1g | |
| D. | 消除路面上的积雪可以撒些盐,这样可以使雪较快地融化 |
17.2015年“世界水日”的主题是“水与可持续发展”.下列说法正确的是( )
| A. | 液态水变成水蒸气时,水分子变大 | |
| B. | 过滤和加热均能使硬水转化为软水 | |
| C. | 蒸馏或用活性炭吸附均可使海水转化为淡水 | |
| D. | 水是生命之源,没有水就没有生命 |
12.下列由有关物质用途的说法错误的是( )
| A. | 氮气:用于保存食品 | B. | 金刚石:用于裁玻璃 | ||
| C. | 明矾:用于净水 | D. | 苛性钠:用于改良土壤 |