题目内容
6.归纳与演绎是重要的科学方法,也常用于化学的学习.请根据下列实验装置,回答问题: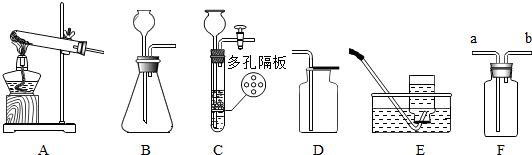
(1)我们已经学过实验室制取氧气、二氧化碳两种气体的反应原理、制取与收集方法,请你归纳出实验室制取这两种气体反应的共同点CD(填代号).
A.需要加热 B.需用催化剂 C.没有气体参加反应 D.生成的气体只有一种
(2)用高锰酸钾制取氧气可选用发生装置是A (填序号,下同),该装置中还缺少的物品是棉花,若某同学用装置F来收集氧气,且进气口为b,在不改变装置连接的情况下,可将装置F倒置或装满水,从而保证收集到一瓶氧气.写出反应的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)实验室制取少量二氧化碳,要随时使反应停止或发生选择的发生装置是C,某同学用装置D收集二氧化碳,因为二氧化碳密度比空气大.
分析 (1)从实验室用加热高锰酸钾或加热氯酸钾的方法制取氧气,也可以用分解过氧化氢的方法制取氧气;实验室用碳酸钙和稀盐酸反应来制取二氧化碳气体.
(2)从用加热高锰酸钾的方法制取氧气,在生成氧气的同时,还有锰酸钾和二氧化锰生成,反应物是固体,且反应条件是加热;实验室用加热分解高锰酸钾的方法制取氧气时,要试管口放一棉花团;
(3)实验室用碳酸钙和稀盐酸反应来制取二氧化碳气体,根据装置特点分析解答.
解答 解:(1)实验室用加热高锰酸钾或加热氯酸钾的方法制取氧气,也可以用分解过氧化氢的方法制取氧气;实验室用碳酸钙和稀盐酸反应来制取二氧化碳气体.
A、实验室制取二氧化碳不用加热;故错误;
B、实验室制取二氧化碳不用催化剂;故错误;
C、由于氧气和二氧化碳都是气体,为防止制取的气体不纯,所以反应物中都不用气体;故正确;
D、为防止收集到的气体不纯,所以生成物中都只有一种气体;故正确;
(2)用加热高锰酸钾的方法制取氧气,在生成氧气的同时,还有锰酸钾和二氧化锰生成,所以化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;由于反应物是固体,且反应条件是加热,所以发生装置应为A;实验室用加热分解高锰酸钾的方法制取氧气时,由于高锰酸钾粉末会随着氧气流进入导管继续进入水槽,使水槽中的水变红,为避免这一现象的发生,往往会要试管口放一棉花团;由于氧气的密度比空气的大,若某同学用装置F来收集氧气,且进气口为b,在不改变装置连接的情况下,可将装置F倒置或装满水;
(3)实验室制取少量二氧化碳,要随时使反应停止或发生选择的发生装置是C,D是向上排空气法收集,用装置D收集二氧化碳,因为二氧化碳密度比空气大.
答案:
(1)CD
(2)A 棉花 倒置或装满水 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)C 二氧化碳密度比空气大
点评 实验室制取气体时,发生装置的选择取决于反应物的状态和反应条件;收集装置的选择取决于水溶性和气体的密度;考查了实验室制取氧气的反应原理,及注意事项,是考试的重点也是中考的重点.

 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案| 实验目的 | 操作所用试剂 | |
| A | 除去NaCl固体中混有的MgSO4 | 溶解、适量BaCl2溶液、过滤、蒸发 |
| B | 除去CO中混有的CO2 | NaOH溶液、浓H2SO4 |
| C | 除去CaCl2溶液中混有的少量盐酸 | 加入过量CaCO3后再过滤 |
| D | 鉴别硝酸铵与食盐固体 | 水 |
| A. | A | B. | B | C. | C | D. | D |
| A. |  闻气味方法 | B. | 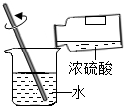 稀释浓硫酸 | ||
| C. | 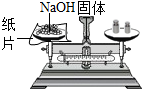 称量氢氧化钠质量 | D. | 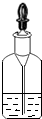 滴管用后不洗涤直接放回原瓶 |
| 选项 | 事实或现象 | 解释 |
| A | 酒香不怕巷子深 | 分子总是在不断运动着 |
| B | 不同的花儿有不同的香味 | 不同的分子性质不同 |
| C | 25m3石油气可加压装入0.024m3的钢瓶中 | 分子间是有间隔的 |
| D | 水银温度计里的水银热胀冷缩 | 分子大小随温度改变而改变 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 对工业污水作处理使之符合排放标准,防止水体污染 | |
| B. | 将废电池填埋,避免重金属污染 | |
| C. | 机动车用压缩天然气替代汽油,减轻空气污染 | |
| D. | 使用微生物降解塑料和光降解塑料,减少白色污染 |