题目内容
7.过氧化钠是一种淡黄色粉末,用于矿山、潜艇、潜水或宇宙飞船等缺氧的场合.它还可以用于消毒、杀菌和漂白等,某化学小组对过氧化钠(Na2O2)用作供氧剂产生了兴趣.【查阅资料】①它能与水反应生成氧气和另一种物质;
②2Na2O2+2CO2═2Na2CO3+O2
③2Na2O2常温下也能与HCl等物质反应生成氧气
实验探究Ⅰ过氧化钠与水反应生成的另一种物质
【实验】将过氧化钠固体溶于水,滴加酚酞试液,试液变红.
有同学对此实验现象,提出猜想:可能生成①NaOH ②Na2CO3;你觉得不合理的是②,理由是反应物中不含有碳元素,因此不能生成碳酸钠,写出过氧化钠与水反应的化学方程式:2Na2O2+2H2O═4NaOH+O2↑;
实验探究Ⅱ实验室中久置的过氧化钠固体组成
【提出问题】如何证明该固体中含有Na2O2、Na2CO3和NaOH?(本实验不考虑其它成分)
【实验方案】①取适量的样品,溶于适量的水中,并用带火星的木条放在管口,木条复燃,则说明该固体中含有Na2O2;
②继续向上述①所得的溶液中,滴加足量的氯化钙溶液,产生白色沉淀,静置后向上层溶液中滴加酚酞试液,溶液变为红色,则由此得出的结论是:该固体还一定含有碳酸钠;
【反思评价】(1)某同学直接取固体样品,加入稀盐酸,若有气泡产生,则说明原固体粉末中有Na2CO3,有同学认为上述方案存在不足,他的理由是过氧化钠与HCl或与稀盐酸中的水反应也产生气体;
(2)上述探究Ⅱ实验方案中可定量分析该固体中是否有NaOH,测定:样品的质量、生成气体的质量和沉淀碳酸钙的质量,通过计算可得出是否有NaOH.
分析 实验探究Ⅰ
化学反应前后,元素的种类不变,原子的种类、总个数不变;
氢氧化钠溶液显碱性,能使酚酞试液变红色;
根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式;
实验探究Ⅱ
氧气能使带火星的木条复燃;
碳酸钠和氯化钙反应生成白色沉淀碳酸钙和氯化钠;
根据测定的数据可以减小相关方面的计算.
解答 解:实验探究Ⅰ
因为反应物中不含有碳元素,所以不可能生成碳酸钠,因此②不合理;
将过氧化钠固体溶于水,滴加酚酞试液,试液变红,说明过氧化钠和水反应生成氧气的同时,生成了氢氧化钠,反应的化学方程式为:2Na2O2+2H2O═4NaOH+O2↑.
故填:②;反应物中不含有碳元素,因此不能生成碳酸钠;2Na2O2+2H2O═4NaOH+O2↑.
实验探究Ⅱ
①取适量的样品,溶于适量的水中,并用带火星的木条放在管口,木条复燃,则说明该固体中含有Na2O2;
②继续向上述①所得的溶液中,滴加足量的氯化钙溶液,产生白色沉淀,静置后向上层溶液中滴加酚酞试液,溶液变为红色,说明该固体还一定含有碳酸钠,不能说明该固体含有氢氧化钠,因为过氧化钠和水反应能够生成氢氧化钠;
(1)因为过氧化钠与HCl或与稀盐酸中的水反应也产生气体,所以上述方案存在不足;
(2)上述探究Ⅱ实验方案中可定量分析该固体中是否有NaOH,测定:样品的质量、生成气体的质量和沉淀碳酸钙的质量,通过计算可得出是否有NaOH.
故填:带火星的木条;碳酸钠;过氧化钠与HCl或与稀盐酸中的水反应也产生气体;沉淀碳酸钙的.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
15.用下列装置进行实验,不能达到实验目的是( )
| A. |  干燥 CO2 | B. |  收集 O2 | C. | 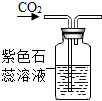 验证 CO2 性质 | D. |  监控气体流速 |
12.下列认识或做法中正确的是( )
| A. | 铁能和稀硫酸、CuSO4溶液、Cu(OH)2发生置换反应 | |
| B. | NaOH能和盐酸、CuSO4溶液、K2SO4溶液反应 | |
| C. | 用过量的CaO除去CaCl2溶液中的盐酸 | |
| D. | 借助酚酞试液可完成稀盐酸、NaCl溶液、NaOH溶液、K2CO3(草木灰的主要成分)溶液间的鉴别 |
19.某同学对下列四个实验都设计了两种方案,其中两个方案都合理的是( )
| 选项 | A | B | C | D |
| 实验 目的 | 鉴别NaOH和 Na2CO3 | 除去NaOH溶液中少量的Na2CO3 | 除去氧化钙中的碳酸钙 | 除去氯化铁溶液中的盐酸 |
| 方案1 | 加水溶解,看是否放热 | 加适量Ca(OH)2溶液,过滤 | 高温煅烧 | 加过量铁粉,过滤 |
| 方案2 | 加入盐酸,看是否有气泡产生 | 加适量的氯化钙溶液,过滤 | 加适量稀盐酸,过滤 | 加过量氧化铁,过滤 |
| A. | A | B. | B | C. | C | D. | D |
16.下列有关食品安全的做法正确的是( )
| A. | 用小苏打焙制糕点 | B. | 用甲醛溶液浸泡海产品 | ||
| C. | 用“地沟油”烹调食物 | D. | 用霉变的花生榨食用油 |
 2015年1月起,国内重型柴油车普推国Ⅳ排放标准.减排的原理为:向反应罐内
2015年1月起,国内重型柴油车普推国Ⅳ排放标准.减排的原理为:向反应罐内