10.我国首创以铝-空气-海水为能源的新型电池.以海水为电解液,靠空气中的氧气使铝不断氧化而产生电流.只要把灯放入海水中数秒钟,就会发出耀眼的白光.电极材料负极用的是铝,总反应为4Al+3O2+6H2O═4Al(OH)3,此反应属于( )
| A. | 分解反应 | B. | 化合反应 | C. | 置换反应 | D. | 复分解反应 |
9.2015年11月,国产大型客机C919在上海总装下线,部分机身采用了新型的铝锂合金,这种材料具有较高的强度和适宜的延展性,铝锂合金中的铝(Al)元素和锂(Li)元素的本质区别是( )
| A. | 原子质量不同 | B. | 元素符号不同 | ||
| C. | 原子核外的电子数不同 | D. | 原子核内的质子数不同 |
8.继黄金、白金之后,钯金(Pd)首饰在市场上悄然兴起,为了获得钯金,取17.7%的PdCl2溶液100g,加入10.0g铁粉使其充分反应得到钯金和铁的氧化物,经分析所得钯金的质量为10.6g.未反应的铁粉质量为4.4g,下列说法正确的是( )
| A. | 生成铁的氯化物质量为12.7g | B. | 生成铁的氯化物质量为16.25g | ||
| C. | 生成铁的氯化物为FeCl2和FeCl3 | D. | 生成铁的氯化物为FeCl3 |
4.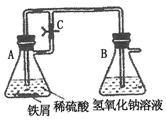 某研究性学习小组在研究由Fe2+制备Fe(OH)2的过程中,设计了如下实验方案:
某研究性学习小组在研究由Fe2+制备Fe(OH)2的过程中,设计了如下实验方案:
按照如图进行实验,容器A中的反应开始时,活塞C处于打开状态,一段时间后,关闭活塞C,容器A中的反应仍在进行.最终在B容器中观察到白色沉淀(填“A”或“B”)
【探究思考】实验表明上述实验中出现白色的沉淀会逐渐转变为灰绿色或绿色,那么如何解释出现灰绿色或绿色的现象呢?
(1)甲同学查阅资料后,得到Fe(OH)2如下信息:
阅读该资料后,你对上述实验中出现灰绿色或绿色的现象的解释是:由于Fe(OH)2部分被氧化,混入少量的Fe(OH)3
资料中提及的微绿色Fe3(OH)8,用氧化物的形式表示可写成FeO•Fe2O3•4H2O.
(2)乙同学依据配色原理:白色和棕色不可能调配成绿色或灰绿色的常识,认为绿色可能是形成Fe(OH)2•nH2O所致.用热水浴的方式加热“方法一”中生成的绿色沉淀,观察到沉淀由绿变白的趋势.
加热时,“方法一”中弹簧夹C应处于打开状态,容器A中的反应须处于发生状态.该实验中支持乙同学观点的化学方程式:Fe(OH)2•nH2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)2+nH2O.
(3)欢迎你参加该研究小组的讨论,请提出一种在研究由Fe2+制备Fe(OH)2的过程中,有助于对沉淀由“白”变“绿”的现象进行合理解释的实验设计新思路.向Fe2+和Fe3+的混合液中加入NaOH溶液后,观察生成的沉淀的颜色是否为灰绿色.
 某研究性学习小组在研究由Fe2+制备Fe(OH)2的过程中,设计了如下实验方案:
某研究性学习小组在研究由Fe2+制备Fe(OH)2的过程中,设计了如下实验方案:按照如图进行实验,容器A中的反应开始时,活塞C处于打开状态,一段时间后,关闭活塞C,容器A中的反应仍在进行.最终在B容器中观察到白色沉淀(填“A”或“B”)
【探究思考】实验表明上述实验中出现白色的沉淀会逐渐转变为灰绿色或绿色,那么如何解释出现灰绿色或绿色的现象呢?
(1)甲同学查阅资料后,得到Fe(OH)2如下信息:
| 资料名称 | 物理性质描述 | 化学性质描述 |
| 《化学辞典》,顾翼东编,1989年版P637 | 白色无定形粉末或白色至淡绿色六方晶体 | 与空气接触易被氧化,将细粉喷于空气中,则立即燃烧出火花 |
| 《大学普通化学(下册)》傅鹰著P637 | 白色沉淀 | 此沉淀易被氧化成微绿色Fe3(OH)8 |
| 《普通化学教程》(下册)P788 | 白色 | 能强烈吸收O2,迅速变成棕色Fe(OH)3.这时作为氧化的中间产物为土绿色,其中含有Fe2+、Fe3+. |
资料中提及的微绿色Fe3(OH)8,用氧化物的形式表示可写成FeO•Fe2O3•4H2O.
(2)乙同学依据配色原理:白色和棕色不可能调配成绿色或灰绿色的常识,认为绿色可能是形成Fe(OH)2•nH2O所致.用热水浴的方式加热“方法一”中生成的绿色沉淀,观察到沉淀由绿变白的趋势.
加热时,“方法一”中弹簧夹C应处于打开状态,容器A中的反应须处于发生状态.该实验中支持乙同学观点的化学方程式:Fe(OH)2•nH2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)2+nH2O.
(3)欢迎你参加该研究小组的讨论,请提出一种在研究由Fe2+制备Fe(OH)2的过程中,有助于对沉淀由“白”变“绿”的现象进行合理解释的实验设计新思路.向Fe2+和Fe3+的混合液中加入NaOH溶液后,观察生成的沉淀的颜色是否为灰绿色.
2.我国化工专家侯德榜的“侯氏制碱法”为世界制碱 工业做出了突出的贡献.他以食盐、水、氨气、二氧化碳为原料,先制得碳酸氢钠和氯化铵,进而生产出纯碱.下表是几种物质在不同温度时的溶解度:
(1)从表中数据可以看出,温度对NaCl的溶解度影响不大.
(2)要使NH4C1饱和溶液中的NH4C1结晶析出,在较低(填“较高”或“较低”)温度下进行比较合适.
(3)“侯氏制碱法”制NaHCO3的方程式是NaCl+CO2+NH3+H2O═NaHCO3↓+NH4Cl,进而生产出纯碱属于盐(填酸、碱、盐),它的浓溶液与澄清石灰水反应的化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
0 159346 159354 159360 159364 159370 159372 159376 159382 159384 159390 159396 159400 159402 159406 159412 159414 159420 159424 159426 159430 159432 159436 159438 159440 159441 159442 159444 159445 159446 159448 159450 159454 159456 159460 159462 159466 159472 159474 159480 159484 159486 159490 159496 159502 159504 159510 159514 159516 159522 159526 159532 159540 211419
(1)从表中数据可以看出,温度对NaCl的溶解度影响不大.
(2)要使NH4C1饱和溶液中的NH4C1结晶析出,在较低(填“较高”或“较低”)温度下进行比较合适.
(3)“侯氏制碱法”制NaHCO3的方程式是NaCl+CO2+NH3+H2O═NaHCO3↓+NH4Cl,进而生产出纯碱属于盐(填酸、碱、盐),它的浓溶液与澄清石灰水反应的化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
| 0℃ | 20℃ | 40℃ | 60℃ | |
| NaHCO3 | 6.9 | 9.6 | 12.7 | 16.4 |
| NaCl | 35.7 | 35.8 | 36.6 | 37.3 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 |
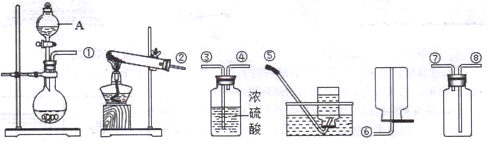
 小明和同学用H2O2溶液制取氧气时,错将KMnO4固体当成MnO2放入了H2O2溶液中,结果也发现溶液中迅速产生气泡.小明想:放出的气体是氧气吗?KMnO4固体是H2O2分解的催化剂吗?
小明和同学用H2O2溶液制取氧气时,错将KMnO4固体当成MnO2放入了H2O2溶液中,结果也发现溶液中迅速产生气泡.小明想:放出的气体是氧气吗?KMnO4固体是H2O2分解的催化剂吗?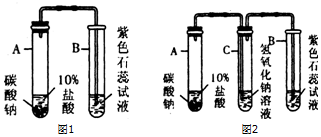
 市售的碳酸氢钠片是一种白色片状药剂,主要成份为碳酸氢钠(NaHCO3),用于缓解胃酸过多引起的胃痛、胃灼热感(烧心)、反酸等有关症状,根据题意,试回答以下问题:
市售的碳酸氢钠片是一种白色片状药剂,主要成份为碳酸氢钠(NaHCO3),用于缓解胃酸过多引起的胃痛、胃灼热感(烧心)、反酸等有关症状,根据题意,试回答以下问题: