题目内容
2.我国化工专家侯德榜的“侯氏制碱法”为世界制碱 工业做出了突出的贡献.他以食盐、水、氨气、二氧化碳为原料,先制得碳酸氢钠和氯化铵,进而生产出纯碱.下表是几种物质在不同温度时的溶解度:(1)从表中数据可以看出,温度对NaCl的溶解度影响不大.
(2)要使NH4C1饱和溶液中的NH4C1结晶析出,在较低(填“较高”或“较低”)温度下进行比较合适.
(3)“侯氏制碱法”制NaHCO3的方程式是NaCl+CO2+NH3+H2O═NaHCO3↓+NH4Cl,进而生产出纯碱属于盐(填酸、碱、盐),它的浓溶液与澄清石灰水反应的化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
| 0℃ | 20℃ | 40℃ | 60℃ | |
| NaHCO3 | 6.9 | 9.6 | 12.7 | 16.4 |
| NaCl | 35.7 | 35.8 | 36.6 | 37.3 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 |
分析 (1)根据表中氯化钠溶解度随温度变化的情况回答.
(2)根据表中氯化钠溶解度随温度变化的情况回答.
(3)根据表中碳酸氢钠在低温下溶解度很小,易结晶析出,形成沉淀物的特点以及盐的特点回答.
解答 解:(1)从表中可以看出,温度对NaHCO3和NH4Cl的溶解度的影响都比较大,对NaCl的溶解度影响不大.
(2)随着温度的升高,NH4Cl的溶解度变大,且受温度变化影响大,可以通过在较高温度下配置NH4Cl的饱和溶液,然后再降温结晶析出NH4Cl的办法将NH4Cl从溶液中分离出来.
(3)NaCl+CO2+NH3+H2O═NaHCO3↓+NH4Cl这个反应能够进行,是因为NaHCO3在水中的溶解度较小,可以结晶析出,相当生成了沉淀,符合复分解反应的基本条件,化学方程式为:NaCl+CO2+NH3+H2O═NaHCO3↓+NH4Cl.纯碱是由钠离子和碳酸根离子构成的,属于盐类物质,碳酸钠能与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
故答案为:(1)NaCl;
(2)较低;
(3)NaCl+CO2+NH3+H2O═NaHCO3↓+NH4Cl;盐;Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
点评 化学来源于生产、生活,又服务于生产、生活,氨碱工业是初中化学重要的应用之一,是考查重点,常涉及化学方程式的书写,二氧化碳和氨气通入的顺序及原因,反应时析出碳酸氢钠的原因与物质溶解度的关系等重点内容.

练习册系列答案
 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案
相关题目
5.下列各组物质中,可直接用过滤的方法将它们分离成两部分的是( )
| A. | 食盐和水形成的溶液 | B. | 食盐水和泥沙形成的悬浊液 | ||
| C. | 食油和水形成的乳浊液 | D. | 酒精和水的混合物 |
10.化学兴趣小组的同学对实验室一瓶没有标签的银白色金属X,展开探究活动.
【实验目的】X在金属活动性顺序中的相对位置关系.
【实验探究】取形状、大小相同的X、Cu、Zn三种金属薄片,用砂纸打磨光亮,分别放入三份等体积、等质量分数的稀硫酸溶液中.
【实验结论】三种金属在金属活动性顺序中的相对位置是锌、X、铜.
【拓展研究】兴趣小组的同学将锌粒放入一定量AgNO3和Mg(NO3)2混合溶液中,反应一段时间后,过滤,对过滤的组成进行探究.
【提出猜想】
①滤液中的溶质为硝酸锌;
②滤液中的溶质为硝酸锌和硝酸镁;
③滤液中的溶质为硝酸银、硝酸锌、硝酸镁;
【交流谈论】你认为猜想①一定不正确,理由是锌不能和硝酸镁反应,滤液中一定含有硝酸镁.
【设计实验】
【实验目的】X在金属活动性顺序中的相对位置关系.
【实验探究】取形状、大小相同的X、Cu、Zn三种金属薄片,用砂纸打磨光亮,分别放入三份等体积、等质量分数的稀硫酸溶液中.
| 实验 | 试管1 | 试管2 | 试管3 |
| 实验操作 |  |  |  |
| 实验现象 | 金属X表面产生气泡缓慢 | 金属锌表面产生气泡较快 | 不产生气泡 |
【拓展研究】兴趣小组的同学将锌粒放入一定量AgNO3和Mg(NO3)2混合溶液中,反应一段时间后,过滤,对过滤的组成进行探究.
【提出猜想】
①滤液中的溶质为硝酸锌;
②滤液中的溶质为硝酸锌和硝酸镁;
③滤液中的溶质为硝酸银、硝酸锌、硝酸镁;
【交流谈论】你认为猜想①一定不正确,理由是锌不能和硝酸镁反应,滤液中一定含有硝酸镁.
【设计实验】
| 实验操作 | 实验现象 | 实验结论 |
| 取少量的滤液于试管中,在滤液中加入 稀盐酸. | 产生白色沉淀 | 猜想③成立 |
12.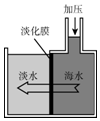 海水淡化可采用膜分离技术.如图所示,对淡化膜右侧的海水加压,水分子可透过淡化膜进入左侧淡水池,而海水中各种溶质不能通过淡化膜,从而得到淡水.对加压后右侧海水成分变化分析正确的是( )
海水淡化可采用膜分离技术.如图所示,对淡化膜右侧的海水加压,水分子可透过淡化膜进入左侧淡水池,而海水中各种溶质不能通过淡化膜,从而得到淡水.对加压后右侧海水成分变化分析正确的是( )
 海水淡化可采用膜分离技术.如图所示,对淡化膜右侧的海水加压,水分子可透过淡化膜进入左侧淡水池,而海水中各种溶质不能通过淡化膜,从而得到淡水.对加压后右侧海水成分变化分析正确的是( )
海水淡化可采用膜分离技术.如图所示,对淡化膜右侧的海水加压,水分子可透过淡化膜进入左侧淡水池,而海水中各种溶质不能通过淡化膜,从而得到淡水.对加压后右侧海水成分变化分析正确的是( )| A. | 溶质质量增加 | B. | 溶液质量增加 | ||
| C. | 溶质的质量不变 | D. | 溶质质量分数减少 |
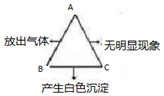 如图所示的A、B、C三种溶液两两混合,发生了化学反应同时产生的实验现象,其中A是初中化学常见的酸,请写出符合实验现象的一组物质的化学式和一个化学方程式.
如图所示的A、B、C三种溶液两两混合,发生了化学反应同时产生的实验现象,其中A是初中化学常见的酸,请写出符合实验现象的一组物质的化学式和一个化学方程式.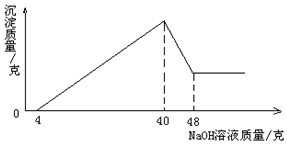 准确称取5克铝土矿(含Al2O3,Fe2O3,SiO2)样品,放入盛有50克某质量分数的硫酸溶液的烧杯中,充分反应后过滤,再向滤液中加入20%的氢氧化钠溶液,产生沉淀的质量与所加入的氢氧化钠溶液质量的关系如图所示.
准确称取5克铝土矿(含Al2O3,Fe2O3,SiO2)样品,放入盛有50克某质量分数的硫酸溶液的烧杯中,充分反应后过滤,再向滤液中加入20%的氢氧化钠溶液,产生沉淀的质量与所加入的氢氧化钠溶液质量的关系如图所示.