题目内容
5.实验探究活动中,小明进行如下实验: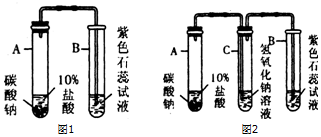
(1)打开两瓶溶质质量分数均为10%的盐酸和硫酸,观察到其中一个试剂瓶瓶口有白雾现象,该试剂瓶盛装的试剂是盐酸;将湿润的蓝色石蕊试纸靠近白雾,将观察到试纸变红.
(2)小明设计如图1装置(固定装置已略去)验证CO2能否与水反应,并认为:如果观察到紫色石蕊试液变红,说明CO2能与水反应并生成酸性物质.
①老师指出:虽然CO2不是酸性物质,但也不能根据石蕊试液变红的现象说明CO2能与水反应并生成酸性物质.为什么?答:紫色石蕊试液遇HCl也能变红色.
②根据老师的提示,小明对实验作如下两种改进:
方案甲:仍用原装置,但用硫酸替代盐酸进行实验.
方案乙:对装置作如图2所示的改进.
上述两科-改进方案中,请你评价哪个实验方案不可行,并说明不可行的原因.乙方案,氢氧化钠溶液不仅吸收HCl,而且也能吸收二氧化碳.
分析 (1)根据盐酸具有挥发性,打开瓶塞会看到白雾,是挥发出的氯化氢气体溶于水形成的盐酸小液滴,可使石蕊变红进行分析;
(2)①根据盐酸挥发的氯化氢气体溶于水显酸性进行分析;
②根据氢氧化钠溶液可与氯化氢气体和二氧化碳反应分析解答.
解答 解:(1)盐酸具有挥发性,打开瓶塞会看到白雾,是挥发出的氯化氢气体溶于水形成的盐酸小液滴,所以该白雾显酸性,可使湿润的蓝色石蕊试纸变红;
(2)①盐酸挥发的氯化氢气体溶于水显酸性,也能使石蕊试液变红,所以该推理是不严密的;
②要检验CO2能与水反应并生成酸性物质,须排除氯化氢气体的干扰,方案甲用硫酸是可行的;方案乙,用氢氧化钠溶液不仅吸收HCl,而且也能吸收CO2,所以是不可行的.
故答案为:(1)试纸变红;
(2)①紫色石蕊试液遇HCl也能变红色;
②乙方案,氢氧化钠溶液不仅吸收HCl,而且也能吸收二氧化碳.
点评 掌握盐酸、硫酸的性质,及二氧化碳和碳酸钠等物质的性质,并能结合所给情景依据相关知识分析和解答是解决问题的关键.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
8.下列仪器常用于物质分离的是( )
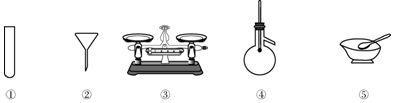

| A. | ①③⑤ | B. | ②③④ | C. | ②④ | D. | ①② |
10.我国首创以铝-空气-海水为能源的新型电池.以海水为电解液,靠空气中的氧气使铝不断氧化而产生电流.只要把灯放入海水中数秒钟,就会发出耀眼的白光.电极材料负极用的是铝,总反应为4Al+3O2+6H2O═4Al(OH)3,此反应属于( )
| A. | 分解反应 | B. | 化合反应 | C. | 置换反应 | D. | 复分解反应 |
17.根据表中数据,求:
(1)第1、2次稀盐酸有剩余;
(2)a=1.7,b=2.2;
(3)样品中碳酸钙的质量分数.(计算结果保留一位小数)
| 实验 | 1 | 2 | 3 | 4 |
| 加入石灰石样品质量/g | 2.5 | 5 | 7.5 | 10 |
| 加入稀盐酸质量/g | 25 | 25 | 25 | 25 |
| 生成CO2质量/g | 0.85 | a | 2.2 | b |
(2)a=1.7,b=2.2;
(3)样品中碳酸钙的质量分数.(计算结果保留一位小数)
14.为了除去粗盐中的Ca2+、Mg2+、SO42-等离子,可将粗盐溶于水后进行如下操作:①加入适量盐酸,②加过量NaOH溶液,③加过量Na2CO3溶液,④加过量BaCl2溶液,⑤过滤.下列操作顺序合理的是( )
| A. | ②③④⑤① | B. | ②④③⑤① | C. | ④②③①⑤ | D. | ④③②①⑤ |