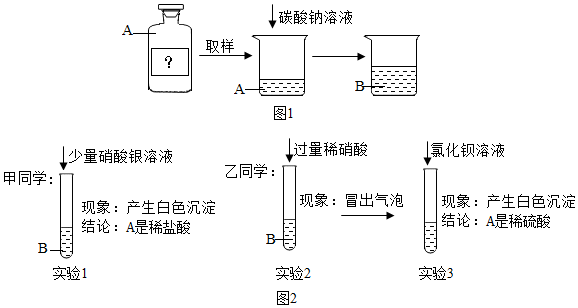
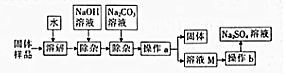
17.一些金属易生锈,某小组同学设计如下实验,对金属锈蚀进行探究.
【实验一】取5枚去油去锈的洁净铁钉,分别装入下表的试管中,进行实验.
(1)通过上述实验可知,温度越高铁钉生锈速率越快(填“慢”或“快”);在酸性(填“酸性”、“碱性”或“中性”)环境中铁钉生锈速率较快.
【实验二】为探究铁锈的成分,用图1所示装置(夹持仪器已省略)进行实验(每步反应和吸收均完全).
【查阅资料】无水硫酸铜能吸收水而变蓝,碱石灰既能吸收水也能吸收CO2.
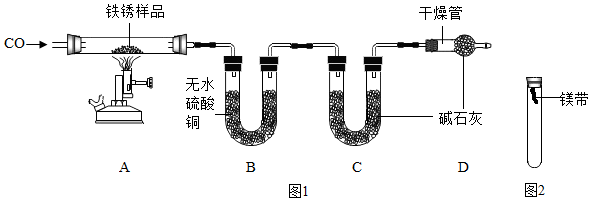
(2)请指出图1所示实验装置的一个明显缺陷:没有进行尾气处理.
(3)加热前,先通入CO一段时间,目的是排尽装置内的空气,防止发生爆炸.
(4)将铁锈样品加热,样品逐渐变黑,无水硫酸铜逐渐变蓝,由此推知铁锈中一定含有氢元素,从而推断出空气中的水参加了铁生锈反应.
【实验记录】
(5)根据上表数据推算,可确定铁锈的成分,用FexOy•nH2O表示,则n=4;若缺少D装置,x:y的值偏小(填“偏大”、“偏小”或“无影响”).
(6)欲通过实验探究镁带在空气中锈蚀的条件,用图2所示装置,试管内可选用的物质如下:
①O2②水③CO2④O2和CO2⑤CO2和水⑥O2和水⑦O2、CO2和水
至少需要选用④⑤⑥⑦(填数字序号),才能达到探究镁带锈蚀的条件.
(7)请写出镁带在空气中锈蚀,生成碱式碳酸镁[Mg3(OH)2(CO3)2]的化学方程式6Mg+3O2+4CO2+2H2O=2Mg3(OH)2(CO3)2.
【实验一】取5枚去油去锈的洁净铁钉,分别装入下表的试管中,进行实验.
| 实验图示 | 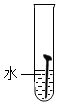 | 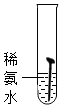 | 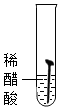 | 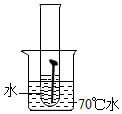 | 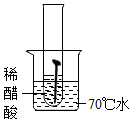 |
| 生锈时间 | 8min | 较长时间不生锈 | 5min | 3min | 1min |
【实验二】为探究铁锈的成分,用图1所示装置(夹持仪器已省略)进行实验(每步反应和吸收均完全).
【查阅资料】无水硫酸铜能吸收水而变蓝,碱石灰既能吸收水也能吸收CO2.

(2)请指出图1所示实验装置的一个明显缺陷:没有进行尾气处理.
(3)加热前,先通入CO一段时间,目的是排尽装置内的空气,防止发生爆炸.
(4)将铁锈样品加热,样品逐渐变黑,无水硫酸铜逐渐变蓝,由此推知铁锈中一定含有氢元素,从而推断出空气中的水参加了铁生锈反应.
【实验记录】
| 铁锈样品的质量/g | 装置B的质量/g | 装置C的质量/g | |
| 反应前 | 23.2 | 232.4 | 198.2 |
| 反应后 | / | 239.6 | 211.4 |
(6)欲通过实验探究镁带在空气中锈蚀的条件,用图2所示装置,试管内可选用的物质如下:
①O2②水③CO2④O2和CO2⑤CO2和水⑥O2和水⑦O2、CO2和水
至少需要选用④⑤⑥⑦(填数字序号),才能达到探究镁带锈蚀的条件.
(7)请写出镁带在空气中锈蚀,生成碱式碳酸镁[Mg3(OH)2(CO3)2]的化学方程式6Mg+3O2+4CO2+2H2O=2Mg3(OH)2(CO3)2.
13.为除去下列物质中的杂质(括号内是杂质),下列操作方法正确的是( )
| 选项 | 物质 | 操作方法 |
| A | Fe(Cu) | 加入过量稀盐酸,充分反应后过滤 |
| B | CaO 粉末(CaCO3 粉末) | 高温煅烧 |
| C | NaOH 溶液(Ca(OH)2 溶液) | 通入 CO2 气体,充分反应后过滤 |
| D | NaCl 溶液(CuSO4 溶液) | 通入过量 Ba(OH)2 溶液,充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |
12.下列图象分别与选项中的操作相对应,其中合理的是( )
| A. |  向一定量氢氧化钠溶液中滴入水 | |
| B. |  向一定量氯化铜溶液中加入一定量铝 | |
| C. |  向一定量盐酸和硫酸钠混合溶液中滴入氢氧化钡溶液 | |
| D. |  向一定量硫酸和硫酸铜混合溶液中滴入氢氧化钠溶液 |
11.向稀盐酸中加入 Z 物质,其 pH 变化情况如图所示,则 Z 物质是( )


| A. | H2O | B. | AgNO3 固体 | C. | 浓盐酸 | D. | KOH 固体 |
10. 经过监测和治理,我省的土壤质量已经得到了很好的改善,但个别地区仍然存在盐碱地.某校化学兴趣小组的同学们为此开展了实践活动,他们采集了本地的土样,并对土样围绕两个问题进行探究
经过监测和治理,我省的土壤质量已经得到了很好的改善,但个别地区仍然存在盐碱地.某校化学兴趣小组的同学们为此开展了实践活动,他们采集了本地的土样,并对土样围绕两个问题进行探究
查阅资料
①枸杞和合欢均可在轻度盐碱地中生存.
②盐碱地显碱性.
③该土样中的可溶性物质只含NaCl,CaCl2和Na2CO3.
探究过程
(1)甲组探究土样的酸碱度
具体操作是取土壤样品于烧杯中,加入蒸馏水搅拌、静置,用玻璃棒蘸取上层清液滴在pH试纸上,将试纸显示颜色与标准比色卡对照,读出pH值,由此得出,该土样的pH>7.
(2)乙组探究土样的成分(如图所示)
向土样中加入足量的蒸馏水,发生反应的化学方程式Na2CO3+CaCl2=CaCO3↓+2NaCl.
同学们对溶液I中的溶质成分很感兴趣,作出如下猜想:
猜想①:只有氯化钠
猜想②:含有氯化钠、氯化钙
猜想③:含有氯化钠、碳酸钠
设计实验,继续探究:
反思与评价:
①通过交流,甲组认为乙组的方案一不太严谨,理由是若溶液中含有氯化钙,滴加AgNO3溶液和稀硝酸,也会产生白色沉淀.
②同学们对沉淀 CaCO3的来源展开了热烈的讨论.一致认为 CaCO3也可能来自土样本身.请解释土样中存在 CaCO3的原因在灌溉或雨水的作用下,碳酸钠和氯化钙也会反应生成碳酸钙沉淀.
总结与提升:
改良我省的盐碱地,充分利用土地资源,造福山西人民,我们任重而道远.以下建议你认为正确的是ac
a.轻度盐碱地可以种植枸杞
b.可以用熟石灰改良盐碱地
c.盐碱地应避免施用碱性化肥.
0 158069 158077 158083 158087 158093 158095 158099 158105 158107 158113 158119 158123 158125 158129 158135 158137 158143 158147 158149 158153 158155 158159 158161 158163 158164 158165 158167 158168 158169 158171 158173 158177 158179 158183 158185 158189 158195 158197 158203 158207 158209 158213 158219 158225 158227 158233 158237 158239 158245 158249 158255 158263 211419
 经过监测和治理,我省的土壤质量已经得到了很好的改善,但个别地区仍然存在盐碱地.某校化学兴趣小组的同学们为此开展了实践活动,他们采集了本地的土样,并对土样围绕两个问题进行探究
经过监测和治理,我省的土壤质量已经得到了很好的改善,但个别地区仍然存在盐碱地.某校化学兴趣小组的同学们为此开展了实践活动,他们采集了本地的土样,并对土样围绕两个问题进行探究查阅资料
①枸杞和合欢均可在轻度盐碱地中生存.
②盐碱地显碱性.
③该土样中的可溶性物质只含NaCl,CaCl2和Na2CO3.
探究过程
(1)甲组探究土样的酸碱度
具体操作是取土壤样品于烧杯中,加入蒸馏水搅拌、静置,用玻璃棒蘸取上层清液滴在pH试纸上,将试纸显示颜色与标准比色卡对照,读出pH值,由此得出,该土样的pH>7.
(2)乙组探究土样的成分(如图所示)
向土样中加入足量的蒸馏水,发生反应的化学方程式Na2CO3+CaCl2=CaCO3↓+2NaCl.
同学们对溶液I中的溶质成分很感兴趣,作出如下猜想:
猜想①:只有氯化钠
猜想②:含有氯化钠、氯化钙
猜想③:含有氯化钠、碳酸钠
设计实验,继续探究:
| 验证猜想所用试剂 | 实验现象 | 实验结果 | |
| 方案一 | AgNO3溶液和稀硝酸 | 由白色沉淀生成 | 猜想①正确 |
| 方案二 | 碳酸钠溶液 | 无明显现象 | 猜想②不正确 |
| 方案三 | 稀盐酸 | 有气泡产生 | 猜想③正确 |
①通过交流,甲组认为乙组的方案一不太严谨,理由是若溶液中含有氯化钙,滴加AgNO3溶液和稀硝酸,也会产生白色沉淀.
②同学们对沉淀 CaCO3的来源展开了热烈的讨论.一致认为 CaCO3也可能来自土样本身.请解释土样中存在 CaCO3的原因在灌溉或雨水的作用下,碳酸钠和氯化钙也会反应生成碳酸钙沉淀.
总结与提升:
改良我省的盐碱地,充分利用土地资源,造福山西人民,我们任重而道远.以下建议你认为正确的是ac
a.轻度盐碱地可以种植枸杞
b.可以用熟石灰改良盐碱地
c.盐碱地应避免施用碱性化肥.