6.中华民族有着光辉灿烂的发明史.下列发明创造或使用中涉及的主要原理不属于化学变化的是( )
| A. | 火药的使用 | B. | 冶炼青铜或生铁 | C. | 陶瓷的烧制 | D. | 磁石磨成指南针 |
3.小明将一定量铜粉和锌粉的混合物放入一定量的硝酸银溶液中,使其充分反应后过滤,得到滤渣和滤液.下列对滤渣组成的分析,不可能出现的一组是( )
0 157720 157728 157734 157738 157744 157746 157750 157756 157758 157764 157770 157774 157776 157780 157786 157788 157794 157798 157800 157804 157806 157810 157812 157814 157815 157816 157818 157819 157820 157822 157824 157828 157830 157834 157836 157840 157846 157848 157854 157858 157860 157864 157870 157876 157878 157884 157888 157890 157896 157900 157906 157914 211419
| A. | Ag | B. | Ag 和 Zn | C. | Cu 和 Ag | D. | Cu、Zn 和 Ag |

 ”和“
”和“ ”表示两种不同的原子.
”表示两种不同的原子.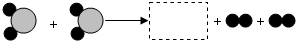
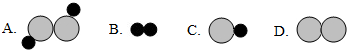
 如图是金属X化学性质网络图(箭头表示转化方向,部分反应物、生成物省略),其中X是目前世界上年产量最高的金属,A是具有磁性的黑色物质,B是可燃性气体,反应③常用于湿法冶金.
如图是金属X化学性质网络图(箭头表示转化方向,部分反应物、生成物省略),其中X是目前世界上年产量最高的金属,A是具有磁性的黑色物质,B是可燃性气体,反应③常用于湿法冶金.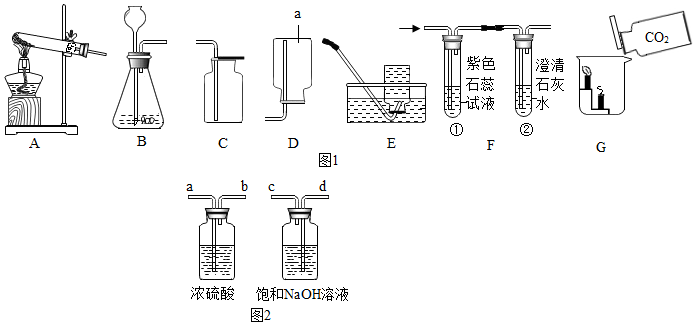
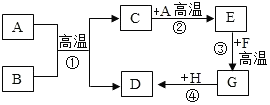 A~H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,H溶液中的溶质是一种盐.它们的转化关系如图所示.请回答:
A~H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,H溶液中的溶质是一种盐.它们的转化关系如图所示.请回答: