题目内容
2.根据下列实验装置图,按要求回答下列问题: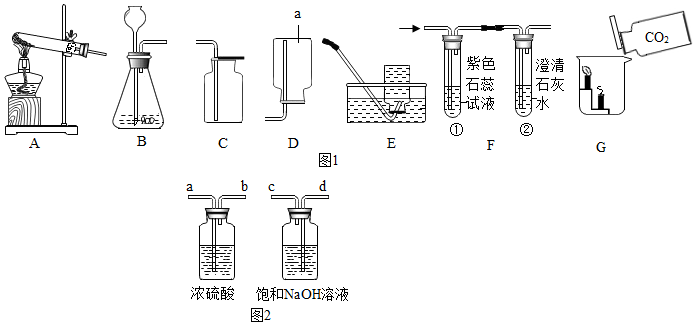
(1)仪器a的名称是集气瓶.
(2)实验室用高锰酸钾制取氧气,反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,应选用的发生和收集装置是AC或AE(填字母序号).
(3)小明同学制取二氧化碳,选用的发生和收集装置是BC(填字母序号).
检验二氧化碳是否收集满方法是将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了,用F装置验证二氧化碳的性质,当通入二氧化碳一段时间后,试管①中产生的现象是紫色变红色; G中观察到蜡烛由低到高依次熄灭,说明二氧化碳具有的性质是二氧化碳既不能燃烧也不能支持燃烧,二氧化碳的密度比空气的密度大.
(4)实验室用盐酸和锌反应制得的氢气中,常含有少量的水蒸气和氯化氢气体,用图2装置可得到干燥、纯净的氢气,
①导管气流方向连接顺序正确的是D(填字母序号).
A.a→b→c→d B.a→b→d→c C.c→d→a→b D.d→c→a→b
②饱和NaOH溶液的作用是吸收并除去氯化氢气体.
分析 集气瓶是收集气体的仪器,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;当通入二氧化碳一段时间后,试管①中产生的现象是紫色变红色;G中观察到蜡烛由低到高依次熄灭,说明二氧化碳具有的性质是:二氧化碳既不能燃烧也不能支持燃烧,二氧化碳的密度比空气的密度大.氢气中常含有少量的水蒸气和氯化氢气体,要先除杂质再干燥,并且是长进短出;饱和NaOH溶液的作用是:吸收并除去氯化氢气体.
解答 解:(1)集气瓶是收集气体的仪器,故答案为:集气瓶;
(2)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;故答案为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;AC或AE;
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;当通入二氧化碳一段时间后,试管①中产生的现象是紫色变红色;G中观察到蜡烛由低到高依次熄灭,说明二氧化碳具有的性质是:二氧化碳既不能燃烧也不能支持燃烧,二氧化碳的密度比空气的密度大;故答案为:BC;将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;紫色变红色,因为二氧化碳和水生成了碳酸;二氧化碳既不能燃烧也不能支持燃烧,二氧化碳的密度比空气的密度大;
(4)氢气中常含有少量的水蒸气和氯化氢气体,要先除杂质再干燥,并且是长进短出;饱和NaOH溶液的作用是:吸收并除去氯化氢气体;故答案为:D;吸收并除去氯化氢气体;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的干燥和除杂等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案| A. | 丙氨酸属于无机化合物 | |
| B. | 丙氨酸中碳、氢元素的质量比为3:1 | |
| C. | 丙氨酸化学式中x=7 | |
| D. | 每个丙氨酸分子中含有一个氧气分子 |
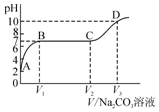 小明测得石灰石与一定量的稀盐酸反应后的溶液pH为2,取适量该溶液向其中逐滴加入碳酸钠溶液,并测得溶液pH随加入碳酸钠溶液体积的变化曲线如图所示.则下列有关说法不正确的是( )
小明测得石灰石与一定量的稀盐酸反应后的溶液pH为2,取适量该溶液向其中逐滴加入碳酸钠溶液,并测得溶液pH随加入碳酸钠溶液体积的变化曲线如图所示.则下列有关说法不正确的是( )| A. | A点处溶液中的溶质是CaCl2 | |
| B. | AB段可观察到的实验现象是有气泡产生 | |
| C. | BC段发生反应的产物是CaCO3、NaCl | |
| D. | CD段pH上升的原因是Na2CO3过量 |
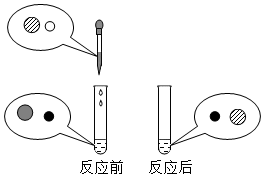 向氢氧化钠溶液中滴加稀盐酸至恰好完全反应,反应前后溶液中存在的离子种类如图所示(其中“〇”“
向氢氧化钠溶液中滴加稀盐酸至恰好完全反应,反应前后溶液中存在的离子种类如图所示(其中“〇”“ ”表示不同离子).则下列说法正确的是( )
”表示不同离子).则下列说法正确的是( )| A. | 〇表示氯离子 | |
| B. |  表示钠离子 表示钠离子 | |
| C. |  可用适量硝酸银溶液和足量稀硝酸进行检测 可用适量硝酸银溶液和足量稀硝酸进行检测 | |
| D. | 此反应的实质是 和〇结合生成水分子 和〇结合生成水分子 |
| A. | 可燃冰燃烧 | B. | 铁钉生锈 | C. | 矿石粉碎 | D. | 光合作用 |
 ”和“
”和“ ”表示两种不同的原子.
”表示两种不同的原子.