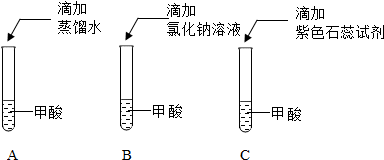
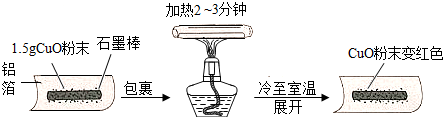
1.用托盘天平称量时,将称量物放在右盘,而砝码放在左盘,天平平衡时砝码读数为9g,游码读数为0.8g,对此实验操作结果叙述正确的是( )
| A. | 无法确定被称量物的质量 | B. | 可确定称量物的质量为9.8g | ||
| C. | 可确定称量物的质量为8.2g | D. | 此操作可确定称量物的质量为9.0g |
20.下列有关化学史的叙述正确的是( )
| A. | 道尔顿和汤姆生等科学家研究得出了重要的结论“物质是由原子或分子构成的” | |
| B. | 1869年,俄国化学家门捷列夫发现了元素周期律和元素周期表 | |
| C. | 原子论和分子学说的创立,奠定了现代化学的基础 | |
| D. | 20世纪末,人类发现和合成的物质超过4000万种 |
19.液化石油气作为燃料已经进入城市家庭,它是由一系列物质混合而成的,在常压下这些物质的沸点如表所示:
在常温下,钢瓶中无气体放出时,钢瓶中还剩余一些液体物质.这些物质最可能的是( )
| 物质名称 | 乙烷 | 丙烷 | 丁烷 | 戊烷 | 己烷 |
| 沸点 (℃) | -88.6 | -42.2 | -0.5 | 36.1 | 69.2 |
| A. | 乙烷、丙烷和丁烷 | B. | 乙烷、丙烷 | C. | 只有乙烷 | D. | 戊烷和己烷 |
15.以下是某同学进行的两个关于金属的探究实验.
【实验一】探究镁条与稀盐酸反应过程中的能量变化以及反应速率的变化

(1)实验前需对镁条进行打磨,目的是去除表面的氧化镁等杂质.
(2)检查图1 装置的气密性
(3)将镁条放入锥形瓶中,将注射器中的稀盐酸快速推入锥形瓶中.若稀盐酸是缓慢推入的,可能造成的后果是生成的热量会随之散失到周围的空气中,造成反应过程中温度几乎不变.
(4)观察注射器活塞运动变化情况,绘制出注射器内收集到的气体体积与时间关系的图象如图2 所示.
则t1~t2时间内反应速率逐渐减慢的主要原因是盐酸的浓度减小; t2~t3时间内注射器内气体体积逐渐减少的原因温度降低,气体体积减小.
【实验二】探究实验一反应后所得溶液的酸碱性
(1)甲同学用pH 试纸测定充分反应后锥形瓶中溶液的酸碱性,发现pH 小于7,说明甲同学所得溶液呈酸性(选填“酸”、“碱”或“中”).
甲同学:猜想Ⅰ:盐酸过量,使溶液pH 小于7;猜想Ⅱ:溶液pH 小于7.
为验证猜想Ⅱ,甲同学测定了该溶液的酸碱性,显弱酸性.
(2)乙同学重复甲同学实验时,发现反应后所得溶液pH 大于7,发现实验与甲同学实验不同的是,反应后的锥形瓶中镁条有剩余.乙同学猜想可能是镁与热水反应生成了碱性物质.乙同学为验证猜想,在滴有两滴酚酞的热水中放入一段打磨过镁条,观察到溶液很快变为红色,同时还观察到镁条表面有气体生成,收集并点燃该气体,发现能燃烧,请根据实验现象写出镁条与水反应的化学方程式Mg+2H2O(热)═Mg(OH)2+H2↑.
【拓展延伸】中和反应也会放出热量.某化学小组初步探究“氢氧化钠溶液和稀盐酸发生中和反应时,溶液温度的变化情况”.
【实验用品】10%的氢氧化钠溶液、10%的稀盐酸、温度计…
【实验过程】在一定体积的10%的氢氧化钠溶液中滴加10%的稀盐酸(室温下),反应中溶液温度的变化如下:
(1)试在图3中绘出溶液温度变化与加入稀盐酸体积之间的关系图.
(2)写出该中和反应的化学方程式HCl+NaOH=NaCl+H2O.
(3)其他条件不变,若改用20%的盐酸进行滴加,结合对上述曲线分析,大胆猜想新曲线最高点的位置(不考虑密度比热容及热量散失等影响因素).
①横坐标及猜想理由:5,当恰好完全反应时,放出热量的最大值与原实验相同,此时所需20%的盐酸的体积是原来的二分之一;
②纵坐标及猜想理由:大于18.2的值,当恰好完全反应时,放出热量的最大值与原实验相同,此时实验总质量比原实验小,所以△t最大值大于18.2℃.
【实验一】探究镁条与稀盐酸反应过程中的能量变化以及反应速率的变化

(1)实验前需对镁条进行打磨,目的是去除表面的氧化镁等杂质.
(2)检查图1 装置的气密性
(3)将镁条放入锥形瓶中,将注射器中的稀盐酸快速推入锥形瓶中.若稀盐酸是缓慢推入的,可能造成的后果是生成的热量会随之散失到周围的空气中,造成反应过程中温度几乎不变.
(4)观察注射器活塞运动变化情况,绘制出注射器内收集到的气体体积与时间关系的图象如图2 所示.
则t1~t2时间内反应速率逐渐减慢的主要原因是盐酸的浓度减小; t2~t3时间内注射器内气体体积逐渐减少的原因温度降低,气体体积减小.
【实验二】探究实验一反应后所得溶液的酸碱性
(1)甲同学用pH 试纸测定充分反应后锥形瓶中溶液的酸碱性,发现pH 小于7,说明甲同学所得溶液呈酸性(选填“酸”、“碱”或“中”).
甲同学:猜想Ⅰ:盐酸过量,使溶液pH 小于7;猜想Ⅱ:溶液pH 小于7.
为验证猜想Ⅱ,甲同学测定了该溶液的酸碱性,显弱酸性.
(2)乙同学重复甲同学实验时,发现反应后所得溶液pH 大于7,发现实验与甲同学实验不同的是,反应后的锥形瓶中镁条有剩余.乙同学猜想可能是镁与热水反应生成了碱性物质.乙同学为验证猜想,在滴有两滴酚酞的热水中放入一段打磨过镁条,观察到溶液很快变为红色,同时还观察到镁条表面有气体生成,收集并点燃该气体,发现能燃烧,请根据实验现象写出镁条与水反应的化学方程式Mg+2H2O(热)═Mg(OH)2+H2↑.
【拓展延伸】中和反应也会放出热量.某化学小组初步探究“氢氧化钠溶液和稀盐酸发生中和反应时,溶液温度的变化情况”.
【实验用品】10%的氢氧化钠溶液、10%的稀盐酸、温度计…
【实验过程】在一定体积的10%的氢氧化钠溶液中滴加10%的稀盐酸(室温下),反应中溶液温度的变化如下:
| 加入稀盐酸的体积(V)/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 |
| 溶液温度的变化 (△t)/℃ | 0 | 5.2 | 9.6 | 12.0 | 16.0 | 18.2 | 16.7 | 15.7 | 14.7 | 13.7 | 12.9 |
(2)写出该中和反应的化学方程式HCl+NaOH=NaCl+H2O.
(3)其他条件不变,若改用20%的盐酸进行滴加,结合对上述曲线分析,大胆猜想新曲线最高点的位置(不考虑密度比热容及热量散失等影响因素).
①横坐标及猜想理由:5,当恰好完全反应时,放出热量的最大值与原实验相同,此时所需20%的盐酸的体积是原来的二分之一;
②纵坐标及猜想理由:大于18.2的值,当恰好完全反应时,放出热量的最大值与原实验相同,此时实验总质量比原实验小,所以△t最大值大于18.2℃.
13. 某校化学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样-个实验:让水蒸气通过一根烧红的枪管,生成了一种气体.同学们对这个实验很感兴趣:难道红热的铁能与水蒸气反应?生成的气体又是什么?带着这些疑问,他们设计了如图所示的装置进行探究.
某校化学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样-个实验:让水蒸气通过一根烧红的枪管,生成了一种气体.同学们对这个实验很感兴趣:难道红热的铁能与水蒸气反应?生成的气体又是什么?带着这些疑问,他们设计了如图所示的装置进行探究.
(1)已知试管内湿棉花不参加化学反应,它的作用是提供水蒸气;
(2)若干燥从a导管出来的气体,应从c(选填“b”或“c”)
端管口通入;
(3)对化学变化过程中生成的气体同学们有以下猜想:
猜想一:生成的气体可能是氢气 猜想二:生成的气体可能是氧气.
(4)请你对猜想二进行探究:
(5)其实红热的铁遇到水蒸气,在生成气体的同时,还会生成一种黑色固体.你认为生成的黑色固体可能是四氧化三铁.
0 149858 149866 149872 149876 149882 149884 149888 149894 149896 149902 149908 149912 149914 149918 149924 149926 149932 149936 149938 149942 149944 149948 149950 149952 149953 149954 149956 149957 149958 149960 149962 149966 149968 149972 149974 149978 149984 149986 149992 149996 149998 150002 150008 150014 150016 150022 150026 150028 150034 150038 150044 150052 211419
 某校化学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样-个实验:让水蒸气通过一根烧红的枪管,生成了一种气体.同学们对这个实验很感兴趣:难道红热的铁能与水蒸气反应?生成的气体又是什么?带着这些疑问,他们设计了如图所示的装置进行探究.
某校化学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样-个实验:让水蒸气通过一根烧红的枪管,生成了一种气体.同学们对这个实验很感兴趣:难道红热的铁能与水蒸气反应?生成的气体又是什么?带着这些疑问,他们设计了如图所示的装置进行探究.(1)已知试管内湿棉花不参加化学反应,它的作用是提供水蒸气;
(2)若干燥从a导管出来的气体,应从c(选填“b”或“c”)
端管口通入;
(3)对化学变化过程中生成的气体同学们有以下猜想:
猜想一:生成的气体可能是氢气 猜想二:生成的气体可能是氧气.
(4)请你对猜想二进行探究:
| 操作方法 | 现象 | 结论 |