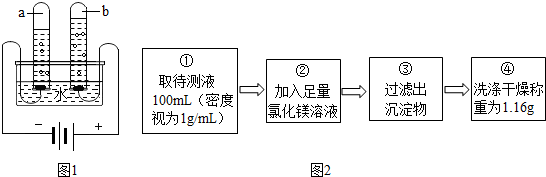
17.小华和小慧两位同学用分别如图1所示的装置进行电解水实验.该反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.为了增强水的导电性,实验前小华向水中加入硫酸钠固体,则b试管中产生的气体是O2(填化学式),检验这种气体的方法是带火星木条.小慧在做实验时误将氯化钠当成硫酸钠加入水中,结果在检验b气体时闻到一股刺激性气味.在老师的指导下小华和小慧一起就这一异常现象开展了研究.
【定性研究】
Ⅰ.小慧猜想刺激性气味气体是氯化氢和氨气,小华测认为不一定是氨气,理由是根据质量守恒定律,反应前后元素的种类不变,反应物中没有氮元素,所以不可能生成氨气.
在老题指导下得知:
①食盐水是通电时发生反应:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$↑NaOH+H2↑+Cl2↑
②氯气是种有刺激性气味的有毒气体.
由此可推测该刺激性气味的气体是氯气.
Ⅱ.为确定剩余溶液中的溶质,小慧进行如下实验,请帮她将实验报告补充完整.
小华则认为实验②不能确定一定有氯化钠,理由是①的反应中氯化铜和氢氧化钠反应,生成氯化钠和氢氧化铜,生成物中有氯化钠,向滤液中加入足量稀硝酸再滴入几滴硝酸银溶液,产生白色沉淀,所以不能证明原溶液中含有氯化钠.
【定量研究】
两位同学按如图2所示的实验步骤进行实验:
(1)步骤②加入氯化镁溶液必需足量,其目的是使氢氧化钠完全反应,滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否的具体操作:静置,取上层溶液,滴加氢氧化钠溶液,如果产生白色沉淀,说明氯化镁过量,如果没有明显现象,说明氯化镁不过量;(写出实验步骤、现象和结论).
(2)计算等测液中氢氧化钠的质量分数(写出计算过程)
(3)若步骤④中缺少洗涤干燥的操作,所测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”)

【定性研究】
Ⅰ.小慧猜想刺激性气味气体是氯化氢和氨气,小华测认为不一定是氨气,理由是根据质量守恒定律,反应前后元素的种类不变,反应物中没有氮元素,所以不可能生成氨气.
在老题指导下得知:
①食盐水是通电时发生反应:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$↑NaOH+H2↑+Cl2↑
②氯气是种有刺激性气味的有毒气体.
由此可推测该刺激性气味的气体是氯气.
Ⅱ.为确定剩余溶液中的溶质,小慧进行如下实验,请帮她将实验报告补充完整.
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量剩余溶液,滴入氯化铜溶液 | 产生蓝色絮状沉淀 | 溶液中含有氢氧化钠 |
| ②将①中反应后混合物过滤,向滤液中加入足量稀硝酸再滴入几滴硝酸银溶液 | 产生白色沉淀 | 溶液中含有氯化钠 |
【定量研究】
两位同学按如图2所示的实验步骤进行实验:
(1)步骤②加入氯化镁溶液必需足量,其目的是使氢氧化钠完全反应,滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否的具体操作:静置,取上层溶液,滴加氢氧化钠溶液,如果产生白色沉淀,说明氯化镁过量,如果没有明显现象,说明氯化镁不过量;(写出实验步骤、现象和结论).
(2)计算等测液中氢氧化钠的质量分数(写出计算过程)
(3)若步骤④中缺少洗涤干燥的操作,所测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”)
16.如表除杂方法中,所用试剂和操作均正确的是( )
| 选项 | 物质(括号内为杂质) | 杂质 | 除杂的试剂和方法 |
| A | NaOH溶液(Na2SO4) | 过量的Ba(OH)2溶液 | 过滤 |
| B | KCl(MnO2) | 水 | 溶解、过滤、洗涤干燥 |
| C | CO(CO2) | 足量氢氧化钠溶液 | 通入并干燥 |
| D | NaCl溶液(Na2CO3) | 足量稀盐酸 | 蒸发 |
| A. | A | B. | B | C. | C | D. | D |
15.铵盐是PM2.5雾霾颗粒的重要组成成分,最新科学家发现,氨气可直接参与到三氧化硫与水的反应中,其反应原理可视为NH3+H2O+SO3═NH4HSO4.下列说法不正确的是( )
| A. | 在雾霾治理过程中,可注重空气中氨气的检测及控制氨气的排放 | |
| B. | PM2.5专用口罩中使用了活性炭,是利用了活性炭的吸附性 | |
| C. | 为有效控制雾霾,应禁止使用氮肥 | |
| D. | 该反应原理中所有元素化合价都不变 |
14.已知酚酞试液显红色的PH范围是8.2-10.0之间,某同学向滴有酚酞的氢氧化钠溶液(该溶液显红色)中滴加稀盐酸至溶液恰好变为无色,则下列说法正确的是( )
| A. | 恰好变为无色时溶液中的溶质除酚酞外可能不止一种 | |
| B. | 恰好变为无色时溶液的PH一定等于7 | |
| C. | 原氢氧化钠溶液的PH大于10 | |
| D. | 不能使酚酞变红的溶液一定不是显碱性 |
13. 兴趣小组同学对“氢氧化钠溶液与稀硫酸混合是否发生了化学反应”进行了如下探究:
兴趣小组同学对“氢氧化钠溶液与稀硫酸混合是否发生了化学反应”进行了如下探究:
【提出问题】氢氧化钠溶液与稀盐酸混合是否发生了化学反应?
【猜想与假设】
a.二者混合发生了化学反应
b.二者混合没有发生化学反应
【设计并实验】
【得出结论】氢氧化钠与稀硫酸发生了化学反应
(1)乙同学认为甲的设计不合理,原因是滴加水也会使溶液pH减小,改进的方法是滴加足量硫酸一直到溶液pH等于7或小于7,根据改进的实验现象说明二者混合后发生了化学变化,写出氢氧化钠与稀硫酸反应的化学方程式2NaOH+H2SO4=Na2SO4+2H2O.
(2)探究稀硫酸与氢氧化钠溶液是否恰好完全反应.
乙同学在做完稀硫酸与氢氧化钠溶液反应得到实验后,为探究稀硫酸与氢氧化钠是否恰好完全反应,设计了实验方案二
【思考与交流】
丙同学在绝热装置中,向分别盛有10 mL10%氢氧化钠溶液加入不同体积某浓度的稀硫酸,充分混合后溶液的温度变化曲线如图(最高温度18℃).
(3)根据图示分析,稀硫酸和氢氧化钠的反应是放热(填“吸热”或“放热”)反应,加入稀硫酸10mL时,二者恰好完全反应.
 兴趣小组同学对“氢氧化钠溶液与稀硫酸混合是否发生了化学反应”进行了如下探究:
兴趣小组同学对“氢氧化钠溶液与稀硫酸混合是否发生了化学反应”进行了如下探究:【提出问题】氢氧化钠溶液与稀盐酸混合是否发生了化学反应?
【猜想与假设】
a.二者混合发生了化学反应
b.二者混合没有发生化学反应
【设计并实验】
| 实验操作 | 实验现象 | |
| 甲同学 | 在盛有10mL一定浓度的氢氧化钠溶液的烧杯中,用胶头滴管慢慢滴入1-2滴稀硫酸,振荡,同时测定溶液的pH | 溶液pH减小但仍大于7 |
| 乙同学 | 在盛有10 mL一定浓度的氢氧化钠溶液的烧杯中,先滴入几滴无色酚酞溶液,然后再加入稀硫酸 | 溶液由红色变为无色 |
(1)乙同学认为甲的设计不合理,原因是滴加水也会使溶液pH减小,改进的方法是滴加足量硫酸一直到溶液pH等于7或小于7,根据改进的实验现象说明二者混合后发生了化学变化,写出氢氧化钠与稀硫酸反应的化学方程式2NaOH+H2SO4=Na2SO4+2H2O.
(2)探究稀硫酸与氢氧化钠溶液是否恰好完全反应.
乙同学在做完稀硫酸与氢氧化钠溶液反应得到实验后,为探究稀硫酸与氢氧化钠是否恰好完全反应,设计了实验方案二
【思考与交流】
| 实验步骤 | 实验现象 | 结论 |
| 取少量碳酸钠固体于试管中滴加乙同学上述反应后的溶液于试管中 | 若有气泡生成 | 稀硫酸过量(“过量”或“不过量” |
| 若没有明显现象 | 稀硫酸与氢氧化钠溶液恰好完全反应 |
(3)根据图示分析,稀硫酸和氢氧化钠的反应是放热(填“吸热”或“放热”)反应,加入稀硫酸10mL时,二者恰好完全反应.
9.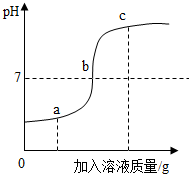 向20g溶质质量分数为3.65%的盐酸中逐滴加入NaOH溶液,得到的溶液pH变化图象如图所示.下列说法不正确的是( )
向20g溶质质量分数为3.65%的盐酸中逐滴加入NaOH溶液,得到的溶液pH变化图象如图所示.下列说法不正确的是( )
 向20g溶质质量分数为3.65%的盐酸中逐滴加入NaOH溶液,得到的溶液pH变化图象如图所示.下列说法不正确的是( )
向20g溶质质量分数为3.65%的盐酸中逐滴加入NaOH溶液,得到的溶液pH变化图象如图所示.下列说法不正确的是( )| A. | a点对应的溶液中的溶质是NaCl和HCl | |
| B. | b点对应的溶液中Na+和Cl-的数目相等 | |
| C. | c点对应的溶液中Cl-的质量为0.71克 | |
| D. | 反应过程中生成NaCl的质量始终等于参加反应的HCl和NaOH的质量总和 |
8.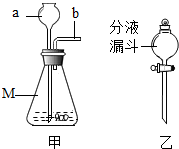 如图中的甲装置可作为实验室制二氧化碳的发生装置,下列说法正确的是( )
如图中的甲装置可作为实验室制二氧化碳的发生装置,下列说法正确的是( )
0 147564 147572 147578 147582 147588 147590 147594 147600 147602 147608 147614 147618 147620 147624 147630 147632 147638 147642 147644 147648 147650 147654 147656 147658 147659 147660 147662 147663 147664 147666 147668 147672 147674 147678 147680 147684 147690 147692 147698 147702 147704 147708 147714 147720 147722 147728 147732 147734 147740 147744 147750 147758 211419
 如图中的甲装置可作为实验室制二氧化碳的发生装置,下列说法正确的是( )
如图中的甲装置可作为实验室制二氧化碳的发生装置,下列说法正确的是( )| A. | M所指仪器的名称是广口瓶 | |
| B. | 仪器a、b插入双孔橡皮塞的先后顺序是先a后b | |
| C. | 甲装置也可以用作实验室制氧气和氢气的发生装置 | |
| D. | 将甲中a换成仪器乙,优点是能控制反应的发生与停止 |