题目内容
13. 兴趣小组同学对“氢氧化钠溶液与稀硫酸混合是否发生了化学反应”进行了如下探究:
兴趣小组同学对“氢氧化钠溶液与稀硫酸混合是否发生了化学反应”进行了如下探究:【提出问题】氢氧化钠溶液与稀盐酸混合是否发生了化学反应?
【猜想与假设】
a.二者混合发生了化学反应
b.二者混合没有发生化学反应
【设计并实验】
| 实验操作 | 实验现象 | |
| 甲同学 | 在盛有10mL一定浓度的氢氧化钠溶液的烧杯中,用胶头滴管慢慢滴入1-2滴稀硫酸,振荡,同时测定溶液的pH | 溶液pH减小但仍大于7 |
| 乙同学 | 在盛有10 mL一定浓度的氢氧化钠溶液的烧杯中,先滴入几滴无色酚酞溶液,然后再加入稀硫酸 | 溶液由红色变为无色 |
(1)乙同学认为甲的设计不合理,原因是滴加水也会使溶液pH减小,改进的方法是滴加足量硫酸一直到溶液pH等于7或小于7,根据改进的实验现象说明二者混合后发生了化学变化,写出氢氧化钠与稀硫酸反应的化学方程式2NaOH+H2SO4=Na2SO4+2H2O.
(2)探究稀硫酸与氢氧化钠溶液是否恰好完全反应.
乙同学在做完稀硫酸与氢氧化钠溶液反应得到实验后,为探究稀硫酸与氢氧化钠是否恰好完全反应,设计了实验方案二
【思考与交流】
| 实验步骤 | 实验现象 | 结论 |
| 取少量碳酸钠固体于试管中滴加乙同学上述反应后的溶液于试管中 | 若有气泡生成 | 稀硫酸过量(“过量”或“不过量” |
| 若没有明显现象 | 稀硫酸与氢氧化钠溶液恰好完全反应 |
(3)根据图示分析,稀硫酸和氢氧化钠的反应是放热(填“吸热”或“放热”)反应,加入稀硫酸10mL时,二者恰好完全反应.
分析 【得出结论】(1)根据稀释溶液,硫酸与氢氧化钠恰好反应,生成硫酸钠和水进行分析;
【思考与交流】(2)根据硫酸与碳酸钠反应,生成硫酸钠,二氧化碳和水进行分析;
(3)根据图示,加入硫酸温度变化情况进行分析.
解答 解:【得出结论】(1)滴加水会使溶液稀释,溶液pH也会减小,但溶液pH减小仍大于7,不能说明氢氧化钠与硫酸反应;滴加足量硫酸一直到溶液pH等于7或小于7,说明氢氧化钠与硫酸反应;氢氧化钠与硫酸反应生成硫酸钠和水,化学方程式:2NaOH+H2SO4=Na2SO4+2H2O;故答案为:滴加水也会使溶液pH减小;滴加足量硫酸一直到溶液pH等于7或小于7;2NaOH+H2SO4=Na2SO4+2H2O;
【思考与交流】(2)取少量碳酸钠固体于试管中滴加乙同学上述反应后的溶液于试管中,碳酸钠与硫酸反应生成二氧化碳气体,故如果发现有气泡冒出,说明硫酸过量;若没有明显现象,说明稀硫酸与氢氧化钠溶液恰好完全反应;故填:有气泡生成;过量;
(3)根据图示随着滴加硫酸温度不断升高,故该反应为放热反应;当滴加到10mL后,温度不再升高,说明当滴加到10mL时,二者恰好完全反应;故填:放热;10.
故答案为:【得出结论】(1)滴加水也会使溶液pH减小;滴加足量硫酸一直到溶液pH等于7或小于7;2NaOH+H2SO4=Na2SO4+2H2O;
(2)有气泡生成;过量;
(3)放热;10.
点评 本题考查了酸碱中和反应,要完成此题可以依据已有的知识进行,所以要求同学们在平时的学习中加强基础知识的储备.

练习册系列答案
 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
8.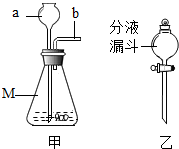 如图中的甲装置可作为实验室制二氧化碳的发生装置,下列说法正确的是( )
如图中的甲装置可作为实验室制二氧化碳的发生装置,下列说法正确的是( )
 如图中的甲装置可作为实验室制二氧化碳的发生装置,下列说法正确的是( )
如图中的甲装置可作为实验室制二氧化碳的发生装置,下列说法正确的是( )| A. | M所指仪器的名称是广口瓶 | |
| B. | 仪器a、b插入双孔橡皮塞的先后顺序是先a后b | |
| C. | 甲装置也可以用作实验室制氧气和氢气的发生装置 | |
| D. | 将甲中a换成仪器乙,优点是能控制反应的发生与停止 |
18.下列化肥中属于复合肥的是( )
| A. | KNO3 | B. | Ca3(PO4)2 | C. | NH4Cl | D. | K2CO3 |
2.下列对有关事实的解释中,错误的是( )
| A. | 生铁和钢的性能不同--含碳量不同 | |
| B. | CO和C02的化学性质不同--分子构成不同 | |
| C. | 钠原子和钠离子化学性质不同--质子数不同 | |
| D. | 金刚石和石墨的物理性质不同--原子排列方式不同 |
3.钠是一种活泼的金属,将一小块银白色的金属钠放置在空气中会发生下列变化:
钠(Na)$\stackrel{O_{2}}{→}$钠的氧化物$\stackrel{H_{2}O}{→}$氢氧化钠溶液$\stackrel{CO_{2}}{→}$白色固体
[提出问题]:常温下钠与氧气反应,产物有哪些?
[查阅资料]:钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:
Na2O+H2O=2NaOH;2Na2O2+2H2O=4NaOH+O2↑
[作出猜想]:常温下钠与氧气反应的产物.
猜想1:Na2O,
猜想2:Na2O2,
猜想3:Na2O和Na2O2
[实验探究一]:
[继续探究]:钠在空气中放置一段时间得到白色固体的成分
[作出猜想]
猜想一:Na2CO3
猜想二:Na2CO3和NaOH
[实验探究二]:
[反思与拓展]
(1)类比Na2O+H2O═2NaOH;Na2O+CO2═Na2CO3;类比2Na2O2+2H2O═4NaOH+O2↑,写出过氧化钠与二氧化碳反应的化学方程式2Na2O2+2CO2═2Na2CO3+O2,消防服的呼吸面具中“氧气再生剂”的主要成分是淡黄色固体过氧化钠,则氧气再生剂的保存方法是密封存在干燥处.
(2)能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断Na2O2不是碱性氧化物(填“是”或“不是”).
钠(Na)$\stackrel{O_{2}}{→}$钠的氧化物$\stackrel{H_{2}O}{→}$氢氧化钠溶液$\stackrel{CO_{2}}{→}$白色固体
[提出问题]:常温下钠与氧气反应,产物有哪些?
[查阅资料]:钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:
Na2O+H2O=2NaOH;2Na2O2+2H2O=4NaOH+O2↑
[作出猜想]:常温下钠与氧气反应的产物.
猜想1:Na2O,
猜想2:Na2O2,
猜想3:Na2O和Na2O2
[实验探究一]:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量钠的氧化物加入足量蒸馏水 | 无气泡生成 | 猜想1正确 |
[作出猜想]
猜想一:Na2CO3
猜想二:Na2CO3和NaOH
[实验探究二]:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量白色固体加入足量CaCl2 | 产生白色沉淀 | 白色固体成分为Na2CO3和NaOH |
| 过滤、取少量滤液加入无色酚酞试液 | 试液变红 |
(1)类比Na2O+H2O═2NaOH;Na2O+CO2═Na2CO3;类比2Na2O2+2H2O═4NaOH+O2↑,写出过氧化钠与二氧化碳反应的化学方程式2Na2O2+2CO2═2Na2CO3+O2,消防服的呼吸面具中“氧气再生剂”的主要成分是淡黄色固体过氧化钠,则氧气再生剂的保存方法是密封存在干燥处.
(2)能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断Na2O2不是碱性氧化物(填“是”或“不是”).