题目内容
17.小华和小慧两位同学用分别如图1所示的装置进行电解水实验.该反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.为了增强水的导电性,实验前小华向水中加入硫酸钠固体,则b试管中产生的气体是O2(填化学式),检验这种气体的方法是带火星木条.小慧在做实验时误将氯化钠当成硫酸钠加入水中,结果在检验b气体时闻到一股刺激性气味.在老师的指导下小华和小慧一起就这一异常现象开展了研究.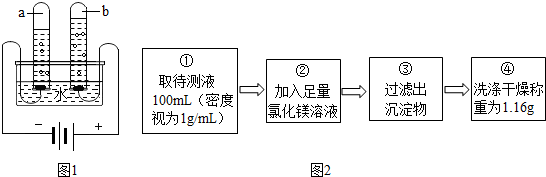
【定性研究】
Ⅰ.小慧猜想刺激性气味气体是氯化氢和氨气,小华测认为不一定是氨气,理由是根据质量守恒定律,反应前后元素的种类不变,反应物中没有氮元素,所以不可能生成氨气.
在老题指导下得知:
①食盐水是通电时发生反应:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$↑NaOH+H2↑+Cl2↑
②氯气是种有刺激性气味的有毒气体.
由此可推测该刺激性气味的气体是氯气.
Ⅱ.为确定剩余溶液中的溶质,小慧进行如下实验,请帮她将实验报告补充完整.
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量剩余溶液,滴入氯化铜溶液 | 产生蓝色絮状沉淀 | 溶液中含有氢氧化钠 |
| ②将①中反应后混合物过滤,向滤液中加入足量稀硝酸再滴入几滴硝酸银溶液 | 产生白色沉淀 | 溶液中含有氯化钠 |
【定量研究】
两位同学按如图2所示的实验步骤进行实验:
(1)步骤②加入氯化镁溶液必需足量,其目的是使氢氧化钠完全反应,滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否的具体操作:静置,取上层溶液,滴加氢氧化钠溶液,如果产生白色沉淀,说明氯化镁过量,如果没有明显现象,说明氯化镁不过量;(写出实验步骤、现象和结论).
(2)计算等测液中氢氧化钠的质量分数(写出计算过程)
(3)若步骤④中缺少洗涤干燥的操作,所测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”)
分析 根据水电解实验的原理、现象及产物检验进行分析,氧气可用带火星木条检验,氢气可用燃着的木条检验;
【定性研究】Ⅰ、根据质量守恒定律进行分析;
Ⅱ、①根据产生蓝色絮状沉淀为氢氧化铜进行分析;
②根据氯离子的检验进行分析;
【定量研究】(1)根据氢氧化钠的性质,氯化镁的性质进行分析;
(2)根据质量分数的计算进行分析;
(3)根据影响计算结果的因素进行分析.
解答 解:电解水生成氢气和氧气,反应的化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
电解水时,正极产生氧气,负极产生氢气,二者的体积比水1:2;b中气体体积小为氧气,能使带火星木条复燃;
【定性研究】Ⅰ、根据质量守恒定律,反应前后元素的种类不变,反应物中没有氮元素,所以不可能生成氨气;故填:根据质量守恒定律,反应前后元素的种类不变,反应物中没有氮元素,所以不可能生成氨气;
食盐水在通电时发生反应:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$↑NaOH+H2↑+Cl2↑,氯气是种有刺激性气味的有毒气体,所以该气体为氯气;
Ⅱ、①取少量剩余溶液,滴入氯化铜溶液,产生蓝色絮状沉淀,为氢氧化铜,所以溶液中含有氢氧化钠;故填:氢氧化钠;
②将①中反应后混合物过滤,向滤液中加入足量稀硝酸再滴入几滴硝酸银溶液,产生白色沉淀,为氯化银,说明溶液中含有氯离子;
在①的反应中氯化铜和氢氧化钠反应,生成氯化钠和氢氧化铜,生成物中有氯化钠,向滤液中加入足量稀硝酸再滴入几滴硝酸银溶液,产生白色沉淀,所以不能证明原溶液中含有氯化钠;故填:①的反应中氯化铜和氢氧化钠反应,生成氯化钠和氢氧化铜,生成物中有氯化钠,向滤液中加入足量稀硝酸再滴入几滴硝酸银溶液,产生白色沉淀,所以不能证明原溶液中含有氯化钠;
【定量研究】(1)氢氧化钠和氯化镁反应,生成氯化钠和氢氧化镁,加入氯化镁溶液必需足量,目的是使氢氧化钠完全反应;判断所加氯化镁溶液是否过量的具体操作:静置,取上层溶液,滴加氢氧化钠溶液,如果产生白色沉淀,说明氯化镁过量,如果没有明显现象,说明氯化镁不过量;故填:使氢氧化钠完全反应;取上层溶液,滴加氢氧化钠溶液,如果产生白色沉淀,说明氯化镁过量,如果没有明显现象,说明氯化镁不过量;
(2)设参加反应的氢氧化钠质量为x
MgCl2+2NaOH=Mg(OH)2↓+2NaCl
80 58
x 1.16g
$\frac{80}{58}$=$\frac{x}{1.16g}$
x=1.6g
待测液中氢氧化钠的质量分数=$\frac{1.6g}{100g}$×100%=1.6%;
(3)若步骤④中缺少洗涤干燥的操作,会使氢氧化镁中含有杂质,使质量增大,从而使计算的氢氧化钠质量增大;故填:偏大;
故答案为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;O2;带火星的木条;
【定性研究】Ⅰ、根据质量守恒定律,反应前后元素的种类不变,反应物中没有氮元素,所以不可能生成氨气;
Ⅱ、①氢氧化钠;
②产生白色沉淀;①的反应中氯化铜和氢氧化钠反应,生成氯化钠和氢氧化铜,生成物中有氯化钠,向滤液中加入足量稀硝酸再滴入几滴硝酸银溶液,产生白色沉淀,所以不能证明原溶液中含有氯化钠;
【定量研究】(1)使氢氧化钠完全反应;取上层溶液,滴加氢氧化钠溶液,如果产生白色沉淀,说明氯化镁过量,如果没有明显现象,说明氯化镁不过量;
(2)设参加反应的氢氧化钠质量为x
MgCl2+2NaOH=Mg(OH)2↓+2NaCl
80 58
x 1.16g
$\frac{80}{58}$=$\frac{x}{1.16g}$
x=1.6g
待测液中氢氧化钠的质量分数=$\frac{1.6g}{100g}$×100%=1.6%;
(3)偏大.
点评 明确水电解的原理、实验现象和结论解答本题关健

【提出问题】这瓶氢氧化钠固体是否变质?
【猜想与假设】
①该氢氧化钠没有变质;②该氢氧化钠部分变质;③该氢氧化钠全部变质.
【查阅资料】CaCl2溶液呈中性.
【设计实验】取该氢氧化钠固体样品溶于水配成溶液A,进行如下实验:
| 实验步骤 | 实验现象 | 结论及解释 |
| (1)取少量溶液A于试管中,向其中滴加足量的稀盐酸; | 有气泡产生 | 猜想①不成立 |
| (2)另取少量溶液A于试管中,向其中滴加足量的氯化钙溶液; | 产生白色沉淀 | 反应的化学方程式为: Na2CO3+CaCl2=CaCO3↓+2NaCl |
| (3)将步骤(2)所得的混合液静置,向上层清液中滴加无色的酚酞溶液. | 溶液呈红色 | 猜想② 成立 |
(4)久置的氢氧化钠变质的原因是(用化学方程式表示)CO2+2NaOH=Na2CO3+H2O;
(5)暴露在空气中会变质的化学药品还有CaO(填一种物质的化学式),
所以化学药品一般要密封保存.
【拓展计算】
为进一步探究氢氧化钠的变质程度,小明称取18.6g氢氧化钠固体样品放入烧杯中,向其中逐滴加入稀盐酸,到不再产生气泡为止,共消耗稀盐酸100g,反应后称得烧杯中溶液的质量为114.2g.
(6)生产气体的质量是4.4g;
(7)该样品中氢氧化钠的质量是8g;
(8)稀盐酸中溶质的质量分数是7.3%(要写出计算过程).
| A. | 可用一种试剂除去KNO3溶液中混有的CuSO4 | |
| B. | 用一种试剂无法将NaOH、Na2CO3、NH4NO3、(NH4)2SO4四种无色溶液一次性鉴别开 | |
| C. | KNO3、HNO3、NaOH、Fe2(SO4)3四种溶液不用其他试剂也可鉴别开 | |
| D. | 向某无色溶液中加入稀盐酸,无现象,再加入BaCl2溶液产生白色沉淀,则说明无色溶液中一定含有SO42- |
 粗盐通过初步的处理可除去其中的难溶性杂质.
粗盐通过初步的处理可除去其中的难溶性杂质.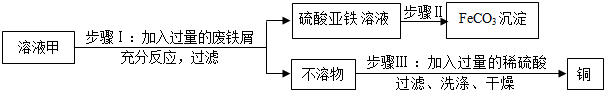
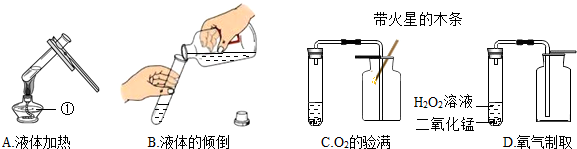
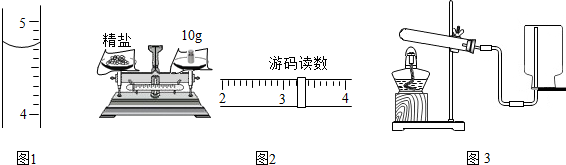
 结合图回答下列问题.
结合图回答下列问题.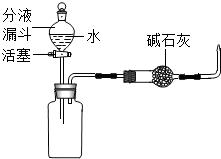 水田或池塘里常常不时地冒出一些气泡,几位同学决心弄清这种气泡的成分.请你与他们一起完成如下的探究.
水田或池塘里常常不时地冒出一些气泡,几位同学决心弄清这种气泡的成分.请你与他们一起完成如下的探究.