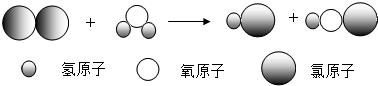
1.下列图象与相应操作对应正确的是( )
| A. |  两份完全相同的过氧化氢在有无催化剂情况下制氧气 | |
| B. | 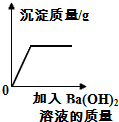 往稀盐酸和CuSO4的混合溶液中加入Ba(OH)2溶液 | |
| C. | 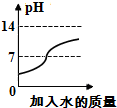 往稀盐酸中加水 | |
| D. | 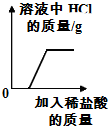 往碳酸钠溶液中加入稀盐酸 |
18.将一小块银白色的金属钠放置在空气中会发生下列变化:
钠(Na)$\stackrel{{O}_{2}}{→}$钠的氧化物$\stackrel{{H}_{2}O}{→}$氢氧化钠溶液$\stackrel{C{O}_{2}}{→}$白色固体
【提出问题】常温下钠与氧气反应,产物有哪些?
【查阅资料】钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:Na2O+H2O═2NaOH;2Na2O2+2H2O═4NaOH+O2↑
【作出猜想】常温下钠与氧气反应的产物.
猜想1:Na2O,
猜想2:Na2O2,
猜想3:①Na2O和Na2O2
【实验探究一】
【继续探究】钠在空气中放置一段时间得到白色固体的成分
【作出猜想】
猜想一:Na2CO3
猜想二:Na2CO3和NaOH
【实验探究二】
【实验反思】
(1)类比氧化铁与盐酸的反应,写出氧化钠与盐酸反应的化学方程式 ⑥Na2O+2HCl=2NaCl+H2O.
(2)过氧化钠也能与盐酸反应,方程式为:2Na2O2+4HCl=4NaCl+2H2O+X,X的化学式为⑦O2.
(3)能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断Na2O2 ⑧不是碱性氧化物(填“是”或“不是”).
钠(Na)$\stackrel{{O}_{2}}{→}$钠的氧化物$\stackrel{{H}_{2}O}{→}$氢氧化钠溶液$\stackrel{C{O}_{2}}{→}$白色固体
【提出问题】常温下钠与氧气反应,产物有哪些?
【查阅资料】钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:Na2O+H2O═2NaOH;2Na2O2+2H2O═4NaOH+O2↑
【作出猜想】常温下钠与氧气反应的产物.
猜想1:Na2O,
猜想2:Na2O2,
猜想3:①Na2O和Na2O2
【实验探究一】
| 实验操作 | 实验现象 | 实验结论 |
| 取少量钠的氧化物加入足量蒸馏水 | ②没有气泡生成 | 猜想1正确 |
【作出猜想】
猜想一:Na2CO3
猜想二:Na2CO3和NaOH
【实验探究二】
| 实验操作 | 实验现象 | 实验结论 |
| 1.取少量白色固体加入足量③氯化钡溶液(或氯化钙溶液). | 产生白色沉淀 | 白色固体成分为Na2CO3和NaOH |
| 2.过滤、取少量滤液加入 ④无色酚酞试液 | ⑤试液变红 |
(1)类比氧化铁与盐酸的反应,写出氧化钠与盐酸反应的化学方程式 ⑥Na2O+2HCl=2NaCl+H2O.
(2)过氧化钠也能与盐酸反应,方程式为:2Na2O2+4HCl=4NaCl+2H2O+X,X的化学式为⑦O2.
(3)能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断Na2O2 ⑧不是碱性氧化物(填“是”或“不是”).
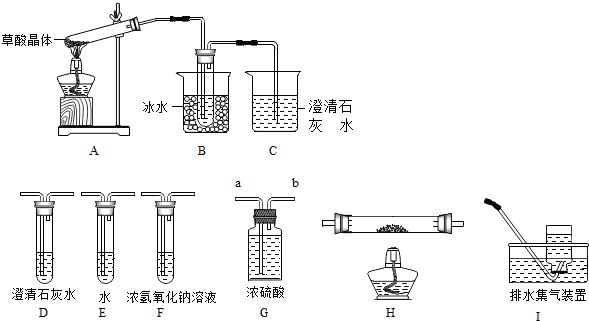
17.如图所示各项实验中,所用试剂及实验操作均正确的是( )
| A. | 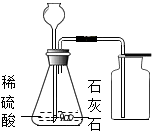 制取CO2 | B. |  加热固体 | ||
| C. |  制取氧气 | D. |  除去O2中的水蒸气 |
15.硫酸亚铁铵晶体俗名为摩尔盐,在制药、电镀方面有广泛的应用.
资料:①硫酸亚铁铵晶体化学式为FeSO4•(NH4)2SO4•6H2O,相对分子质量为392,易溶于水,不溶于乙醇;
②相关物质的溶解度(单位:g)如表:
③硫酸亚铁铵晶体受热时,在200℃以下只有结晶水失去.
某兴趣小组的学生用含有少量铜的废铁屑制备硫酸亚铁铵晶体,流程如图:
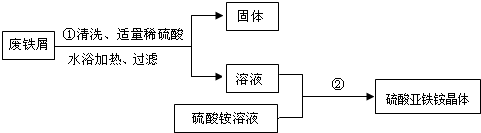
(1)操作①中发生反应的化学方程式为Fe+H2SO4═FeSO4+H2↑;
(2)过滤所需的玻璃仪器有烧杯、玻璃棒、漏斗;
(3)操作①中过滤时,要趁热进行的原因是防止温度降低FeSO4晶体析出,产量(产率)降低或使FeSO4尽可能多的溶解,提高产量(产率);
(4)操作②的目的是得到硫酸亚铁铵晶体.操作顺序是b→c→a→d;
a.过滤 b.加热浓缩 c.冷却结晶 d.洗涤干燥
(5)操作②中使用乙醇洗涤,可快速晾干.这样做的优点是AB;
A.避免用水洗涤所造成的晶体损耗
B.酒精易挥发,可低温晾干晶体
(6)该实验取废铁屑15g,最终得到硫酸亚铁铵晶体39.2g,则原废铁屑中铁元素的质量分数不低于37.3(精确到0.1%,不要求写过程).
0 147360 147368 147374 147378 147384 147386 147390 147396 147398 147404 147410 147414 147416 147420 147426 147428 147434 147438 147440 147444 147446 147450 147452 147454 147455 147456 147458 147459 147460 147462 147464 147468 147470 147474 147476 147480 147486 147488 147494 147498 147500 147504 147510 147516 147518 147524 147528 147530 147536 147540 147546 147554 211419
资料:①硫酸亚铁铵晶体化学式为FeSO4•(NH4)2SO4•6H2O,相对分子质量为392,易溶于水,不溶于乙醇;
②相关物质的溶解度(单位:g)如表:
| 温度/℃ | FeSO4 | (NH4)2SO4 | FeSO4•(NH4)2SO4•6H2O |
| 10 | 20.0 | 73 | 17.2 |
| 20 | 26.5 | 75.4 | 21.6 |
| 30 | 32.9 | 78 | 28.1 |
某兴趣小组的学生用含有少量铜的废铁屑制备硫酸亚铁铵晶体,流程如图:

(1)操作①中发生反应的化学方程式为Fe+H2SO4═FeSO4+H2↑;
(2)过滤所需的玻璃仪器有烧杯、玻璃棒、漏斗;
(3)操作①中过滤时,要趁热进行的原因是防止温度降低FeSO4晶体析出,产量(产率)降低或使FeSO4尽可能多的溶解,提高产量(产率);
(4)操作②的目的是得到硫酸亚铁铵晶体.操作顺序是b→c→a→d;
a.过滤 b.加热浓缩 c.冷却结晶 d.洗涤干燥
(5)操作②中使用乙醇洗涤,可快速晾干.这样做的优点是AB;
A.避免用水洗涤所造成的晶体损耗
B.酒精易挥发,可低温晾干晶体
(6)该实验取废铁屑15g,最终得到硫酸亚铁铵晶体39.2g,则原废铁屑中铁元素的质量分数不低于37.3(精确到0.1%,不要求写过程).
 小明同学绘制了如图所示A、B两种固体物质的溶解度曲线:
小明同学绘制了如图所示A、B两种固体物质的溶解度曲线: