题目内容
15.硫酸亚铁铵晶体俗名为摩尔盐,在制药、电镀方面有广泛的应用.资料:①硫酸亚铁铵晶体化学式为FeSO4•(NH4)2SO4•6H2O,相对分子质量为392,易溶于水,不溶于乙醇;
②相关物质的溶解度(单位:g)如表:
| 温度/℃ | FeSO4 | (NH4)2SO4 | FeSO4•(NH4)2SO4•6H2O |
| 10 | 20.0 | 73 | 17.2 |
| 20 | 26.5 | 75.4 | 21.6 |
| 30 | 32.9 | 78 | 28.1 |
某兴趣小组的学生用含有少量铜的废铁屑制备硫酸亚铁铵晶体,流程如图:
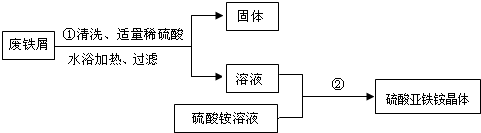
(1)操作①中发生反应的化学方程式为Fe+H2SO4═FeSO4+H2↑;
(2)过滤所需的玻璃仪器有烧杯、玻璃棒、漏斗;
(3)操作①中过滤时,要趁热进行的原因是防止温度降低FeSO4晶体析出,产量(产率)降低或使FeSO4尽可能多的溶解,提高产量(产率);
(4)操作②的目的是得到硫酸亚铁铵晶体.操作顺序是b→c→a→d;
a.过滤 b.加热浓缩 c.冷却结晶 d.洗涤干燥
(5)操作②中使用乙醇洗涤,可快速晾干.这样做的优点是AB;
A.避免用水洗涤所造成的晶体损耗
B.酒精易挥发,可低温晾干晶体
(6)该实验取废铁屑15g,最终得到硫酸亚铁铵晶体39.2g,则原废铁屑中铁元素的质量分数不低于37.3(精确到0.1%,不要求写过程).
分析 (1)根据铁和硫酸反应生成硫酸亚铁和氢气进行分析;
(2)根据过滤所需的玻璃仪器有烧杯、玻璃棒、漏斗进行分析;
(3)根据硫酸亚铁的溶解度进行分析;
(4)根据制取硫酸亚铁晶体的基本操作解答;
(5)根据硫酸亚铁难溶于酒精,酒精有挥发性进行分析;
(6)根据硫酸亚铁铵晶体中铁元素的质量分数和废铁屑的质量进行分析.
解答 解:(1)铁和硫酸反应生成硫酸亚铁和氢气,化学方程式为:Fe+H2SO4═FeSO4+H2↑;
(2)过滤所需的玻璃仪器有烧杯、玻璃棒、漏斗;
(3)根据硫酸亚铁的溶解表格可知,硫酸亚铁在50℃到80℃时溶解度是比较大的,所以操作①中过滤时,要趁热进行的原因是防止温度降低FeSO4晶体析出,产量(产率)降低或使FeSO4尽可能多的溶解,提高产量(产率);
(4)操作②的目的是得到硫酸亚铁铵晶体,基本操作步骤:加热浓缩,然后冷却结晶;再过滤;最后洗涤干燥;
(5)硫酸亚铁溶于水不溶于酒精,用A方法洗涤硫酸亚铁晶体损失较多,可用酒精洗涤,酒精又易挥发,能得到大量的纯净的硫酸亚铁晶体,故选:AB;
(6)原废铁屑中铁元素的质量分数不低于$\frac{39.2g×\frac{56}{392}}{15g}$×100%=37.3%.
故答案为:(1)Fe+H2SO4═FeSO4+H2↑;
(2)漏斗;
(3)防止温度降低FeSO4晶体析出,产量(产率)降低或使FeSO4尽可能多的溶解,提高产量(产率);
(4)c,a;
(5)AB;
(6)37.3%.
点评 过这个题培养学生观察视图的能力,以及比较分析的能力.本题考查了常见金属的性质以及某些盐的性质,完成此题,可以依据题干提供的内容,从中抽取有用的信息,结合已有的知识进行.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
10.下列化学小实验中不涉及化学变化的是( )
| A. | 用食醋除水壶壁上的水垢 | B. | 用活性炭除天然水中的臭味物质 | ||
| C. | 用蜡烛不充分燃烧制炭黑 | D. | 用柠檬酸、小苏打、水等自制汽水 |
4.现有Mg(OH)2和MgCO3的固体混合物6g,经测定镁元素的质量分数为40%,向固体混合物中加入100g一定溶质质量分数的稀盐酸,恰好完全反应,下列说法不正确的是( )
| A. | 反应过程中有气泡产生 | |
| B. | 生成MgCl2的质量为9.5g | |
| C. | 反应后溶液中的溶质只有MgCl2 | |
| D. | 所用稀盐酸中溶质的质量分数为14.6% |
 为了测定空气中氧气的含量,小华设计了如下方案:选用实际溶剂为40ml的直玻璃管作反应容器,将过量的白磷放入试管,用橡皮塞紧直玻璃管,通过导管与实际容积为60mL的且润滑性很好的针筒注射器组成如图所示的实验装置.假设此装置能按照小华的设想正常进行,且白磷所占体积与导管内的气体体积忽略不计,请回答下列问题:
为了测定空气中氧气的含量,小华设计了如下方案:选用实际溶剂为40ml的直玻璃管作反应容器,将过量的白磷放入试管,用橡皮塞紧直玻璃管,通过导管与实际容积为60mL的且润滑性很好的针筒注射器组成如图所示的实验装置.假设此装置能按照小华的设想正常进行,且白磷所占体积与导管内的气体体积忽略不计,请回答下列问题: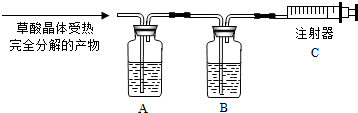

 哈尔滨市“滨江湿地公园”是集湿地观赏、亲水游乐、休闲度假为一体的湿地公园,它将被打造成为国家5A级湿地旅游风景区.“湿地蘑菇采摘园”种植的蘑菇主要为人体提供的营养素为维生素,其作用为调节新陈代谢,预防疾病,维持身体健康;种植蘑菇期间,为使蘑菇抗寒抗旱,同时提高植物体内蛋白质的含量,农民经常要施加的一种化肥为NH4H2PO4(具体的化学式),农民在施用此化肥时不能与草木灰同时施用的主要原因是草木灰显碱性,与铵态氮肥混合使用会丧失肥效.肥料使用过程中提倡使用适量,合理施用化肥,否则会造成水体污染,水体污染的危害为水体富营养化;请举出你在生活中防治水体污染的具体措施:电池不随便乱扔.
哈尔滨市“滨江湿地公园”是集湿地观赏、亲水游乐、休闲度假为一体的湿地公园,它将被打造成为国家5A级湿地旅游风景区.“湿地蘑菇采摘园”种植的蘑菇主要为人体提供的营养素为维生素,其作用为调节新陈代谢,预防疾病,维持身体健康;种植蘑菇期间,为使蘑菇抗寒抗旱,同时提高植物体内蛋白质的含量,农民经常要施加的一种化肥为NH4H2PO4(具体的化学式),农民在施用此化肥时不能与草木灰同时施用的主要原因是草木灰显碱性,与铵态氮肥混合使用会丧失肥效.肥料使用过程中提倡使用适量,合理施用化肥,否则会造成水体污染,水体污染的危害为水体富营养化;请举出你在生活中防治水体污染的具体措施:电池不随便乱扔.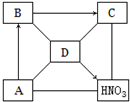 A、B、C、D四种物质分别是酸碱盐和氧化物中的一种,其中有一种是胃液的主要成分,B是一种常用的食品干燥剂.它们之间的转化关系如图所示,“-”表示相互反应,“→”表示相互转化.请回答:
A、B、C、D四种物质分别是酸碱盐和氧化物中的一种,其中有一种是胃液的主要成分,B是一种常用的食品干燥剂.它们之间的转化关系如图所示,“-”表示相互反应,“→”表示相互转化.请回答: