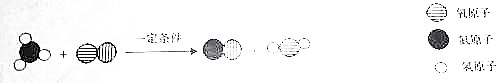
题目内容
18.将一小块银白色的金属钠放置在空气中会发生下列变化:钠(Na)$\stackrel{{O}_{2}}{→}$钠的氧化物$\stackrel{{H}_{2}O}{→}$氢氧化钠溶液$\stackrel{C{O}_{2}}{→}$白色固体
【提出问题】常温下钠与氧气反应,产物有哪些?
【查阅资料】钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:Na2O+H2O═2NaOH;2Na2O2+2H2O═4NaOH+O2↑
【作出猜想】常温下钠与氧气反应的产物.
猜想1:Na2O,
猜想2:Na2O2,
猜想3:①Na2O和Na2O2
【实验探究一】
| 实验操作 | 实验现象 | 实验结论 |
| 取少量钠的氧化物加入足量蒸馏水 | ②没有气泡生成 | 猜想1正确 |
【作出猜想】
猜想一:Na2CO3
猜想二:Na2CO3和NaOH
【实验探究二】
| 实验操作 | 实验现象 | 实验结论 |
| 1.取少量白色固体加入足量③氯化钡溶液(或氯化钙溶液). | 产生白色沉淀 | 白色固体成分为Na2CO3和NaOH |
| 2.过滤、取少量滤液加入 ④无色酚酞试液 | ⑤试液变红 |
(1)类比氧化铁与盐酸的反应,写出氧化钠与盐酸反应的化学方程式 ⑥Na2O+2HCl=2NaCl+H2O.
(2)过氧化钠也能与盐酸反应,方程式为:2Na2O2+4HCl=4NaCl+2H2O+X,X的化学式为⑦O2.
(3)能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断Na2O2 ⑧不是碱性氧化物(填“是”或“不是”).
分析 【作出猜想】根据钠与氧气反应的产物进行猜想;
【实验探究一】:根据氧化钠与水反应的现象分析;
【实验探究二】:根据碳酸钠、氢氧化钠的性质、检验方法分析回答;
【实验反思】(1)根据氧化铜与盐酸的反应,写出氧化钠与盐酸反应的化学方程式;
(2)根据质量守恒定律分析X的化学式;
(3)根据氧化钠与盐酸反应的生成物分析判断.
解答 解:【作出猜想】由于钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),所以猜想三是:①Na2O和Na2O2;
【实验探究一】:由于氧化钠与水反应生成了氢氧化钠,所以,取少量钠的氧化物加入足量蒸馏水,现象是②没有气泡生成,证明猜想一正确;所以.填表如下:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量钠的氧化物加入足量蒸馏水 | ②没有气泡生成 | 猜想1正确 |
| 实验操作 | 实验现象 | 实验结论 |
| 1.取少量白色固体加入足量③氯化钡溶液(或氯化钙溶液) | 产生白色沉淀 | 白色固体成分为Na2CO3和NaOH |
| 2.过滤、取少量滤液加入 ④无色酚酞试液 | ⑤试液变红 |
【实验反思】(1)由氧化铜与盐酸的反应生成了氯化铜和水可知,氧化钠与盐酸反应生成了氯化钠和水,化学方程式是:⑥Na2O+2HCl=2NaCl+H2O;
(2)由质量守恒定律反应后原子的种类及数目不变可知,方程式得到右边还缺少两个氧原子,所以,分析X的化学式是:O2.
(3)由上述方程式可知,过氧化钠与盐酸反应生成了氯化钠、水和氧气,不属于碱性氧化物.
故本题答案为:
【作出猜想】①Na2O和Na2O2.
【实验探究一】②无气泡生成.
【实验探究二】③氯化钡溶液(或氯化钙溶液)(合理即可).④无色酚酞试液.⑤试液变红.
【实验反思】⑥Na2O+2HCl=2NaCl+H2O.⑦O2. ⑧不是.
点评 该题根据查阅资料提供的信息并结合实验步骤和现象解决问题.主要考查读题能力,能把题目所给信息与所学知识进行牵连.知道性质决定用途,用途体现性质.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.下列实验操作正确的是( )
| A. |  量取液体 | B. |  问气体气味 | C. |  甲烷验纯 | D. |  稀释浓硫酸 |
9.在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化见表.下列说法中不正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前物质质量/g | 8 | 32 | 5 | 4 |
| 反应后物质质量/g | 16 | 4 | x | 24 |
| A. | 该反应为分解反应 | |
| B. | 乙、丁两种物质间反应的质量比为7:5 | |
| C. | 甲、乙两种物质间参加反应的质量比为1:4 | |
| D. | 丙可能为该反应的催化剂 |
13.用滤纸做成的小花喷洒某无色溶液后放在具有挥发性溶液的上方,片刻后变成红色.则可作为喷洒液和挥发性物质的一组物质是( )
| A. | 石蕊试液和浓硫酸 | B. | 石蕊试液和石灰水 | ||
| C. | 酚酞溶液和浓盐酸 | D. | 酚酞溶液和浓氨水 |
7.“H68黄铜”(即铜含昼为68%的铜锌合金),可焊性、耐蚀性能等均佳,是应用最广的一种黄铜.小东为测定市场上某黄铜制品中铜的实际含量,将10g黄铜样品加入烧杯中,分六次加人某稀硫酸,每次充分反应后,测得剩余固体的质量,数据记录如下:
(1)小东要配制50g溶质的质量分数为19.6%的稀硫酸用于测得黄铜样品,计算他所需98%的浓硫酸的质量和加入水的质量.(写出计算过程)
(2)分析上表数据,小东测得的黄铜样品的实际含铜质量分数为67.5%.
(3)实验结束后,小东测得剩余溶液显酸性.计算剩余溶液中硫酸的质量分数.(精确到0.1%)
| 实验记录序号 | (1) | (2) | (3) | (4) | (5) | (6) |
| 加入稀硫酸质量/g | 5 | 5 | 5 | 5 | 5 | 5 |
| 剩余固体质量/g | 9.35 | 8.70 | 8.05 | 7.40 | 6.75 | 6.75 |
(2)分析上表数据,小东测得的黄铜样品的实际含铜质量分数为67.5%.
(3)实验结束后,小东测得剩余溶液显酸性.计算剩余溶液中硫酸的质量分数.(精确到0.1%)
 小明同学绘制了如图所示A、B两种固体物质的溶解度曲线:
小明同学绘制了如图所示A、B两种固体物质的溶解度曲线: