题目内容
12.将某暗紫色固体粉末A加热,可产生无色气体B,同时生成一种黑色固体C和另一种固体物质D.黑色固体C通常可用于加热氯酸钾制氧气时的催化剂.另一黑色固体E在无色气体B中燃烧,产生使澄清石灰水变浑浊的气体F.绿色植物可将气体F通过光合作用吸收,并转化为无色气体B.回答:①A高锰酸钾C二氧化锰F二氧化碳;②加热暗紫色固体A时所发生的反应属于分解反应.分析 将某暗紫色固体粉末A加热,可产生无色气体B,同时生成一种黑色固体C和另一种固体物质D.黑色固体C通常可用于加热氯酸钾制氧气时的催化剂.则C为二氧化锰,高锰酸钾是一种暗紫色固体,在加热条件下生成锰酸钾、二氧化锰和氧气,可确定ABD;另一黑色固体E在无色气体B中燃烧,产生使澄清石灰水变浑浊的气体F.绿色植物可将气体F通过光合作用吸收,并转化为无色气体B,由碳是一种黑色固体,在氧气中燃烧生成二氧化碳气体,二氧化碳发生光合作用生成氧气;进行分析解答.
解答 解:将某暗紫色固体粉末A加热,可产生无色气体B,同时生成一种黑色固体C和另一种固体物质D.黑色固体C通常可用于加热氯酸钾制氧气时的催化剂.则C为二氧化锰,高锰酸钾是一种暗紫色固体,在加热条件下生成锰酸钾、二氧化锰和氧气,则A为高锰酸钾、B为氧气、D为锰酸钾;另一黑色固体E在无色气体B中燃烧,产生使澄清石灰水变浑浊的气体F;绿色植物可将气体F通过光合作用吸收,并转化为无色气体B,由碳是一种黑色固体,在氧气中燃烧生成二氧化碳气体,二氧化碳发生光合作用生成氧气,则E为碳,F为二氧化碳.
高锰酸钾是一种暗紫色固体,在加热条件下生成锰酸钾、二氧化锰和氧气,该反应符合“一变多”的特征,属于分解反应.
故答案为:①高锰酸钾;二氧化锰;二氧化碳;②分解.
点评 本题难度不大,解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征等),获得结论,最后把结论代入原题中验证.

练习册系列答案
相关题目
2.水是生命之源,下列关于水的说法不正确的是( )
| A. | 水是一种最常见的溶剂 | |
| B. | 水由液态变成气态时,分子间隙变大 | |
| C. | 一个水分子由两个氢原子和一个氧原子构成 | |
| D. | 电解水生成氢气和氧气,说明水是由氢气和氧气组成 |
3.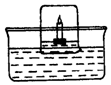 如图,为得知空气中氧气的大致体积分数,用一只干冷的烧杯,沿水面罩住漂浮在水面燃烧的蜡烛.烧杯壁上很快出现小水珠,烧杯底变成黑色(即产生烟炱).不一会儿,蜡烛自动熄灭,杯内水位上升.待冷却后,发现上升部分水的体积约占烧杯容积的1/5,关于该实验的说法错误的是( )
如图,为得知空气中氧气的大致体积分数,用一只干冷的烧杯,沿水面罩住漂浮在水面燃烧的蜡烛.烧杯壁上很快出现小水珠,烧杯底变成黑色(即产生烟炱).不一会儿,蜡烛自动熄灭,杯内水位上升.待冷却后,发现上升部分水的体积约占烧杯容积的1/5,关于该实验的说法错误的是( )
 如图,为得知空气中氧气的大致体积分数,用一只干冷的烧杯,沿水面罩住漂浮在水面燃烧的蜡烛.烧杯壁上很快出现小水珠,烧杯底变成黑色(即产生烟炱).不一会儿,蜡烛自动熄灭,杯内水位上升.待冷却后,发现上升部分水的体积约占烧杯容积的1/5,关于该实验的说法错误的是( )
如图,为得知空气中氧气的大致体积分数,用一只干冷的烧杯,沿水面罩住漂浮在水面燃烧的蜡烛.烧杯壁上很快出现小水珠,烧杯底变成黑色(即产生烟炱).不一会儿,蜡烛自动熄灭,杯内水位上升.待冷却后,发现上升部分水的体积约占烧杯容积的1/5,关于该实验的说法错误的是( )| A. | 现象的发生跟大气压强及气体的溶解性等有关 | |
| B. | 化学能转化为光能和热能,有熔化、液化等现象发生 | |
| C. | 实验说明,空气中氧气体积约占$\frac{1}{5}$ | |
| D. | 通过该实验还可证明蜡烛中肯定含有碳、氢、氧二种元素 |
17.Cu-Zn合金外观类似黄金.甲、乙、丙三位同学分别取Cu-Zn合金粉末与某稀硫酸反应,所得数据如表:
计算:
( 1 )金属混合物中锌的质量分数.
( 2 )该硫酸中溶质的质量分数.
| 甲 | 乙 | 丙 | |
| 取用金属混合物的质量(/g) | 10 | 10 | 20 |
| 取用稀硫酸的质量(/g) | 100 | 200 | 200 |
| 充分反应后过滤得到干燥固体的质量(/g) | 3.5 | 2 | 7 |
( 1 )金属混合物中锌的质量分数.
( 2 )该硫酸中溶质的质量分数.
4.人体缺碘会引起甲状腺肿大,造成思维迟钝.结合如图,下列描述正确的是( )


| A. | 碘原子的质量是126.9g | B. | 碘离子核外电子数为54 | ||
| C. | 碘是微量元素,摄入越多越好 | D. | 碘原子内中子数约为72 |
