题目内容
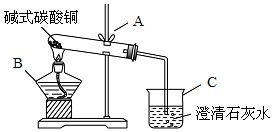
11.某碳酸钠样品中含有少量氯化钠杂质,为测定该样品中碳酸钠的质量分数,进行了如下实验:
请回答下列问题:
(1)在实验过程中加入饱和石灰水后发生反应的化学方程式是Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
(2)为探究上述反应后滤液中的溶质成分,甲同学向滤液中滴加过量稀盐酸,发现有气泡产生,则滴加盐酸前滤液中的溶质除氯化钠外还有Na2CO3 和NaOH;滴加盐酸的过程中发生反应的化学方程式为Na2CO3+2HCl=2NaCl+H2O+CO2↑ 和NaOH+HCl=NaCl+H2O.
分析 (1)根据碳酸钠和饱和石灰水反应生成碳酸钙沉淀和氢氧化钠,进行分析解答.
(2)由反应流程图,滤液中含有碳酸钠与氢氧化钙反应生成的氢氧化钠;甲同学向滤液中滴加过量稀盐酸,发现有气泡产生,说明碳酸钠溶液过量,该滤液中还含有碳酸钠,据此进行分析解答.
解答 解:(1)碳酸钠和饱和石灰水反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
(2)甲同学向滤液中滴加过量稀盐酸,发现有气泡产生,说明碳酸钠溶液过量;碳酸钠与氢氧化钙反应反应生成了碳酸钙和氢氧化钠,则滴加盐酸前滤液中的溶质除氯化钠外,还有碳酸钠和氢氧化钠,反应的化学方程式分别是:Na2CO3+2HCl═2NaCl+H2O+CO2↑,NaOH+HCl=NaCl+H2O.
故答为:(1)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.(2)Na2CO3,NaOH; Na2CO3+2HCl=2NaCl+H2O+CO2↑,NaOH+HCl=NaCl+H2O.
点评 本题难度不是很大,掌握盐的化学性质、化学方程式的书写方法等是正确解答本题的关键.

练习册系列答案
相关题目
2.从海水中提取金属镁,可按如图流程进行,下列说法正确的是( )


| A. | 步骤Ⅰ通过一步反应即可实现 | |
| B. | 步骤Ⅱ、Ⅲ、Ⅳ的目的是从海水中提纯氯化镁 | |
| C. | 步骤Ⅴ中化学能转化为电能 | |
| D. | 该流程涉及的基本反应类型有4种 |
19.如图为元素周期表的一部分,下列说法正确的是( )
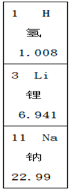

| A. | 它们都是金属元素 | B. | 氢的相对原子质量为1.008 | ||
| C. | 锂的核外电子数是6.941 | D. | 钠属于人体中的微量元素 |
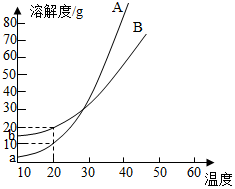 A、B两种化合物的溶解度曲线如图.现要用结晶法从A、B混合物中提取A.(不考虑A、B共存时,对各自溶解度的影响.)
A、B两种化合物的溶解度曲线如图.现要用结晶法从A、B混合物中提取A.(不考虑A、B共存时,对各自溶解度的影响.)
 :
: