题目内容
3.碳和碳的化合物是初中化学学习的重要内容.(1)木炭在氧气中燃烧的实验现象是发出白光,放出大量热.
(2)2017年5月,我国在南海试采“可燃冰”取得成功.“可燃冰”的主要成分是甲烷的水合物,化学式可表示为mCH4•nH2O,其中碳、氢元素的质量比为12m:(4m+2n)(用含m、n的代数式表示).开采的“可燃冰”挥发出甲烷气体,写出甲烷充分燃烧的化学方程式:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(3)点燃的镁条能与二氧化碳反应生成氧化镁和一种单质,反应的化学方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
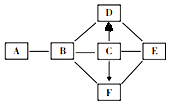
(4)如图是实验室制取气体的常见装置.
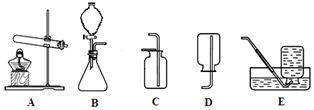
①实验室用石灰石和稀盐酸制取CO2气体应选择的装置是BC(填装置编号).
②检查B装置气密性的方法是连接导气管,把导气管口插入水中,关闭漏斗活塞,双手捂住锥形瓶,若导管口有气泡冒出,则装置不漏气.
③甲烷是一种极难溶于水的气体,实验室常用加热无水醋酸钠和碱石灰的固体混合物制取甲烷,制取甲烷需要选择的装置是AE(或AD)(填装置编号).
(5)一氧化碳用作炼铁的还原剂.在高温下一氧化碳与Fe2O3反应生成铁和二氧化碳.某炼钢厂每天消耗4900t含Fe2O380%的赤铁矿(其他成分不反应),计算该厂理论上每天产生二氧化碳的质量为多少.
分析 (1)根据木炭在氧气中燃烧的实验现象分析回答.
(2)根据化学式的意义分析计算可燃冰中碳、氢元素的质量比,根据甲烷充分燃烧的反应写出化学方程式.
(3)根据点燃的镁条与二氧化碳的反应写出反应的化学方程式.
(4)①根据实验室制取CO2气体的药品的状态和反应条件确定发生装置,根据二氧化碳的收集方法确定收集装置.
②根据装置的特点和压强的变化分析回答检查B装置气密性的方法.
③根据实验室制取甲烷气体的药品的状态和反应条件确定发生装置,根据甲烷的收集方法确定收集装置.
(5)根据在高温下一氧化碳与Fe2O3反应生成铁和二氧化碳的反应,由氧化铁的质量可求出二氧化碳的质量.
解答 解:(1)木炭在氧气中燃烧的实验现象是:发出白光,放出大量热.
(2)“可燃冰”的主要成分是甲烷的水合物,化学式可表示为mCH4•nH2O,其中碳、氢元素的质量比为:12m:(4m+2n),甲烷充分燃烧生成了二氧化碳和水,反应的化学方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(3)点燃的镁条能与二氧化碳反应生成氧化镁和一种单质,由质量守恒定律可知该单质为碳,反应的化学方程式为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
(3)①实验室用石灰石和稀盐酸制取CO2气体,属于固液常温下反应制取气体,应选用的发生装置是B,二氧化碳能能溶于水,密度比空气大,可用向上排气发收集,应选用的收集装置是C;
②检查B装置气密性的方法是:连接导气管,把导气管口插入水中,关闭漏斗活塞,双手捂住锥形瓶,若导管口有气泡冒出,则装置不漏气.
③实验室常用加热无水醋酸钠和碱石灰的固体混合物制取甲烷,属于加热固体制取气体,应选用的发生装置是A,由于甲烷是极难溶于水的气体,可用排水法收集,可选用的收集装置是E;又由于甲烷的密度比空气小,可用向下排气法收集,可选用的收集装置是D.所以制取甲烷气体制取甲烷需要选择的装置是:AE(或AD);
(5)设理论上产生CO2的质量为x
Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2↑
160 132
4900 t×80% x
$\frac{160}{132}=\frac{4900t×80%}{x}$ 解得:x=3234 t.
故答为:(1)发出白光,放出大量热;(2)12m:(4m+2n); CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;(3)2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;(4)①BC; ②连接导气管,把导气管口插入水中,关闭漏斗活塞,双手捂住锥形瓶,若导管口有气泡冒出,则装置不漏气; ③AE(或AD).
点评 本题主要考查了碳和碳的化合物的知识,涉及的知识点较多,难度不大,加强基础知识的学习有利于解答本题.

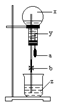 如图所示,烧瓶内充有x气体,若挤压滴管的胶头a,使液体y进入烧瓶中,振荡烧瓶,并倒放在铁架台上,将导管伸入滴有z的水中,打开弹簧夹b,可见烧杯中液体如喷泉一样喷入烧瓶中,并出现颜色的改变,则x、y、z可能是( )
如图所示,烧瓶内充有x气体,若挤压滴管的胶头a,使液体y进入烧瓶中,振荡烧瓶,并倒放在铁架台上,将导管伸入滴有z的水中,打开弹簧夹b,可见烧杯中液体如喷泉一样喷入烧瓶中,并出现颜色的改变,则x、y、z可能是( )| x气体 | y液 | z试剂 | |
| ① | O2 | H2SO4 | 紫色石蕊试液 |
| ② | CO2 | NaOH | 无色酚酞试液 |
| ③ | CO | Ca(OH)2 | 无色酚酞试液 |
| ④ | HCl | H2O | 紫色石蕊试液 |
| A. | ②④ | B. | 只有② | C. | ①② | D. | ③④ |
| A. | 滴入浓硫酸 | B. | 看颜色是否鲜艳 | C. | 灼烧后闻气味 | D. | 无法鉴别 |
| A. | 滤液中一定有Fe(NO3)3 和Zn(NO3)2 | B. | 滤渣中一定有Ag、Cu、Fe和Zn | ||
| C. | 滤渣中只有Ag和Cu,一定无Zn | D. | 滤渣中一定有Ag、Cu和Fe,一定无Zn |
| A. | FeO | B. | Fe2O3 | C. | Fe3O4 | D. | FeSO4 |
沈艳同学观察到瓶上的标签如下表所示.
| 二氧化氯(ClO2)1000毫升 | |
| 溶质的质量分数 | 80% |
| 密度 | 1.2克/厘米3 |
| 强腐蚀性,阴冷,密封储藏 | |
(1)这1000毫升二氧化氯消毒液的质量是1200克,其中含溶质二氧化氯960克.
(2)若将这1000毫升二氧化氯消毒液与5000克水均匀混合,所得稀二氧化氯消毒液中二氧化氯的质量分数是15.48%.(保留两位小数)
(3)我校欲配制30千克质量分数为20%的稀二氧化氯消毒液用来消毒,需要多少千克这种二氧化氯消毒液和多少千克水?(写出计算过程)