题目内容
20.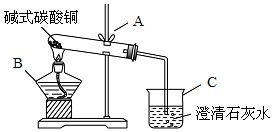 :
:(1)装置中,仪器B的名称是酒精灯;
(2)写出生成碱式碳酸铜的化学方程式Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+CO2↑+H2O;这个化学反应属于四大基本反应类型中的分解反应(填“化合”、“分解”、“置换”或“复分解”);
(3)在加热分解铜绿时,根据“澄清石灰水变浑浊”的现象,说明有二氧化碳生成.
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据碱式碳酸铜在加热的条件下生成氧化铜、水和二氧化碳进行分析;
(3)根据二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,B是酒精灯;
(2)碱式碳酸铜在加热的条件下生成氧化铜、水和二氧化碳,化学方程式为:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+CO2↑+H2O,该反应属于分解反应;
(3)二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,所以在加热分解铜绿时,根据“澄清石灰水变浑浊”的现象,说明有二氧化碳生成.
故答案为:(1)酒精灯;
(2)Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+CO2↑+H2O,分解反应;
(3)二氧化碳.
点评 本题主要考查了盐的化学性质和化学方程式的书写,难度不大,需要在平时的学习中加强记忆即可完成.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.在AgNO3、Cu(NO3)2和Zn(NO3)2混合溶液中,加入定量的铁粉,充分反应后过滤,在滤渣中加入稀盐酸,有气体产生.则下列结论正确的是 ( )
| A. | 滤液中一定有Fe(NO3)3 和Zn(NO3)2 | B. | 滤渣中一定有Ag、Cu、Fe和Zn | ||
| C. | 滤渣中只有Ag和Cu,一定无Zn | D. | 滤渣中一定有Ag、Cu和Fe,一定无Zn |
15.工业上制硫酸的生产过程可分为三个步骤,其中第一步为黄铁矿煅烧,反应的化学方程式为:4FeS2+11O2═2X+8SO2,则,根据质量守恒定律推测X的化学式为( )
| A. | FeO | B. | Fe2O3 | C. | Fe3O4 | D. | FeSO4 |
12.近几年,甲型H1N1型流感日趋严重,并出现了许多变种,上半年新塍菜场不幸有人感染H7N9病毒现已治愈.最有效的预防方法之一就是用消毒液对菜场空气消毒.新塍镇镇政府采用的二氧化氯消毒液是国际上公认的新一代强力,广谱,安全,高效的消毒剂,已被世界卫生组织(WHO)列为A1级安全消毒剂.二氧化氯消毒液能够迅速,彻底杀灭各种细菌(大肠杆菌,白色念珠菌等)和病毒(肝炎病毒,流感病毒等).
沈艳同学观察到瓶上的标签如下表所示.
求:
(1)这1000毫升二氧化氯消毒液的质量是1200克,其中含溶质二氧化氯960克.
(2)若将这1000毫升二氧化氯消毒液与5000克水均匀混合,所得稀二氧化氯消毒液中二氧化氯的质量分数是15.48%.(保留两位小数)
(3)我校欲配制30千克质量分数为20%的稀二氧化氯消毒液用来消毒,需要多少千克这种二氧化氯消毒液和多少千克水?(写出计算过程)
沈艳同学观察到瓶上的标签如下表所示.
| 二氧化氯(ClO2)1000毫升 | |
| 溶质的质量分数 | 80% |
| 密度 | 1.2克/厘米3 |
| 强腐蚀性,阴冷,密封储藏 | |
(1)这1000毫升二氧化氯消毒液的质量是1200克,其中含溶质二氧化氯960克.
(2)若将这1000毫升二氧化氯消毒液与5000克水均匀混合,所得稀二氧化氯消毒液中二氧化氯的质量分数是15.48%.(保留两位小数)
(3)我校欲配制30千克质量分数为20%的稀二氧化氯消毒液用来消毒,需要多少千克这种二氧化氯消毒液和多少千克水?(写出计算过程)
9.人们对事物的认识常需经历一个不断修正和完善的过程,如对酸的认识就是如此.下列各项是不同时期对酸的认识,其中与我们现在所学酸的定义最相近的是( )
| A. | 有酸味的物质 | B. | 一切酸中都含有氧 | ||
| C. | 只有氢才是酸不可缺少的元素 | D. | 与碱作用时失去原有性质的物质 |
10.粗盐提纯实验的部分操作如图所示,其中不正确的是( )
| A. | 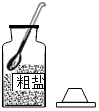 取一定量粗盐 | B. | 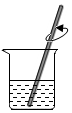 溶解 | C. | 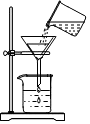 过滤 | D. |  蒸发 |

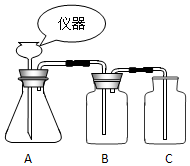 根据如图装置回答下列问题:
根据如图装置回答下列问题: