题目内容
17.实验操作正确的是( )| A. | 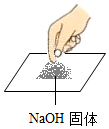 取用氢氧化钠固体 | B. |  取用氯化钠固体 | ||
| C. |  取用液体 | D. | 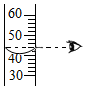 读取液体体积 |
分析 A、根据取用化学药品的注意事项分析;
B、根据取用粉末状固体的方法进行分析判断;
C、根据向试管中倾倒液体药品的方法进行分析判断;
D、根据量取液体药品时读数的方法进行分析判断.
解答 解:A、禁止用手直接去拿化学药品,图中所示操作错误.
B、取用固体粉末时,将试管平放,把纸槽伸到试管底部,再把试管慢慢竖起,图中所示操作错误.
C、向试管中倾倒液体药品时,瓶塞要倒放,标签要对准手心,瓶口紧挨,图中所示操作正确.
D、用量筒量取液体药品读数时,视线要与凹液面的最底处保持水平,图中所示操作错误.
故选:C.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.氢元素和氧元素的本质区别是( )
| A. | 质子数不同 | B. | 中子数不同 | ||
| C. | 核外电子数不同 | D. | 相对原子质量不同 |
2.化学就在我们身边,在日常生活中我们要用心留意身边发生的物质变化,发现一个问题往往要比解决一个问题重要得多.
【发现问题】某化学兴趣小组的同学们正在制取二氧化碳,为了验证制取的气体是否是二氧化碳,它们将生成的气体通入澄清的石灰水中,结果发现澄清石灰水没有变浑浊.经回想,同学们觉得可能是将澄清石灰水错拿成了氢氧化钠溶液,很多同学对此提出了新的问题:二氧化碳通入氢氧化钠溶液中无明显现象,那它们发生化学反应了吗?同学们决定对该问题进行探究.
【提出猜想】二氧化碳与氢氧化钠溶液发生了化学反应.
【实验验证】
【交流反思】(1)你认为实验一一定是错误的,理由是氢氧化钠和二氧化碳反应生成的碳酸钠溶液显碱性,也能使酚酞试液变红色.
(2)小明认为实验二不严谨,原因是二氧化碳能够溶于水,并且能和水反应生成碳酸.
请你写出一种改进实验的方法:取另一相同矿泉水瓶,收集满二氧化碳,向矿泉水瓶中加入和氢氧化钠溶液体积相同的水,振荡观察现象.
(3)请写出实验三种产生实验现象的反应的化学方程式:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
【拓展分析】(4)实验三中,除滴加稀盐酸外,可以滴加的盐溶液有氯化钙溶液(写一种即可)
【发现问题】某化学兴趣小组的同学们正在制取二氧化碳,为了验证制取的气体是否是二氧化碳,它们将生成的气体通入澄清的石灰水中,结果发现澄清石灰水没有变浑浊.经回想,同学们觉得可能是将澄清石灰水错拿成了氢氧化钠溶液,很多同学对此提出了新的问题:二氧化碳通入氢氧化钠溶液中无明显现象,那它们发生化学反应了吗?同学们决定对该问题进行探究.
【提出猜想】二氧化碳与氢氧化钠溶液发生了化学反应.
【实验验证】
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 将二氧化碳通入盛有氢氧化钠溶液的试管中,向试管中滴加无色酚酞溶液 | 溶液变为红色 | 氢氧化钠没有与二氧化碳发生反应 |
| 实验二 | 取一矿泉水瓶,收集满一瓶二氧化碳,向矿泉水瓶加入少量氢氧化钠溶液,振荡 | 矿泉水瓶 变瘪 | 氢氧化钠与二氧化碳发生了化学反应 |
| 实验三 | 将二氧化碳通入盛有氢氧化钠溶液的试管中,然后向试管中滴加足量稀盐酸 | 产生气泡 | 氢氧化钠与二氧化碳发生了化学反应 |
(2)小明认为实验二不严谨,原因是二氧化碳能够溶于水,并且能和水反应生成碳酸.
请你写出一种改进实验的方法:取另一相同矿泉水瓶,收集满二氧化碳,向矿泉水瓶中加入和氢氧化钠溶液体积相同的水,振荡观察现象.
(3)请写出实验三种产生实验现象的反应的化学方程式:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
【拓展分析】(4)实验三中,除滴加稀盐酸外,可以滴加的盐溶液有氯化钙溶液(写一种即可)
9.由于MnO2和CuSO4溶液都能作H2O2溶液分解的催化剂,某校化学兴趣小组想探究其他一些金属氧化物和盐溶液是否也可以作H2O2溶液分解的催化剂.请你参与他们的探究过程.
【进行猜想】小华的猜想:Al2O3能作过氧化氢分解的催化剂.
小明的猜想:FeCl3溶液能作过氧化氢分解的催化剂.
【实验验证】请你填写下表空白处:
【反思】①有的同学认为小华的实验,不能完全证明Al2O3是H2O2溶液分解的催化剂.还应补充探究Al2O3在反应前后质量和化学性质没有改变.
②已知FeCl3在水中可解离出Fe3+和Cl-,同学们又提出以下猜想:
甲同学的猜想是:真正催化分解H2O2的是FeCl3溶液中的H2O;
乙同学的猜想是:真正催化分解H2O2的是FeCl3溶液中的Fe3+;
丙同学的猜想是:真正催化分解H2O2的是FeCl3溶液中的Cl-;
同学们认为最不可能的是甲同学的猜想,理由是过氧化氢溶液中有水.
同学们对余下的两个猜想,用实验进行了探究.请你完成下面的实验报告:
【进行猜想】小华的猜想:Al2O3能作过氧化氢分解的催化剂.
小明的猜想:FeCl3溶液能作过氧化氢分解的催化剂.
【实验验证】请你填写下表空白处:
| 实验步骤 | 实验操作 | 实验现象 | 结论 |
| 小华的实验 |  | ③的现象是 试管中有大量气泡产生,带火星的木条复燃 | Al2O3和FeCl3溶液都能作为H2O2溶液分解的催化剂 |
| 小明的实验 |  |
②已知FeCl3在水中可解离出Fe3+和Cl-,同学们又提出以下猜想:
甲同学的猜想是:真正催化分解H2O2的是FeCl3溶液中的H2O;
乙同学的猜想是:真正催化分解H2O2的是FeCl3溶液中的Fe3+;
丙同学的猜想是:真正催化分解H2O2的是FeCl3溶液中的Cl-;
同学们认为最不可能的是甲同学的猜想,理由是过氧化氢溶液中有水.
同学们对余下的两个猜想,用实验进行了探究.请你完成下面的实验报告:
| 实验过程 | 实验现象 | 结论 |
| 向盛有5mL5%的H2O2溶液的试管中加入少量 的HCl,并把带火星的木条伸入试管. | 无明显现象 | Cl-不能催化分解H2O2 |
| 向盛有5mL5%的H2O2溶液的试管中加入少量 的Fe(NO3)3溶液,并把带火星的木条伸入试管. | 试管中有大量气泡产生,带火星的木条复燃 | 乙同学猜想成立,反应的化学方程式是2H2O2$\frac{\underline{\;FeCl_{3}\;}}{\;}$2H2O+O2↑ |
6.某温度下,氯化镁饱和溶液浓度为40%,在足量的此溶液中加入4.6g无水氯化镁,最终析出结晶水合物40.6g,则该结晶水合物的化学式是( )
| A. | MgCl2•7H2O | B. | MgCl2•2H2O | C. | MgCl2•6H2O | D. | MgCl2•5H2O |
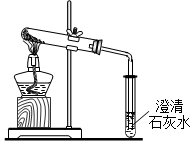 取少量碳酸氢钠(NaHCO3)粉末,用如图装置进行实验,充分加热后发现:大试管中管口有水珠出现,管底有白色固体残留;小试管中澄清石灰水变浑浊.完全反应后,取残留固体溶于水配成溶液,往该溶液中滴加CaCl2溶液,有白色沉淀生成.
取少量碳酸氢钠(NaHCO3)粉末,用如图装置进行实验,充分加热后发现:大试管中管口有水珠出现,管底有白色固体残留;小试管中澄清石灰水变浑浊.完全反应后,取残留固体溶于水配成溶液,往该溶液中滴加CaCl2溶液,有白色沉淀生成.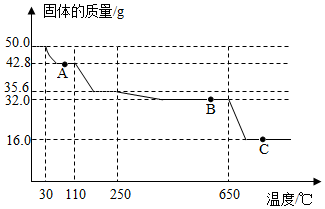 将50g胆矾放在坩埚中加热,使温度缓慢升高,在加热过程中,温度与残余固体质量的关系如图所示:
将50g胆矾放在坩埚中加热,使温度缓慢升高,在加热过程中,温度与残余固体质量的关系如图所示: