题目内容
8.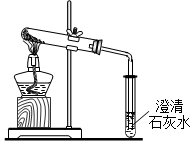 取少量碳酸氢钠(NaHCO3)粉末,用如图装置进行实验,充分加热后发现:大试管中管口有水珠出现,管底有白色固体残留;小试管中澄清石灰水变浑浊.完全反应后,取残留固体溶于水配成溶液,往该溶液中滴加CaCl2溶液,有白色沉淀生成.
取少量碳酸氢钠(NaHCO3)粉末,用如图装置进行实验,充分加热后发现:大试管中管口有水珠出现,管底有白色固体残留;小试管中澄清石灰水变浑浊.完全反应后,取残留固体溶于水配成溶液,往该溶液中滴加CaCl2溶液,有白色沉淀生成.(1)小试管中澄清石灰水变浑浊,说明碳酸氢钠受热有CO2生成(填化学式).
(2)通过上述实验,下列归纳出的碳酸氢钠性质
或推理正确的有B(填编号).
A.NaHCO3能与NaOH溶液发生反应
B.NaHCO3受热易分解:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$ Na2CO3+CO2↑+H2O
C.无法比较NaHCO3与Na2CO3受热分解的难易程度.
分析 (1)根据二氧化碳能使澄清石灰水变浑浊考虑;
(2)根据题中信息结合所学化学知识进行分析即可.
解答 解:(1)二氧化碳能使澄清石灰水变浑浊,小试管中澄清石灰水变浑浊,说明碳酸氢钠受热生成了二氧化碳;
(2)A、该实验无法判断NaHCO3能与NaOH溶液是否能发生反应,故错误.
B、大试管中管口有水珠出现,说明碳酸氢钠受热生成了水,小试管中澄清石灰水变浑浊,说明碳酸氢钠受热生成了二氧化碳,取残留固体溶于水配成溶液,往该溶液中滴加CaCl2溶液,有白色沉淀生成,说明生成了碳酸盐,因为碳酸氢钠中含有钠元素,所以生成了碳酸钠,即碳酸氢钠加热生成了碳酸钠、水、二氧化碳,用观察法配平即可,故正确;
C、由于碳酸氢钠加热生成了碳酸钠,所以加热时NaHCO3比Na2CO3易分解,故错误.
故答案为:(1)CO2;(2)B.
点评 解答本题关键是要知道从题干中所给的信息中提取有用信息.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案
相关题目
18.在学习中要不断总结,归纳发现规律,就能不断提高自己的能力.在标准状况下各气体相对分子质量、密度和实验室收集方法如下表,通过比较找出规律:
(1)从“相对分子质量”和“标况下密度”两列,可归纳出:一般来说,气体相对分子质量越大,标准状况下的密度越大;
(2)密度大于空气的气体可采用向上排空气法收集.
(3)实验室制取的氨气(化学式为NH3),可推测知密度比空气小,可用向下排空气法收集(氨气极易溶于水).
| 气体 | 相对分子质量 | 标况下密度(g/L) | 收集方法 |
| 空气 | 29 | 1.293 | 排水集气法 |
| 氧气 | 32 | 1.429 | 向上排空气法 |
| 二氧化碳 | 44 | 1.964 | 向上排空气法 |
| 氢气 | 2 | 0.089 | 向下排空气法 |
(2)密度大于空气的气体可采用向上排空气法收集.
(3)实验室制取的氨气(化学式为NH3),可推测知密度比空气小,可用向下排空气法收集(氨气极易溶于水).
16.2017年6月1日,大连理工大学梁长海团队研发出单相金属硅化物作为苯乙炔高效选择加氢催化剂.该工作开发的一系列金属硅化物催化剂,为工业选择加氢催化剂设计提供了一种思路,具有一定的学术意义和实际应用潜力.下列说法不正确的是( )
| A. | 催化剂是催化反应的核心 | |
| B. | 金属硅化物属于化合物 | |
| C. | 在化学反应中能加快其他物质的反应速率,而本身的质量和性质在化学反应前后都没有改变的物质称为催化剂 | |
| D. | 催化剂只能改变化学反应速率,不能增加或减少生成物的质量 |
3.某兴趣小组对4瓶无色溶液Na2CO3溶液、NaOH溶液、Ca(OH)2溶液、稀盐酸进行鉴别.
(1)甲组同学利用紫色石蕊试液进行鉴别.
乙组同学不用其他试剂进行鉴别.
乙组同学经过交流后发现,根据小红与小敏的实验现象,小红的结论是错误的.如果小刚所滴加的是NaOH溶液,则他的实验现象是三支试管都无现象.
(1)甲组同学利用紫色石蕊试液进行鉴别.
| 实验步骤 | 现象与结论 |
| ①用4支试管,分别取少量的不同溶液,各滴加紫色石蕊试液. | 1支试管中出现红色,则原溶液是稀盐酸. |
| ②另用3支试管,分别取少量未确定的溶液,各滴加步骤①检验出的溶液. | 1支试管中有气泡产生.则原溶液是Na2CO3溶液. |
| ③另用2支试管,分别取少量未确定的溶液,分别滴加碳酸钠溶液. | 1支试管中有白色沉淀析出,则原溶液是Ca(OH)2溶液. 1支试管中无现象,则原溶液是NaOH溶液. |
| 同学 | 实验操作 | 现 象 | 结 论 |
| 小敏 | 用3支试管,分别取少量不同的溶液,各滴加剩余的另一种溶液. | 1支试管中有气泡产生,其余2支试管中无现象. | 所滴加的溶液是稀盐酸. |
| 小红 | 1支试管中有白色沉淀析出,其余2支试管中无现象. | 所滴加的溶液是Na2CO3溶液. | |
| 小刚 | … | … |
17.实验操作正确的是( )
| A. | 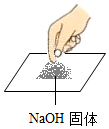 取用氢氧化钠固体 | B. |  取用氯化钠固体 | ||
| C. |  取用液体 | D. | 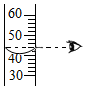 读取液体体积 |
 小李用甲图气体发生装置制取二氧化碳,老师给他提供了石灰石、无标签的稀盐酸和氯化钠水溶液各一瓶.
小李用甲图气体发生装置制取二氧化碳,老师给他提供了石灰石、无标签的稀盐酸和氯化钠水溶液各一瓶.