题目内容
5.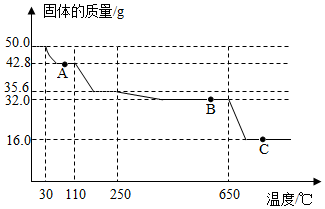 将50g胆矾放在坩埚中加热,使温度缓慢升高,在加热过程中,温度与残余固体质量的关系如图所示:
将50g胆矾放在坩埚中加热,使温度缓慢升高,在加热过程中,温度与残余固体质量的关系如图所示:A点的固体成分是CuSO4•3H2O,
B点的固体成分是CuSO4,
C点的固体成分是CuO.
分析 根据失去水的质量,根据关系式:CuSO4•5H2O~CuSO4•xH2O利用差量法求出x,从而得出化学式;无水硫酸铜进一步受热时可以生成氧化铜和三氧化硫.
解答 解:A点时,失去水的质量为50.0g-42.8g=7.2g
CuSO4•5H2O~CuSO4•xH2O△m
250 18(5-x)
50.0g 7.2g
则$\frac{250}{50.0g}=\frac{18(5-x)}{7.2g}$,
解得:x=3,
所以在A点时所得固体的成分为CuSO4•3H2O,故填:CuSO4•3H2O;
B点时,失去水的质量为50.0g-32.0g=18g
CuSO4•5H2O~CuSO4•xH2O△m
250 18(5-x)
50.0g 18g
$\frac{250}{50.0g}=\frac{18(5-x)}{18g}$
x=0,
所以在B点时所得固体的成分为CuSO4,故填:CuSO4;
C点时,为无水硫酸铜进一步受热,
设完全转化为氧化铜质量为w
CuSO4•5H2O~CuSO~CuO
250 80
50.0g w
$\frac{250}{50.0g}=\frac{80}{w}$
w=16g
正好等于剩余固体的质量,所以C点时固体成分是CuO,故填:CuO.
点评 该题为硫酸铜晶体的受热知识为线索,考查了多方面的知识,综合性很强,难度较大.

 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案| A. |  | B. |  | C. |  | D. |  |
| A. | 催化剂是催化反应的核心 | |
| B. | 金属硅化物属于化合物 | |
| C. | 在化学反应中能加快其他物质的反应速率,而本身的质量和性质在化学反应前后都没有改变的物质称为催化剂 | |
| D. | 催化剂只能改变化学反应速率,不能增加或减少生成物的质量 |
| A. | 100克水最多可溶解36克氯化钠,则氯化钠的溶解度为36克 | |
| B. | 20℃时100克饱和氯化钠溶液中含有26克氯化钠,则20℃时氯化钠的溶解度为26克 | |
| C. | 25℃时100克水中溶解了35克氯化钠,则25℃时氯化钠的溶解度为35克 | |
| D. | 20℃时50克水中最多溶解氯化钠18克,则20℃时氯化钠的溶解度为36克 |
| A. | 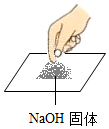 取用氢氧化钠固体 | B. |  取用氯化钠固体 | ||
| C. |  取用液体 | D. | 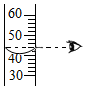 读取液体体积 |
 用某金属颗粒与足量的稀盐酸反应,如生成氢气的质量(以纵坐标表示,单位:g)与所用金属的质量(以横坐标表示,单位:g)之间的关系如图,该金属颗粒可能是( )
用某金属颗粒与足量的稀盐酸反应,如生成氢气的质量(以纵坐标表示,单位:g)与所用金属的质量(以横坐标表示,单位:g)之间的关系如图,该金属颗粒可能是( )| A. | 纯净的锌 | B. | 含铜的锌 | ||
| C. | 含有不与酸反应的杂质的锌 | D. | 含有不与酸反应的杂质的铁 |
 小李用甲图气体发生装置制取二氧化碳,老师给他提供了石灰石、无标签的稀盐酸和氯化钠水溶液各一瓶.
小李用甲图气体发生装置制取二氧化碳,老师给他提供了石灰石、无标签的稀盐酸和氯化钠水溶液各一瓶.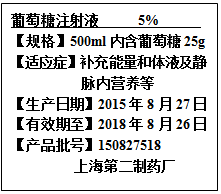 医生给病人输液时,常用葡萄糖注射液.如图为葡萄糖注射液的部分标签图,(葡萄糖注射液密度近似水的密度)根据右图回答下列问题
医生给病人输液时,常用葡萄糖注射液.如图为葡萄糖注射液的部分标签图,(葡萄糖注射液密度近似水的密度)根据右图回答下列问题