题目内容
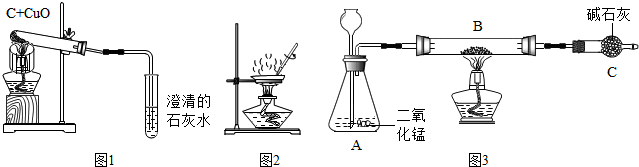
1.某校化学学习小组在学习碳的化学性质的过程中,按如图1进行了木炭与氧化铜在高温加热条件下反应的实验.【小组实验】
(1)木炭与氧化铜反应的化学方程式是C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
(2)该同学现察到反应的现象一是:澄清石灰水变浑浊.
现象二是:冷却后的试管里的粉末由黑色变成红色.
【提出猜想】
(3)小组某同学对充分反应冷却后的试管里粉末的成分,提出了如下猜想,请将猜想五补充完整.
猜想一:粉末是铜
猜想二:粉末是氧化铜
猜想三:粉末是铜、氧化铜和木炭
猜想四:粉末是铜和木炭
猜想五:粉末是氧化铜、铜
【设计实验、验证猜想】
(4)上述猜想中,明显不合理的是猜想三;
(5)小组同学为了验证猜想一的成立,设计了如图2实验,取样品粉末于钳埚中,通过称取加热前后粉末的质量来进行实验.要证明猜想一成立的依据是红色粉末变成黑色.用相同的实验来证明猜想四可(填“可”或“不可”)行.试说明理由.
【拓展延伸】
如果猜想四成立,某同学再用如图3所示装置(铁架台等略).取10.0g粉末放入装置B中,通过测出的反应前后装置C的质量來测定粉末中钢的质量分数.
| 反应前/g | 反应后/g | |
| 装置C的质量 | 10.0 | 14.4 |
通过计算,粉末中铜的质量分数是88%.
【问题和讨论】
(7)实验完成后,老师评议说:“为了减少实验的误差,上述实验设计还需要做两处改进.”其改进的措施是在B装置前加浓硫酸的干燥装置,在C装置后再加一个碱石灰装置.
分析 【小组实验】(1)根据碳和氧化铜在高温的条件下生成铜和二氧化碳进行分析;
(2)根据二氧化碳和氢氧化钙反应会生成碳酸钙沉淀和水,氧化铜是黑色,铜是红色金属进行分析;
【提出猜想】(3)根据反应物和生成物的组合进行猜想;
【设计实验、验证猜想】(4)根据氧化铜和碳高温会发生反应进行分析;
(5)根据铜和氧气加热会生成氧化铜,碳和氧气点燃会生成二氧化碳进行分析;
【拓展延伸】根据碱石灰增加的质量就是二氧化碳的质量,然后依据化学方程式进行计算;
【问题和讨论】(7)根据过氧化氢溶液中的水蒸气、空气中的二氧化碳会与碱石灰反应进行分析.
解答 解:【小组实验】(1)碳和氧化铜在高温的条件下生成铜和二氧化碳,化学方程式为:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑;
(2)二氧化碳和氢氧化钙反应会生成碳酸钙沉淀和水,氧化铜是黑色,铜是红色金属,所以同学现察到反应的现象一是:澄清石灰水变浑浊,现象二是:冷却后的试管里的粉末由黑色变成红色;
【提出猜想】(3)通过分析题中的猜想可知,猜想五:氧化铜、铜;
【设计实验、验证猜想】(4)氧化铜和碳高温会发生反应,所以明显不合理的是猜想三;
(5)铜和氧气加热会生成氧化铜,所以要证明猜想一成立的依据是红色粉末变成黑色,碳和氧气点燃会生成二氧化碳,所以用相同的实验来证明猜想四可行,理由是:加热固体粉末,固体粉末减少;
【拓展延伸】碱石灰增加的质量就是二氧化碳的质量,所以二氧化碳的质量是:4.4g,
设参加反应的碳的质量为x
C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,
12 44
x 4.4g
$\frac{12}{x}$=$\frac{44}{4.4g}$
x=1.2g
所以铜的质量分数为:$\frac{10g-1.2g}{10g}$×100%=88%;
【问题和讨论】(7)过氧化氢溶液中的水蒸气、空气中的二氧化碳会与碱石灰反应,所以改进的措施是:在B装置前加浓硫酸的干燥装置,在C装置后再加一个碱石灰装置.
故答案为:【小组实验】(1)C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑;
(2)澄清石灰水变浑浊,由黑色变成红;
【提出猜想】(3)氧化铜、铜;
【设计实验、验证猜想】(4)三;
(5)红色粉末变成黑色,加热固体粉末,固体粉末减少;
【拓展延伸】88;
【问题和讨论】(7)在B装置前加浓硫酸的干燥装置,在C装置后再加一个碱石灰装置.
点评 在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中的提示进行解答.

 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案| A. | 甲醛会破坏蛋白质的结构使其变质,可用来浸泡水产品以防腐 | |
| B. | 氢氧化钠固体能吸水,可用来干燥CO2气体 | |
| C. | 葡萄糖氧化时放出能量,可用来为人体供能 | |
| D. | 氢氧化钠能与酸反应,可用来治疗胃酸过多 |
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(g) | 12 | 5 | 8 | 3 |
| 反应后质量(g) | 0 | 5 | 17 | x |
| A. | x的值为6 | |
| B. | 乙一定是催化剂 | |
| C. | 反应中的丙和丁的质量之比为3:1 | |
| D. | 该反应中甲和丙的计量数之比为1:3,则甲和丙的相对分子质量之比为4:1 |
 小琪往图所示的烧杯中加入一种物质,搅拌后,发现塑料片脱离了烧杯.她加入的物质是C
小琪往图所示的烧杯中加入一种物质,搅拌后,发现塑料片脱离了烧杯.她加入的物质是C