题目内容
6.金属材料与人类的生产和生活密切相关,请回答:(1)下列用品中,主要利用金属导电性的是C(填字母).
A.铂金饰品 B.铁锅 C.铝导线
(2)为了验证铝、铜、银三种金属的活动性顺序,设计了下列四种方案,其中可行的是①④.(填序号)
①将铝、银分别浸入到硫酸铜溶液中
②将银分别浸入到硫酸铝、硫酸铜溶液中
③将铜、银分别浸入到硫酸铝溶液中
④将铜分别浸入到硫酸铝、硝酸银溶液中
(3)在氯化铜和氯化亚铁的混合溶液中加入一定质量的镁粉,充分反应后过滤,得到滤渣和滤液.滤液中一定含有的溶质是MgCl2(填化学式).
(4)某钢铁厂每天需消耗4900t含Fe2O376%的赤铁矿石,该厂理论上可日产含Fe98%的生铁多少吨?
分析 (1)根据金属材料的性质和用途分析回答;
(2)在金属活动顺序表中,前边的金属可以把后边的金属从其盐溶液中置换出来,所以可以选择相应的金属和盐溶液进行反应来证明这三种金属的活动性强弱;
(3)根据金属与盐溶液的反应分析回答;
(4)利用赤铁矿石的质量与赤铁矿石中氧化铁的质量分数和生铁中铁的质量分数,根据氧化铁与一氧化碳反应的化学方程式,可以计算出生铁的质量.
解答 解:(1)在常见的金属材料用品中,铝导线主要利用金属导电性;
(2)①铝与硫酸铜反应,可验证铝的活动性比铜强.银与硫酸铜不反应,可知银的活动性比铜弱,可验证铝、铜、银三种金属的活动性顺序,故①是可行的方案;
②银与硫酸铝、硫酸铜都不反应反应,可验证铝、铜的活动性比银强.与但不能验证铝、铜的活动性,不可验证铝、铜、银三种金属的活动性顺序,故②是不可行的方案;
③铜、银与硫酸铝都不反应反应,可验证铝的活动性比铜、银强.但不能验证铜、银的活动性,不可验证铝、铜、银三种金属的活动性顺序,故③是不可行的方案;
④铜与硫酸铝不反应,可知铜的活动性比铝弱;铜与硝酸银反应,可验证铜的活动性比银强,可验证铝、铜、银三种金属的活动性顺序,故④是可行的方案,;
故选:①④;
(3)在氯化铜和氯化亚铁的混合溶液中加入一定量的镁粉,充分反应后过滤,得到滤渣和滤液,由于镁的活泼性大于同和铜、铁,能与氯化铜和氯化亚铁反应,则滤液中一定含有的溶质是MgCl2,不能确定氯化铜和氯化亚铁的存在;
(4)设日产含Fe98%的生铁的质量为x
Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
160 112
4900t×76% x×98%
$\frac{160}{4900t×76%}$=$\frac{112}{x×98%}$
x=2660t
故答案为:(1)C;
(2)①④;
(3)①MgCl2;
(4)2660t.
点评 金属的活动性顺序表以及金属与酸、金属与盐溶液反应的条件,是初中化学的重点内容,要求学生一定要牢牢的掌握,并会加以运用.

 消化药片所含的物质能中和胃里过多的胃酸.某种消化药品的标记如右图所示.医生给某胃酸过多的患者开出服用此药的处方为:每日三次,每次二片.试计算:患者按处方服用该药一天,理论上可中和氢氯酸多少毫克?
消化药片所含的物质能中和胃里过多的胃酸.某种消化药品的标记如右图所示.医生给某胃酸过多的患者开出服用此药的处方为:每日三次,每次二片.试计算:患者按处方服用该药一天,理论上可中和氢氯酸多少毫克? | A. | 尿素 | B. | 氯化铵 | C. | 硫酸铵 | D. | 硝酸铵 |
【小组实验】
(1)木炭与氧化铜反应的化学方程式是C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
(2)该同学现察到反应的现象一是:澄清石灰水变浑浊.
现象二是:冷却后的试管里的粉末由黑色变成红色.
【提出猜想】
(3)小组某同学对充分反应冷却后的试管里粉末的成分,提出了如下猜想,请将猜想五补充完整.
猜想一:粉末是铜
猜想二:粉末是氧化铜
猜想三:粉末是铜、氧化铜和木炭
猜想四:粉末是铜和木炭
猜想五:粉末是氧化铜、铜
【设计实验、验证猜想】
(4)上述猜想中,明显不合理的是猜想三;
(5)小组同学为了验证猜想一的成立,设计了如图2实验,取样品粉末于钳埚中,通过称取加热前后粉末的质量来进行实验.要证明猜想一成立的依据是红色粉末变成黑色.用相同的实验来证明猜想四可(填“可”或“不可”)行.试说明理由.
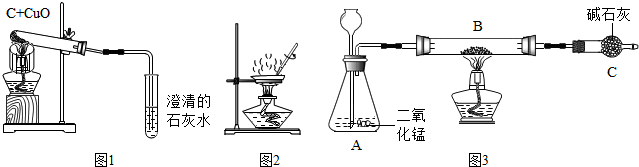
【拓展延伸】
如果猜想四成立,某同学再用如图3所示装置(铁架台等略).取10.0g粉末放入装置B中,通过测出的反应前后装置C的质量來测定粉末中钢的质量分数.
| 反应前/g | 反应后/g | |
| 装置C的质量 | 10.0 | 14.4 |
通过计算,粉末中铜的质量分数是88%.
【问题和讨论】
(7)实验完成后,老师评议说:“为了减少实验的误差,上述实验设计还需要做两处改进.”其改进的措施是在B装置前加浓硫酸的干燥装置,在C装置后再加一个碱石灰装置.
| A. | 硫在空气中燃烧-蓝紫色火焰,生成三氧化硫 | |
| B. | 木炭在空气中燃烧-生成有刺激性气味的气体 | |
| C. | 镁在氧气中燃烧-生成白色固体,发出耀眼的白光 | |
| D. | 氯酸钾受热分解-生成氧气和氯化钾,并放出热量 |
| A. | 淀粉与碘作用呈红色 | |
| B. | 常温下油脂都呈固态 | |
| C. | 青菜、黄瓜中含大量的油脂 | |
| D. | 葡萄糖在人体内缓慢氧化为二氧化碳和水并释放出热量 |
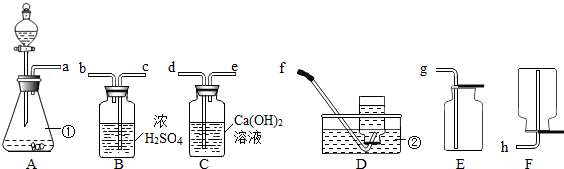
 侯氏联合制碱法其反应的化学方程式:
侯氏联合制碱法其反应的化学方程式: