题目内容
2. 小琪往图所示的烧杯中加入一种物质,搅拌后,发现塑料片脱离了烧杯.她加入的物质是C
小琪往图所示的烧杯中加入一种物质,搅拌后,发现塑料片脱离了烧杯.她加入的物质是CA.食盐 B.硝酸铵 C.生石灰 D.氢氧化钾.
分析 由于用石蜡粘住的塑料片脱落,说明加入物质在溶解或者反应过程中放热.有的物质溶于水时会放出热量,使溶液温度升高,如浓硫酸、氢氧化钾等,也可以是反应过程中是放热的,如氧化钙溶解于水.
解答 解:A、食盐溶于水时,溶液温度变化不大,石蜡仍为固态,粘在烧杯上的塑料片不会脱落.
B、甲烧杯中加入硝酸铵晶体,溶于水时吸收热量,使溶液的温度降到0℃以下,石蜡仍为固态,粘在烧杯上的塑料片不会脱落.
C、氧化钙 放入水中与水反应放出热量会使石蜡熔化,粘在烧杯上的塑料片脱落;
D.补充:由于是石蜡融化,所以加入的物质可以是溶解放热,也可以是反应放热,所以可以补充为硫酸、氢氧化钾等物质.
故答案为:C; 氢氧化钾(硫酸等).
点评 物质溶解于水时有三种表现:溶解时放出热量使溶液温度升高,以氢氧化钠、浓硫酸为代表;溶解时吸收热量使溶液温度降低,以硝酸铵为代表;其它大部分物质溶解时无明显的热量变化,溶液温度基本保持不变.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.有XYZ三种金属,把Y投入X(NO3)2溶液中,Y表面有X析出,Y和Z的金属同时加到稀盐酸中,Z比Y反应剧烈,则三种金属活动性由强到弱的顺序是( )
| A. | X Y Z | B. | X Z Y | C. | Y X Z | D. | Z Y X |
13.如图所示图象能正确反应其对应的实验操作的是( )
| A. | 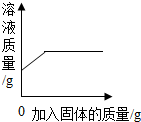 一定温度下,向饱和的硝酸钾溶液中不断加入硝酸钾固体 | |
| B. | 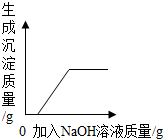 向硫酸和硫酸铜混合溶液中滴加过量的氢氧化钠溶液 | |
| C. | 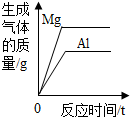 将等质量的镁粉和铝粉分别与足量等浓度的稀硫酸反应 | |
| D. | 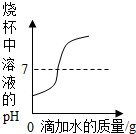 向盛有一定量稀硫酸的烧杯中不断加水稀释 |
10. 消化药片所含的物质能中和胃里过多的胃酸.某种消化药品的标记如右图所示.医生给某胃酸过多的患者开出服用此药的处方为:每日三次,每次二片.试计算:患者按处方服用该药一天,理论上可中和氢氯酸多少毫克?
消化药片所含的物质能中和胃里过多的胃酸.某种消化药品的标记如右图所示.医生给某胃酸过多的患者开出服用此药的处方为:每日三次,每次二片.试计算:患者按处方服用该药一天,理论上可中和氢氯酸多少毫克?
 消化药片所含的物质能中和胃里过多的胃酸.某种消化药品的标记如右图所示.医生给某胃酸过多的患者开出服用此药的处方为:每日三次,每次二片.试计算:患者按处方服用该药一天,理论上可中和氢氯酸多少毫克?
消化药片所含的物质能中和胃里过多的胃酸.某种消化药品的标记如右图所示.医生给某胃酸过多的患者开出服用此药的处方为:每日三次,每次二片.试计算:患者按处方服用该药一天,理论上可中和氢氯酸多少毫克?
7.小麦在生长过程中施用氮肥,下列氮肥中能和熟石灰混用的是( )
| A. | 尿素 | B. | 氯化铵 | C. | 硫酸铵 | D. | 硝酸铵 |
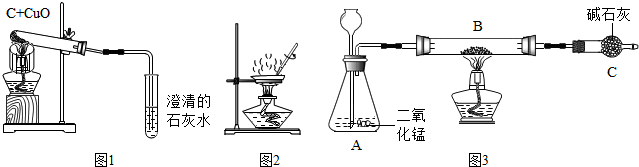
1.某校化学学习小组在学习碳的化学性质的过程中,按如图1进行了木炭与氧化铜在高温加热条件下反应的实验.
【小组实验】
(1)木炭与氧化铜反应的化学方程式是C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
(2)该同学现察到反应的现象一是:澄清石灰水变浑浊.
现象二是:冷却后的试管里的粉末由黑色变成红色.
【提出猜想】
(3)小组某同学对充分反应冷却后的试管里粉末的成分,提出了如下猜想,请将猜想五补充完整.
猜想一:粉末是铜
猜想二:粉末是氧化铜
猜想三:粉末是铜、氧化铜和木炭
猜想四:粉末是铜和木炭
猜想五:粉末是氧化铜、铜
【设计实验、验证猜想】
(4)上述猜想中,明显不合理的是猜想三;
(5)小组同学为了验证猜想一的成立,设计了如图2实验,取样品粉末于钳埚中,通过称取加热前后粉末的质量来进行实验.要证明猜想一成立的依据是红色粉末变成黑色.用相同的实验来证明猜想四可(填“可”或“不可”)行.试说明理由.
【拓展延伸】
如果猜想四成立,某同学再用如图3所示装置(铁架台等略).取10.0g粉末放入装置B中,通过测出的反应前后装置C的质量來测定粉末中钢的质量分数.
(己知:碱石灰是生石灰(CaO)和氢气化钠固体混合物,是一种干燥剂,它还能吸收二氧化碳气体)
通过计算,粉末中铜的质量分数是88%.
【问题和讨论】
(7)实验完成后,老师评议说:“为了减少实验的误差,上述实验设计还需要做两处改进.”其改进的措施是在B装置前加浓硫酸的干燥装置,在C装置后再加一个碱石灰装置.
【小组实验】
(1)木炭与氧化铜反应的化学方程式是C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
(2)该同学现察到反应的现象一是:澄清石灰水变浑浊.
现象二是:冷却后的试管里的粉末由黑色变成红色.
【提出猜想】
(3)小组某同学对充分反应冷却后的试管里粉末的成分,提出了如下猜想,请将猜想五补充完整.
猜想一:粉末是铜
猜想二:粉末是氧化铜
猜想三:粉末是铜、氧化铜和木炭
猜想四:粉末是铜和木炭
猜想五:粉末是氧化铜、铜
【设计实验、验证猜想】
(4)上述猜想中,明显不合理的是猜想三;
(5)小组同学为了验证猜想一的成立,设计了如图2实验,取样品粉末于钳埚中,通过称取加热前后粉末的质量来进行实验.要证明猜想一成立的依据是红色粉末变成黑色.用相同的实验来证明猜想四可(填“可”或“不可”)行.试说明理由.

【拓展延伸】
如果猜想四成立,某同学再用如图3所示装置(铁架台等略).取10.0g粉末放入装置B中,通过测出的反应前后装置C的质量來测定粉末中钢的质量分数.
| 反应前/g | 反应后/g | |
| 装置C的质量 | 10.0 | 14.4 |
通过计算,粉末中铜的质量分数是88%.
【问题和讨论】
(7)实验完成后,老师评议说:“为了减少实验的误差,上述实验设计还需要做两处改进.”其改进的措施是在B装置前加浓硫酸的干燥装置,在C装置后再加一个碱石灰装置.
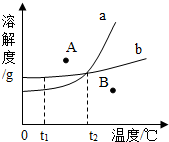 如图是某实验小组的同学绘制的两种固体物质的溶解度曲线图.请你根据图示回答问题:
如图是某实验小组的同学绘制的两种固体物质的溶解度曲线图.请你根据图示回答问题:
 同学为了测定实验室一瓶稀盐酸的溶质质量分数,他们没有找到纯金属,只好用铜锌合金和此盐酸完成了如图所示的实验.
同学为了测定实验室一瓶稀盐酸的溶质质量分数,他们没有找到纯金属,只好用铜锌合金和此盐酸完成了如图所示的实验.