题目内容
5.在一张洁白干燥的滤纸上依次喷洒 A、B、C三种无色液体,当喷洒A时滤纸无明显变化,再喷洒B时滤纸上显出一间红色小屋,最后喷洒C时红色小屋又消失了,回答下列问题:滤纸上的小屋事先是用酚酞试剂画出的.无色溶液A是水; B是氢氧化钠; C是稀盐酸.分析 根据已有的知识进行分析解答,酚酞试液在碱性溶液中变红,在酸性和中性溶液中不变色,酸和碱能中和生成盐和水,据此解答.
解答 解:白色的滤纸,说明是用酚酞试液画的,酚酞在酸性和中性溶液中不变色,在碱性溶液中变红,故喷洒的A可以是水,B是氢氧化钠溶液,当喷C时红色消失,说明碱性消失,故喷洒的C是酸性溶液,可以是盐酸,故填:酚酞,水,氢氧化钠,稀盐酸.
点评 本题考查了酸碱指示剂与溶液酸碱性的关系,完成此题,可以依据已有的知识进行.

练习册系列答案
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
15.市场上有一种“吹不灭”的蜡烛,外表和普通蜡烛一模一样,但是点燃后任你怎么吹都不灭.到底这种蜡烛中有什么玄机呢?学校化学兴趣小组决定一探究竟.
【查阅资料】普通蜡烛由石蜡和蜡烛芯制成的,而吹不灭的蜡烛是在蜡烛芯上包裹一层打火石的粉末.打火石是由某种金属掺入少量稀土元素制成的合金,它的着火点只有150℃.当蜡烛燃烧时,金属并不燃烧;但当蜡烛吹灭后,未冷却的金属接触到氧气就发生燃烧,从而使蜡烛复燃.
【探究与反思】
(1)打火石是混合物(填“混合物”或“纯净物”).
(2)这种蜡烛燃烧时,蜡烛芯里的金属为什么不燃烧?金属被石蜡包围,无法接触到氧气.
(3)这种蜡烛也可以熄灭,你采用的方法是隔绝氧气.
【实验探究】吹不灭的蜡烛芯内的金属可能是镁、铝、铁或铜中的一种,为确定该金属的成分,请你继续探究并完成下列有关问题:(注:不考虑打火石中稀土元素对探究金属性质的影响)
【分析思考】
请写出“实验3”中可能涉及到的化学方程式Mg+CuSO4=MgSO4+Cu.
【查阅资料】普通蜡烛由石蜡和蜡烛芯制成的,而吹不灭的蜡烛是在蜡烛芯上包裹一层打火石的粉末.打火石是由某种金属掺入少量稀土元素制成的合金,它的着火点只有150℃.当蜡烛燃烧时,金属并不燃烧;但当蜡烛吹灭后,未冷却的金属接触到氧气就发生燃烧,从而使蜡烛复燃.
【探究与反思】
(1)打火石是混合物(填“混合物”或“纯净物”).
(2)这种蜡烛燃烧时,蜡烛芯里的金属为什么不燃烧?金属被石蜡包围,无法接触到氧气.
(3)这种蜡烛也可以熄灭,你采用的方法是隔绝氧气.
【实验探究】吹不灭的蜡烛芯内的金属可能是镁、铝、铁或铜中的一种,为确定该金属的成分,请你继续探究并完成下列有关问题:(注:不考虑打火石中稀土元素对探究金属性质的影响)
| 实验 | 操作步骤 | 实验现象 | 实验结论 |
| 1 | 切开蜡烛,取出打火石,用砂纸打磨 | 打火石是银白色 | |
| 2 | 取少量打磨后的打火石加试管中,滴加盐酸 | 该金属一定不是铁 | |
| 3 | 取少量打磨后的打火石加试管中,滴加硫酸铜溶液 | 有色物质析出 | 该金属一定是镁 |
请写出“实验3”中可能涉及到的化学方程式Mg+CuSO4=MgSO4+Cu.
16.生活中的下列现象,属于化学变化的是( )
| A. | 海水晒盐 | B. | 胆矾研碎 | C. | 盐酸除锈 | D. | 石油分馏 |
13.如图所示图象能正确反应其对应的实验操作的是( )
| A. | 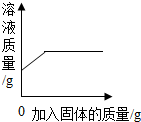 一定温度下,向饱和的硝酸钾溶液中不断加入硝酸钾固体 | |
| B. | 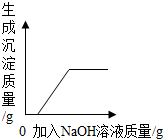 向硫酸和硫酸铜混合溶液中滴加过量的氢氧化钠溶液 | |
| C. | 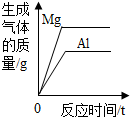 将等质量的镁粉和铝粉分别与足量等浓度的稀硫酸反应 | |
| D. | 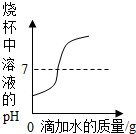 向盛有一定量稀硫酸的烧杯中不断加水稀释 |
20.物质的用途与性质密切相关.下列说法正确的是( )
| A. | 小苏打能作发酵粉,是因为小苏打能与面粉反应 | |
| B. | 洗洁精能洗去碗筷上的油污,是因为油污能溶于洗洁精 | |
| C. | 浓硫酸可用作干燥剂,是因为浓硫酸具有吸水性 | |
| D. | 液氧可用于火箭发射,是因为氧气具有可燃性 |
10. 消化药片所含的物质能中和胃里过多的胃酸.某种消化药品的标记如右图所示.医生给某胃酸过多的患者开出服用此药的处方为:每日三次,每次二片.试计算:患者按处方服用该药一天,理论上可中和氢氯酸多少毫克?
消化药片所含的物质能中和胃里过多的胃酸.某种消化药品的标记如右图所示.医生给某胃酸过多的患者开出服用此药的处方为:每日三次,每次二片.试计算:患者按处方服用该药一天,理论上可中和氢氯酸多少毫克?
 消化药片所含的物质能中和胃里过多的胃酸.某种消化药品的标记如右图所示.医生给某胃酸过多的患者开出服用此药的处方为:每日三次,每次二片.试计算:患者按处方服用该药一天,理论上可中和氢氯酸多少毫克?
消化药片所含的物质能中和胃里过多的胃酸.某种消化药品的标记如右图所示.医生给某胃酸过多的患者开出服用此药的处方为:每日三次,每次二片.试计算:患者按处方服用该药一天,理论上可中和氢氯酸多少毫克?
1.某校化学学习小组在学习碳的化学性质的过程中,按如图1进行了木炭与氧化铜在高温加热条件下反应的实验.
【小组实验】
(1)木炭与氧化铜反应的化学方程式是C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
(2)该同学现察到反应的现象一是:澄清石灰水变浑浊.
现象二是:冷却后的试管里的粉末由黑色变成红色.
【提出猜想】
(3)小组某同学对充分反应冷却后的试管里粉末的成分,提出了如下猜想,请将猜想五补充完整.
猜想一:粉末是铜
猜想二:粉末是氧化铜
猜想三:粉末是铜、氧化铜和木炭
猜想四:粉末是铜和木炭
猜想五:粉末是氧化铜、铜
【设计实验、验证猜想】
(4)上述猜想中,明显不合理的是猜想三;
(5)小组同学为了验证猜想一的成立,设计了如图2实验,取样品粉末于钳埚中,通过称取加热前后粉末的质量来进行实验.要证明猜想一成立的依据是红色粉末变成黑色.用相同的实验来证明猜想四可(填“可”或“不可”)行.试说明理由.
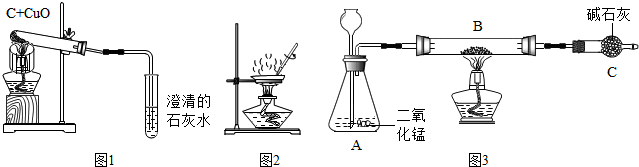
【拓展延伸】
如果猜想四成立,某同学再用如图3所示装置(铁架台等略).取10.0g粉末放入装置B中,通过测出的反应前后装置C的质量來测定粉末中钢的质量分数.
(己知:碱石灰是生石灰(CaO)和氢气化钠固体混合物,是一种干燥剂,它还能吸收二氧化碳气体)
通过计算,粉末中铜的质量分数是88%.
【问题和讨论】
(7)实验完成后,老师评议说:“为了减少实验的误差,上述实验设计还需要做两处改进.”其改进的措施是在B装置前加浓硫酸的干燥装置,在C装置后再加一个碱石灰装置.
【小组实验】
(1)木炭与氧化铜反应的化学方程式是C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
(2)该同学现察到反应的现象一是:澄清石灰水变浑浊.
现象二是:冷却后的试管里的粉末由黑色变成红色.
【提出猜想】
(3)小组某同学对充分反应冷却后的试管里粉末的成分,提出了如下猜想,请将猜想五补充完整.
猜想一:粉末是铜
猜想二:粉末是氧化铜
猜想三:粉末是铜、氧化铜和木炭
猜想四:粉末是铜和木炭
猜想五:粉末是氧化铜、铜
【设计实验、验证猜想】
(4)上述猜想中,明显不合理的是猜想三;
(5)小组同学为了验证猜想一的成立,设计了如图2实验,取样品粉末于钳埚中,通过称取加热前后粉末的质量来进行实验.要证明猜想一成立的依据是红色粉末变成黑色.用相同的实验来证明猜想四可(填“可”或“不可”)行.试说明理由.

【拓展延伸】
如果猜想四成立,某同学再用如图3所示装置(铁架台等略).取10.0g粉末放入装置B中,通过测出的反应前后装置C的质量來测定粉末中钢的质量分数.
| 反应前/g | 反应后/g | |
| 装置C的质量 | 10.0 | 14.4 |
通过计算,粉末中铜的质量分数是88%.
【问题和讨论】
(7)实验完成后,老师评议说:“为了减少实验的误差,上述实验设计还需要做两处改进.”其改进的措施是在B装置前加浓硫酸的干燥装置,在C装置后再加一个碱石灰装置.
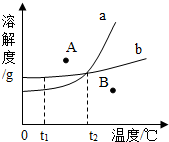 如图是某实验小组的同学绘制的两种固体物质的溶解度曲线图.请你根据图示回答问题:
如图是某实验小组的同学绘制的两种固体物质的溶解度曲线图.请你根据图示回答问题: