题目内容
3.如图是实验室制取气体的常用装置,请根据装置图回答下列问题:
(1)仪器名称①铁架台,②长颈漏斗.
(2)为探究二氧化碳的性质,小雪制取并收集了一瓶二氧化碳气体,她选择的装置是BC(填字母序号),反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,该反应属于的基本反应类型是复分解反应.
分析 铁架台是常用的夹持仪器,长颈漏斗方便加液体药品;制取装置包括加热和不需加热两种,实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.
解答 解:(1)铁架台是常用的夹持仪器,长颈漏斗方便加液体药品,故答案为:铁架台;长颈漏斗;
(2)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热,该反应属于复分解反应;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;故答案为:BC;CaCO3+2HCl=CaCl2+H2O+CO2↑;复分解反应;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和反应类型等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
相关题目
18.质量分数不同的硫酸溶液其密度不相同,对照表如下:
(1)分析表中数据,可以归纳出硫酸溶液的质量分数与密度的关系是质量分数越大密度越大.
(2)质量分数80%和20%的两种硫酸溶液等体积混合后,溶液中溶质的质量分数是56.2%.(结果保留一位小数)
(3)欲配制300克溶质的质量分数为30%的稀硫酸,需要溶质的质量分数为90%的浓硫酸多少克?水多少克?
| 质量分数 | 10% | 20% | 30% | 40% | 50% | 60% | 70% | 80% | 90% | 98% |
| 密度(g/mL) | 1.07 | 1.14 | 1.22 | 1.30 | 1.40 | 1.50 | 1.61 | 1.73 | 1.80 | 1.84 |
(2)质量分数80%和20%的两种硫酸溶液等体积混合后,溶液中溶质的质量分数是56.2%.(结果保留一位小数)
(3)欲配制300克溶质的质量分数为30%的稀硫酸,需要溶质的质量分数为90%的浓硫酸多少克?水多少克?
8.只用试剂水,不能一次性鉴别出来的一组物质是( )
| A. | 固体:氢氧化钠、硝酸铵、氯化钠 | B. | 液体:浓盐酸、植物油、浓硫酸 | ||
| C. | 固体:高锰酸钾、硫酸铜、氯化铁 | D. | 固体:硫酸镁、硝酸钾、氯化钠 |
12.下列有关物质的性质和用途,说法正确的是( )
| A. | 苏打不仅常在做馒头面包中使用,实验室还可以用于检验SO42- | |
| B. | 浓硫酸具有吸水性,常用作食品干燥剂 | |
| C. | 食醋不仅是生活中的调味品,还可用于除水垢 | |
| D. | 氢氧化钠呈碱性,可用于治疗胃酸过多 |

 用如图所示装置分别进行以下实验.
用如图所示装置分别进行以下实验.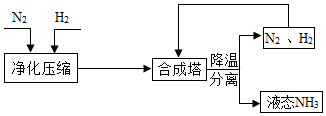 工业上合成 NH 3 的工艺流程可简化为:
工业上合成 NH 3 的工艺流程可简化为: