题目内容
2.下列各组物质分类一致的是( )| A. | HNO3、H2SO4、NaOH | B. | H2CO3、Ca(OH)2、NaCl | ||
| C. | CuSO4、Al2O3、NH3•H2O | D. | CaCO3、MgCl2、AgNO3 |
分析 酸是指电离时生成的阳离子全部是氢离子的化合物,碱是指电离时生成的阴离子全部是氢氧根离子的化合物,盐是指由金属离子和酸根离子构成的化合物,氧化物是指由两种元素组成的且其中一种是氧元素的化合物.
解答 解:A、硝酸、硫酸属于酸,而氢氧化钠属于碱;故不正确;
B、碳酸属于酸;氢氧化钙属于碱;氯化钠属于盐,故错误;
C、硫酸铜属于盐;氧化铝属于氧化物;氨水属于碱;故不正确;
D、碳酸钙、氯化镁和硝酸银都属于盐;故正确.
故选D.
点评 物质的分类知识是初中化学的教学难点,也是考查的热点之一,透彻理解有关概念,明确概念间的含义及相互关系是解题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.如表是元素周期表中部分元素的原子结构示意图,请分析:
(1)在化学反应中Mg原子易失(填“得”或“失”)电子•
(2)Na+离子核外的电子数为10;
(3)经分析发现,元素的周期数与原子的电子层数、元素的主族数与原子的最外层电子数有着密切的关系;请推断X原子的最外层电子数为3,Y原子的电子层数为4;
(4)若镓(Ga)元素与氯元素只组成一种属于盐的化合物,请写出该化合物的化学式GaCl3.
| ⅠA | ⅡA | ⅢA | |
| 第2周期 |  | 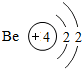 | 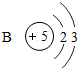 |
| 第3周期 |  |  | X |
| 第4周期 | Y | 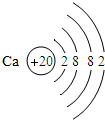 | 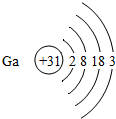 |
(2)Na+离子核外的电子数为10;
(3)经分析发现,元素的周期数与原子的电子层数、元素的主族数与原子的最外层电子数有着密切的关系;请推断X原子的最外层电子数为3,Y原子的电子层数为4;
(4)若镓(Ga)元素与氯元素只组成一种属于盐的化合物,请写出该化合物的化学式GaCl3.
10. 2016年我国继续加大了对光伏(太阳能)发电的资金支持,以转变能源结构,节省能源、减少污染,关于光伏太阳能所用材料的叙述不正确的是( )
2016年我国继续加大了对光伏(太阳能)发电的资金支持,以转变能源结构,节省能源、减少污染,关于光伏太阳能所用材料的叙述不正确的是( )
 2016年我国继续加大了对光伏(太阳能)发电的资金支持,以转变能源结构,节省能源、减少污染,关于光伏太阳能所用材料的叙述不正确的是( )
2016年我国继续加大了对光伏(太阳能)发电的资金支持,以转变能源结构,节省能源、减少污染,关于光伏太阳能所用材料的叙述不正确的是( )| A. | 铝合金支架属于金属材料 | |
| B. | 过程中太阳能转化成电能 | |
| C. | 硅电池板中的硅元素是地壳中含量最多的金属元素 | |
| D. | 电线塑料外壳属于有机合成高分子材料 |
14.物质的性质决定其用途.下列物质的用途与性质对应关系错误的是( )
| A. | 氢氧化钙可用来改良酸性土壤--氢氧化钙溶液呈碱性 | |
| B. | 铁粉能做食品包装中的“双吸剂”--铁在常温下能与水和氧气共同反应 | |
| C. | 固体二氧化碳可用人工降雨--二氧化碳能与水反应 | |
| D. | 氧化钙可做食品干燥剂--氧化钙能与水反应 |
11. 分析图判断关于氧元素的相关信息正确的是( )
分析图判断关于氧元素的相关信息正确的是( )
 分析图判断关于氧元素的相关信息正确的是( )
分析图判断关于氧元素的相关信息正确的是( )| A. | 氧原子的质量为16.00g | B. | 氧原子的结构示意图为 | ||
| C. | 氧为金属元素 | D. | 氧原子的质子数为8 |
12.某学校化学兴趣小组为了测定实验中高锰酸钾样品的纯度,取10g该样品进行了加热,加热的时间与剩余固体的质量关系如表所示(假设杂质不参加反应,数值看作为理论值).
(1)加热t4时间后,高锰酸钾是否已经完全反应是(填“是”或“否”).
(2)求该样品中高锰酸钾的质量分数(即纯度)(可能用到的相对原子质量:O-16,K-39,Mn-55).
| 加热时间 | t1 | t2 | t3 | t4 |
| 剩余固体质量(g) | 9.56 | 9.28 | 9.04 | 9.04 |
(2)求该样品中高锰酸钾的质量分数(即纯度)(可能用到的相对原子质量:O-16,K-39,Mn-55).

 几种常见物质之间的相互转化关系如图所示(各字母代表一种物质,部分反应物、生成物及反应条件略去),已知:①五种物质均含铜元素,且化合物中铜元素的化合价均为+2;②A为单质,在空气中加热后生成黑色物质B;③X溶液与铁反应可得到A;④X溶液与氯化钡溶液反应可得到D,同时有白色沉淀产生;⑤D溶液中加入少量的氢氧化钠溶液得到E,结合信息推断:
几种常见物质之间的相互转化关系如图所示(各字母代表一种物质,部分反应物、生成物及反应条件略去),已知:①五种物质均含铜元素,且化合物中铜元素的化合价均为+2;②A为单质,在空气中加热后生成黑色物质B;③X溶液与铁反应可得到A;④X溶液与氯化钡溶液反应可得到D,同时有白色沉淀产生;⑤D溶液中加入少量的氢氧化钠溶液得到E,结合信息推断: