题目内容
14.物质的性质决定其用途.下列物质的用途与性质对应关系错误的是( )| A. | 氢氧化钙可用来改良酸性土壤--氢氧化钙溶液呈碱性 | |
| B. | 铁粉能做食品包装中的“双吸剂”--铁在常温下能与水和氧气共同反应 | |
| C. | 固体二氧化碳可用人工降雨--二氧化碳能与水反应 | |
| D. | 氧化钙可做食品干燥剂--氧化钙能与水反应 |
分析 A、根据氢氧化钙的性质与用途进行分析判断.
B、根据铁生锈的条件进行分析判断.
C、干冰是固体的二氧化碳,升华时吸收大量的热.
D、氧化钙能与水反应生成氢氧化钙,据此进行分析判断.
解答 解:
A、氢氧化钙溶液呈碱性,能中和酸性土壤,可用来改良酸性土壤,故选项说法正确.
B、铁在常温下能与水和氧气共同反应,故铁粉能做食品包装中的“双吸剂”,故选项说法正确.
C、干冰是固体的二氧化碳,升华时吸收大量的热,可用于人工降雨,故选项说法错误.
D、氧化钙能与水反应生成氢氧化钙,可做食品干燥剂,故选项说法正确.
答案:C.
点评 本题难度不大,是化学常考的题型,物质的性质决定物质的用途,掌握常见化学物质的性质和用途是正确解答此类题的关键.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
5.如图是某反应前后的微观示意图,关于该示意图表示的化学变化的说法正确的是( )
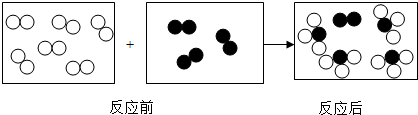

| A. | 该反应是分解反应 | |
| B. | 参加反应的“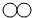 ”和“ ”和“ ”分子的个数比是2:1 ”分子的个数比是2:1 | |
| C. | 反应前后原子的种类和数目没变 | |
| D. | 反应前后元素的化合价没有发生改变 |
2.下列各组物质分类一致的是( )
| A. | HNO3、H2SO4、NaOH | B. | H2CO3、Ca(OH)2、NaCl | ||
| C. | CuSO4、Al2O3、NH3•H2O | D. | CaCO3、MgCl2、AgNO3 |
9.下列有关原子的说法正确的是( )
| A. | 原子能构成分子,但不能直接构成物质 | |
| B. | 原子中一定含有质子、中子、电子三种粒子 | |
| C. | 不同种原子的本质区别是中子数不同 | |
| D. | 原子在化学变化中不能再分,只能重新组合 |
19.某课外兴趣小组的同学设计了如下三个实验来验证质量守恒定律: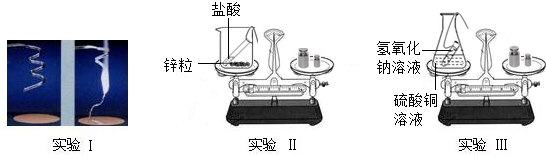
实验Ⅰ:称量镁条,在空气中点燃,待反应结束后,将生成物全部收回再称量.
实验Ⅱ:将装有稀盐酸的小试管放入装有锌粒的烧杯中,称量,然后将盐酸与锌粒接触,过一会在称量.
实验Ⅲ:将装有氢氧化钠溶液的试管放入盛有硫酸铜的锥形瓶中,并在锥型瓶口塞上橡皮塞,称量,然后设法将两种溶液接触(有蓝色氢氧化铜沉淀和硫酸钠生成)过一会再称量.数据如表:
(1)在实验Ⅰ中,反应后的质量比反应前明显增加,请用质量守恒定律加以解释根据质量守恒定律,参加反应的镁带和氧气的质量总和,等于反应后生成的氧化镁的质量,由于空气中的氧气参与了反应,因此,生成氧化镁的质量比原来镁带的质量增加了;
(2)这三个实验中,实验Ⅲ正确反映了反应物与生成物之间的质量关系.请从分子、原子的角度解释反应前后质量相等的原因化学反应前后原子的种类、数目和质量没有发生改变;
(3)实验Ⅰ、Ⅱ不能正确反映反应物和生成物之间的质量关系,选一例说明实验设计中的不当之处,并提出改进思路实验I应将镁条放在密闭的金属容器中引燃,再称量.

实验Ⅰ:称量镁条,在空气中点燃,待反应结束后,将生成物全部收回再称量.
实验Ⅱ:将装有稀盐酸的小试管放入装有锌粒的烧杯中,称量,然后将盐酸与锌粒接触,过一会在称量.
实验Ⅲ:将装有氢氧化钠溶液的试管放入盛有硫酸铜的锥形瓶中,并在锥型瓶口塞上橡皮塞,称量,然后设法将两种溶液接触(有蓝色氢氧化铜沉淀和硫酸钠生成)过一会再称量.数据如表:
| 编号 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
| 反应前/g | 4.8 | 112.6 | 118.4 |
| 反应后/g | 8.0 | 112.4 | 118.4 |
(2)这三个实验中,实验Ⅲ正确反映了反应物与生成物之间的质量关系.请从分子、原子的角度解释反应前后质量相等的原因化学反应前后原子的种类、数目和质量没有发生改变;
(3)实验Ⅰ、Ⅱ不能正确反映反应物和生成物之间的质量关系,选一例说明实验设计中的不当之处,并提出改进思路实验I应将镁条放在密闭的金属容器中引燃,再称量.
3.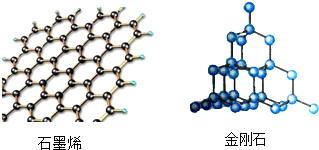 碳及其化合物广泛在于自然界中,如图是石墨烯和金刚石两种碳单质的结构模型(图中每一个球代表一个碳原子),下列有关说法正确的是( )
碳及其化合物广泛在于自然界中,如图是石墨烯和金刚石两种碳单质的结构模型(图中每一个球代表一个碳原子),下列有关说法正确的是( )
 碳及其化合物广泛在于自然界中,如图是石墨烯和金刚石两种碳单质的结构模型(图中每一个球代表一个碳原子),下列有关说法正确的是( )
碳及其化合物广泛在于自然界中,如图是石墨烯和金刚石两种碳单质的结构模型(图中每一个球代表一个碳原子),下列有关说法正确的是( )| A. | 石墨烯和金刚石中的碳原子间都存在间隔 | |
| B. | 石墨烯和金刚石中的碳原子静止不动 | |
| C. | 石墨烯或金刚石在空气中燃烧只能生成一种碳的氧化物 | |
| D. | 常温下,石墨烯和金刚石的化学性质都比较活泼 |