题目内容
10. 2016年我国继续加大了对光伏(太阳能)发电的资金支持,以转变能源结构,节省能源、减少污染,关于光伏太阳能所用材料的叙述不正确的是( )
2016年我国继续加大了对光伏(太阳能)发电的资金支持,以转变能源结构,节省能源、减少污染,关于光伏太阳能所用材料的叙述不正确的是( )| A. | 铝合金支架属于金属材料 | |
| B. | 过程中太阳能转化成电能 | |
| C. | 硅电池板中的硅元素是地壳中含量最多的金属元素 | |
| D. | 电线塑料外壳属于有机合成高分子材料 |
分析 A、根据金属材料包括纯金属以及它们的合金,据此行分析判断即可.
B、根据氮气化学性质不活泼进行分析判断.
C、根据太阳能发电的能量转化进行分析判断.
D、根据常见材料的分类进行分析判断.
解答 解:A、铝合金支架是用铝合金制成的,属于金属材料,故选项说法正确.
B、太阳能发电是将太阳能转化为电能,故选项说法正确.
C、地壳含量较多的元素(前四种)按含量从高到低的排序为:氧、硅、铝、铁,其中含量最多的金属元素是铝元素,硅属于非金属元素,故选项说法错误.
D、有机合成材料必须具备三个特征:人工合成、有机物、高分子,透明的塑料灯罩是用塑料制成的,属于有机合成高分子材料,故选项说法正确.
故选C.
点评 化学来源于生产生活,也必须服务于生产生活,所以与人类生产生活相关的化学知识也是重要的中考热点之一.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案
相关题目
5.如图是某反应前后的微观示意图,关于该示意图表示的化学变化的说法正确的是( )
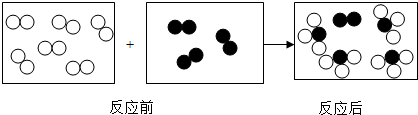

| A. | 该反应是分解反应 | |
| B. | 参加反应的“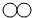 ”和“ ”和“ ”分子的个数比是2:1 ”分子的个数比是2:1 | |
| C. | 反应前后原子的种类和数目没变 | |
| D. | 反应前后元素的化合价没有发生改变 |
2.下列各组物质分类一致的是( )
| A. | HNO3、H2SO4、NaOH | B. | H2CO3、Ca(OH)2、NaCl | ||
| C. | CuSO4、Al2O3、NH3•H2O | D. | CaCO3、MgCl2、AgNO3 |
19.某课外兴趣小组的同学设计了如下三个实验来验证质量守恒定律: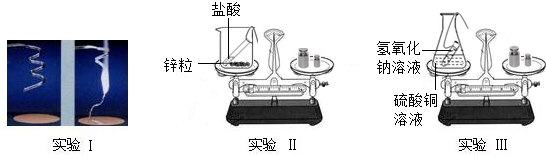
实验Ⅰ:称量镁条,在空气中点燃,待反应结束后,将生成物全部收回再称量.
实验Ⅱ:将装有稀盐酸的小试管放入装有锌粒的烧杯中,称量,然后将盐酸与锌粒接触,过一会在称量.
实验Ⅲ:将装有氢氧化钠溶液的试管放入盛有硫酸铜的锥形瓶中,并在锥型瓶口塞上橡皮塞,称量,然后设法将两种溶液接触(有蓝色氢氧化铜沉淀和硫酸钠生成)过一会再称量.数据如表:
(1)在实验Ⅰ中,反应后的质量比反应前明显增加,请用质量守恒定律加以解释根据质量守恒定律,参加反应的镁带和氧气的质量总和,等于反应后生成的氧化镁的质量,由于空气中的氧气参与了反应,因此,生成氧化镁的质量比原来镁带的质量增加了;
(2)这三个实验中,实验Ⅲ正确反映了反应物与生成物之间的质量关系.请从分子、原子的角度解释反应前后质量相等的原因化学反应前后原子的种类、数目和质量没有发生改变;
(3)实验Ⅰ、Ⅱ不能正确反映反应物和生成物之间的质量关系,选一例说明实验设计中的不当之处,并提出改进思路实验I应将镁条放在密闭的金属容器中引燃,再称量.

实验Ⅰ:称量镁条,在空气中点燃,待反应结束后,将生成物全部收回再称量.
实验Ⅱ:将装有稀盐酸的小试管放入装有锌粒的烧杯中,称量,然后将盐酸与锌粒接触,过一会在称量.
实验Ⅲ:将装有氢氧化钠溶液的试管放入盛有硫酸铜的锥形瓶中,并在锥型瓶口塞上橡皮塞,称量,然后设法将两种溶液接触(有蓝色氢氧化铜沉淀和硫酸钠生成)过一会再称量.数据如表:
| 编号 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
| 反应前/g | 4.8 | 112.6 | 118.4 |
| 反应后/g | 8.0 | 112.4 | 118.4 |
(2)这三个实验中,实验Ⅲ正确反映了反应物与生成物之间的质量关系.请从分子、原子的角度解释反应前后质量相等的原因化学反应前后原子的种类、数目和质量没有发生改变;
(3)实验Ⅰ、Ⅱ不能正确反映反应物和生成物之间的质量关系,选一例说明实验设计中的不当之处,并提出改进思路实验I应将镁条放在密闭的金属容器中引燃,再称量.
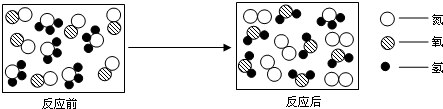
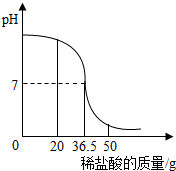 某小组同学利用“酸碱中和反应”的实验原理测定一标签破损的氢氧化钠溶液的溶质质量分数.先取40g氢氧化钠溶液于烧杯中,将10%的稀盐酸逐滴加入到样品中,边加边搅拌.利用接在传感上的计算机绘制出了如图所示的pH随所加的稀盐酸质量变化的曲线.
某小组同学利用“酸碱中和反应”的实验原理测定一标签破损的氢氧化钠溶液的溶质质量分数.先取40g氢氧化钠溶液于烧杯中,将10%的稀盐酸逐滴加入到样品中,边加边搅拌.利用接在传感上的计算机绘制出了如图所示的pH随所加的稀盐酸质量变化的曲线.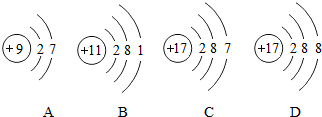 根据下列微粒的结构示意图填空:
根据下列微粒的结构示意图填空: