题目内容
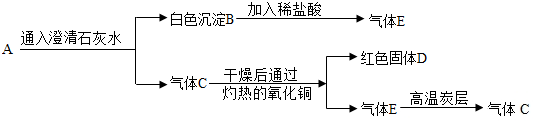
16.A与B有如下的反应:A+B→C+D(1)若C为厨房内常用的调味品;在A溶液中加入铁粉能产生氢气,则A是盐酸
若A、B两溶液恰好反应完全,则反应后溶液的pH=7(填“<”、“>”或“=”);写出A、B两溶液反应的化学方程式HCl+NaOH═NaCl+H2O.
(2)若B常用来改良酸性土壤;D是重要的化工原料且与B的类别相同;B与CO2反应也能生成C;则A为Na2CO3,C的用途是建筑材料(合理即可)(只要写一种).写出B溶液与CO2反应的化学方程式CO2+Ca(OH)2=CaCO3↓+H2O.
(3)若A为单质,A与B在高温下反应,可观察到固体粉末由黑色变为红色,则B是氧化铜,反应的化学方程式是C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
分析 (1)若C为厨房内常用的调味品,则C为氯化钠;在A溶液中加入铁粉能产生氢气,结合铁能与酸反应生成氢气,则A为酸;A与B反应生成氯化钠和D,则A为稀盐酸,稀盐酸能与氢氧化钠溶液反应生成氯化钠和水,进行分析解答;
(2))B常用来改良酸性土壤,则B是氢氧化钙,D是重要的化工原料且与B的类别相同,则D是氢氧化钠,B与CO2反应也能生成C,故C是碳酸钙,A是碳酸钠,据此进行分析解答;
(3)A为单质,A与B在高温下反应,可观察到固体粉末由黑色变为红色,因此可以是碳还原氧化铜的反应,据此分析.
解答 解:(1)若C为厨房内常用的调味品,在A溶液中加入铁粉能产生氢气,则A是酸,酸能与B反应生成厨房内的调味品,故C是氯化钠,A是盐酸,B是氢氧化钠,二者反应的方程式为:HCl+NaOH═NaCl+H2O;酸碱恰好反应,溶液为中性,因此pH=7;故填:稀盐酸;=;HCl+NaOH═NaCl+H2O;
(2)B常用来改良酸性土壤,则B是氢氧化钙,D是重要的化工原料且与B的类别相同,则D是氢氧化钠,B与CO2反应也能生成C,故C是碳酸钙,A是碳酸钠,碳酸钙可以用于建筑材料等;故填:Na2CO3,建筑材料(合理即可);CO2+Ca(OH)2=CaCO3↓+H2O;
(3)A为单质,A与B在高温下反应,可观察到固体粉末由黑色变为红色,因此可以是碳还原氧化铜的反应产生铜和二氧化碳,则B是氧化铜;故填:CuO; C+2CuO $\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑;
点评 本题考查的是常见的物质的推断,完成此题,可以依据已有的物质的性质进行分析.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目
11.关于水的组成说法中正确的是( )
| A. | 水是水元素组成 | B. | 水的组成复杂,没有明确的答案 | ||
| C. | 水是由氢气和氧气组成 | D. | 水是由氢元素和氧元素组成 |
6.“蜡烛及其燃烧”的探究
(1)探究内容名称:“蜡烛及其燃烧”的探究.
(2)探究用品:蜡烛,火柴,2个烧杯(洁净干燥),澄清石灰水.
(3)、探究的目的:蜡烛的物理特性,燃烧的条件,燃烧后有何生成物.
(4)探究步骤.
(5)通过该实验知道了蜡烛的燃烧产物,请写出蜡烛燃烧的文字表达式:石蜡+氧气$\stackrel{点燃}{→}$水+二氧化碳
(6)通过探究;谈谈对学习化学的感受:化学能够为我们展现化学反应的现象、本质,能够指导我们的生活和生产.
(1)探究内容名称:“蜡烛及其燃烧”的探究.
(2)探究用品:蜡烛,火柴,2个烧杯(洁净干燥),澄清石灰水.
(3)、探究的目的:蜡烛的物理特性,燃烧的条件,燃烧后有何生成物.
(4)探究步骤.
| 步 骤 | 对现象观察及描述 | 分析现象成因(可以是假想、推理) | |
| 点燃前 | |||
| 燃着时 | 火焰上方罩一个烧杯 | ||
| 火焰上方罩内壁涂有 石灰水的烧杯 | |||
| 用烧杯完全罩住蜡烛 | |||
| 熄灭后 | |||
(6)通过探究;谈谈对学习化学的感受:化学能够为我们展现化学反应的现象、本质,能够指导我们的生活和生产.


 某兴趣小组对生锈废铁锅中铁的含量进行了测定.生锈的铁锅中除Fe、Fe2O3外,还含有碳、硅、锰等元素(除Fe、Fe2O3以外的物质都不与稀硫酸反应).兴趣小组的同学称取33g废铁锅片放入特制容器中,缓慢加入39.2%的稀硫酸,直到反应完全(假设硫酸先与表面的铁锈发生反应),实验数据如图所示.
某兴趣小组对生锈废铁锅中铁的含量进行了测定.生锈的铁锅中除Fe、Fe2O3外,还含有碳、硅、锰等元素(除Fe、Fe2O3以外的物质都不与稀硫酸反应).兴趣小组的同学称取33g废铁锅片放入特制容器中,缓慢加入39.2%的稀硫酸,直到反应完全(假设硫酸先与表面的铁锈发生反应),实验数据如图所示.