题目内容
11.在一次化学实验中,同学们将饱和硫酸铜溶液逐滴加到5mL饱和氢氧化钠溶液中,观察到以下异常实验现象:| 实验序号 | 滴加CuSO4溶液的量 | 实验现象 |
| ① | 第1~6滴 | 有蓝色沉淀,但振荡后沉淀消失,形成亮蓝色溶液 |
| ② | 第7~9滴 | 产生蓝色沉淀,且沉淀逐渐增多,振荡后沉淀不消失,很快沉淀逐渐变黑色 |
实验①中蓝色沉淀为什么消失?同学们继续进行如下探究.
【查阅资料】
Ⅰ.氢氧化铜在温度70℃-80℃时可分解生成氧化铜;
Ⅱ.四羟基合铜酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色.
【猜想与讨论】小陶认为蓝色沉淀消失可能是氢氧化铜发生了分解.其他同学一致否定了他的猜测,理由是如分解则会生成氧化铜是黑色固体,而蓝色沉淀消失后是形成亮蓝色溶液.
同学们交流讨论后,提出以下两种猜想.
猜想一:少许氢氧化铜可溶于足量水中.
猜想二:氢氧化铜可在足量氢氧化钠浓溶液中溶解,溶液呈亮蓝色.
【实验探究】同学们用氢氧化铜粉末(其它试剂可任选)设计如下实验.请填写表中空格.
| 实验序号 | 实验方法与操作 | 实验现象 | 结论 |
| ③ | 将少许Cu(OH)2粉末加到5mL蒸馏水中,充分振荡 | 沉淀不溶解,液体仍为无色 | 猜想一错误 |
| ④ | 将少许Cu(OH)2粉末加入到足量氢氧化钠浓溶液中,充分振荡,固体溶解 | 溶液呈亮蓝色 | 猜想二正确 |
(1)根据实验可知饱和硫酸铜溶液与饱和氢氧化钠溶液的反应是放热反应依据的实验现象是蓝色沉淀逐渐变为黑色.
(2)写出氢氧化铜受热分解生成黑色固体的化学方程式Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O;
【实践与运用】将8.0g氢氧化钠完全溶于水形成溶液,向其中加入一定质量的硫酸铜溶液,恰好完全反应,所得混合物总质量为109.8g.计算:
(1)反应产生沉淀的质量.(写出计算过程)
(2)反应后所得溶液的溶质质量分数.(写出计算过程,结果精确到0.1%)
分析 根据硫酸铜和氢氧化钠反应产生氢氧化铜蓝色沉淀和硫酸钠,写出反应的方程式;
【猜想与讨论】根据实验①的现象是沉淀消失,形成亮蓝色溶液,而不是产生黑色固体分析;
【实验探究】③根据实验的目的否定猜想一分析实验现象;
④根据实验目的是验证猜想二成立设计实验并描述实验现象;
【结论与反思】(1)根据现象及资料信息分析能量变化.
(2)根据给蓝色的氢氧化铜加热生成物分析解答.
【拓展与运用】根据氢氧化钠的质量利用反应的化学方程式求出生成沉淀的质量和硫酸钠的质量.
解答 解:硫酸铜和氢氧化钠反应产生氢氧化铜蓝色沉淀和硫酸钠,故反应的方程式为:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
【猜想与讨论】根据实验①的现象是沉淀消失,形成亮蓝色溶液,而不是产生黑色固体,因此小陶认为蓝色沉淀消失可能是Cu(OH)2发生了分解是错误的;
【实验探究】③实验的目的否定猜想一,因此加水沉淀不溶解;
④实验目的是验证猜想二成立,即是氢氧化铜溶于氢氧化钠溶液产生的亮蓝色的溶液;
故答案为:
| 实验序号 | 实验方法与操作 | 实验现象 | 结论 |
| ③ | 将少许Cu(OH)2粉末加到5mL蒸馏水中,充分振荡 | 沉淀不溶解,液体仍为无色 | 猜想一错误 |
| ④ | 将少许Cu(OH)2粉末加入到足量氢氧化钠浓溶液中,充分振荡,固体溶解 | 溶液呈亮蓝色 | 猜想二正确 |
(1)根据表格1可知随着氢氧化钠溶液的滴加,观察到产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变黑色,结合资料Ⅰ.Cu(OH)2在室温下稳定,70℃-80℃时可脱水分解生成CuO,因此说明饱和CuSO4溶液与饱和NaOH溶液的反应是放热反应;
(2)根据氢氧化铜不稳定,在加热的情况下易分解,生成一种黑色固体和水,则推测该反应产物为氧化铜和水,则其化学方程式是Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O
【拓展与运用】
设反应产生沉淀的质量为x,反应后所得溶液的溶质质量为Y.
2NaOH+CuSO4═Cu(OH)2↓+Na2 SO4
80 98 142
8g x y
$\frac{80}{8g}=\frac{98}{x}=\frac{142}{y}$
x=9.8g y=14.2g
反应后所得溶液的溶质质量分数为:为:$\frac{14.2g}{109.8g-9.8g}$×100%=14.2%.
答案:
【猜想与讨论】如分解则会生成氧化铜是黑色固体,而蓝色沉淀消失后是形成亮蓝色溶液;
【实验探究】
| 实验序号 | 实验方法与操作 | 实验现象 | 结论 |
| ③ | 将少许Cu(OH)2粉末加到5mL蒸馏水中,充分振荡 | 沉淀不溶解,液体仍为无色 | 猜想一错误 |
| ④ | 将少许Cu(OH)2粉末加入到足量氢氧化钠浓溶液中,充分振荡,固体溶解 | 溶液呈亮蓝色 | 猜想二正确 |
【拓展与运用】
反应产生沉淀的质量是9.8g.反应后所得溶液的溶质质量分数为14.2%.
点评 本题属于信息题的考查,解题的依据是题目的信息结合已有的相关知识进行分析,能够考查学生的知识迁移能力.

练习册系列答案
相关题目
10.下列选项中物质的俗名、化学式、类别、用途完全对应的是( )
| A. | 纯碱 Na2CO3 碱 制玻璃 | B. | 生石灰 CaO 氧化物 补钙剂 | ||
| C. | 食盐 NaCl 盐 除铁锈 | D. | 火碱 NaOH 碱 生产橡胶 |
3.向一定质量的AgNO3和Cu(NO3)2的混合溶液中加入ngZn,充分反映后过滤,将滤渣洗涤、干燥后再称量,得到的质量为ng,据此,下列说法正确的是( )
| A. | 滤渣中的物质至少有两种 | |
| B. | 取反应后的滤液滴加稀盐酸,有白色沉淀产生 | |
| C. | 取滤渣滴加稀硫酸,一定有气泡产生 | |
| D. | 取反应后的滤液观察,滤液不可能呈蓝色 |
1.化学与我们的生活息息相关,下列说法不正确的是( )
| A. | 减少燃煤发电,增加太阳能发电,有利于治理雾霾 | |
| B. | 小苏打可用于治疗胃酸过多 | |
| C. | 人体缺锌会引起生长发育缓慢,因此锌元素摄入的越多越好 | |
| D. | 垃圾中的有些金属、塑料可以循环利用,因此生活垃圾要分类回收 |
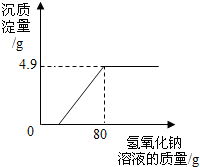 某校化学兴趣小组在参加社会实践活动时,环保组监测到一湿法冶铜厂排放的废水中含有硫酸和硫酸铜两种污染物,为测定该废水中各污染物的含量,给冶铜厂提供处理废水的参考,环保组的同学进行了以下实验:取废水300g,向其中加入溶质质量分数为20%的氢氧化钠溶液,测得沉淀质量与所加入的氢氧化钠溶液的质量关系如图,请分析计算:
某校化学兴趣小组在参加社会实践活动时,环保组监测到一湿法冶铜厂排放的废水中含有硫酸和硫酸铜两种污染物,为测定该废水中各污染物的含量,给冶铜厂提供处理废水的参考,环保组的同学进行了以下实验:取废水300g,向其中加入溶质质量分数为20%的氢氧化钠溶液,测得沉淀质量与所加入的氢氧化钠溶液的质量关系如图,请分析计算: