题目内容
20.食盐水中含有杂质CaCl2和Na2SO4,依次加入过量BaCl2和Na2CO3,溶液后过滤,滤液中溶质为:NaCl、Na2CO3.溶解、过滤和蒸发都要用到一种玻璃仪器,该仪器在溶解时的作用是搅拌,以加速溶解.向饱和食盐水中先后通入足量NH3和CO2,生成小苏打(在该溶液中难溶)和一种氮肥,写出该反应的化学方程式CO2+H2O+NH3+NaCl=NaHCO3↓+NH4Cl.分析 根据氯化钡和碳酸钠反应生成碳酸钡沉淀和氯化钠,氯化钡和硫酸钠反应生成硫酸钡沉淀和氯化钠,溶解、过滤和蒸发都要用到一种玻璃仪器是玻璃棒,二氧化碳、水、氨气和氯化钠反应生成碳酸氢钠和氯化铵进行分析.
解答 解:氯化钡和碳酸钠反应生成碳酸钡沉淀和氯化钠,氯化钡和硫酸钠反应生成硫酸钡沉淀和氯化钠,所以依次加入过量BaCl2和Na2CO3,加入的碳酸钠是过量的,所以充分反应后过滤,滤液中溶质为:NaCl、Na2CO3,溶解、过滤和蒸发都要用到一种玻璃仪器是玻璃棒,玻璃棒在溶解过程中的作用是:搅拌,以加速溶解,二氧化碳、水、氨气和氯化钠反应生成碳酸氢钠和氯化铵,化学方程式为:CO2+H2O+NH3+NaCl=NaHCO3↓+NH4Cl.
故答案为:NaCl、Na2CO3;搅拌,以加速溶解;CO2+H2O+NH3+NaCl=NaHCO3↓+NH4Cl.
点评 本题主要考查了物质的除杂和化学方程式的书写,难度不大,注意除去杂质不能引入新的杂质进行分析.

练习册系列答案
相关题目
18.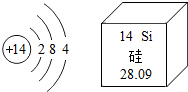 硅的原子结构示意图及在元素周期表的信息如图,下列说法错误的是( )
硅的原子结构示意图及在元素周期表的信息如图,下列说法错误的是( )
 硅的原子结构示意图及在元素周期表的信息如图,下列说法错误的是( )
硅的原子结构示意图及在元素周期表的信息如图,下列说法错误的是( )| A. | 硅属于非金属元素 | B. | 硅原子核内有14个质子 | ||
| C. | 硅原子核外有3个电子层 | D. | 硅的相对原子质量是28.09g |
11.在一次化学实验中,同学们将饱和硫酸铜溶液逐滴加到5mL饱和氢氧化钠溶液中,观察到以下异常实验现象:
在实验①中同学们根据所学初中化学知识判断蓝色沉淀是氢氧化铜.
实验①中蓝色沉淀为什么消失?同学们继续进行如下探究.
【查阅资料】
Ⅰ.氢氧化铜在温度70℃-80℃时可分解生成氧化铜;
Ⅱ.四羟基合铜酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色.
【猜想与讨论】小陶认为蓝色沉淀消失可能是氢氧化铜发生了分解.其他同学一致否定了他的猜测,理由是如分解则会生成氧化铜是黑色固体,而蓝色沉淀消失后是形成亮蓝色溶液.
同学们交流讨论后,提出以下两种猜想.
猜想一:少许氢氧化铜可溶于足量水中.
猜想二:氢氧化铜可在足量氢氧化钠浓溶液中溶解,溶液呈亮蓝色.
【实验探究】同学们用氢氧化铜粉末(其它试剂可任选)设计如下实验.请填写表中空格.
【结论与反思】
(1)根据实验可知饱和硫酸铜溶液与饱和氢氧化钠溶液的反应是放热反应依据的实验现象是蓝色沉淀逐渐变为黑色.
(2)写出氢氧化铜受热分解生成黑色固体的化学方程式Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O;
【实践与运用】将8.0g氢氧化钠完全溶于水形成溶液,向其中加入一定质量的硫酸铜溶液,恰好完全反应,所得混合物总质量为109.8g.计算:
(1)反应产生沉淀的质量.(写出计算过程)
(2)反应后所得溶液的溶质质量分数.(写出计算过程,结果精确到0.1%)
| 实验序号 | 滴加CuSO4溶液的量 | 实验现象 |
| ① | 第1~6滴 | 有蓝色沉淀,但振荡后沉淀消失,形成亮蓝色溶液 |
| ② | 第7~9滴 | 产生蓝色沉淀,且沉淀逐渐增多,振荡后沉淀不消失,很快沉淀逐渐变黑色 |
实验①中蓝色沉淀为什么消失?同学们继续进行如下探究.
【查阅资料】
Ⅰ.氢氧化铜在温度70℃-80℃时可分解生成氧化铜;
Ⅱ.四羟基合铜酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色.
【猜想与讨论】小陶认为蓝色沉淀消失可能是氢氧化铜发生了分解.其他同学一致否定了他的猜测,理由是如分解则会生成氧化铜是黑色固体,而蓝色沉淀消失后是形成亮蓝色溶液.
同学们交流讨论后,提出以下两种猜想.
猜想一:少许氢氧化铜可溶于足量水中.
猜想二:氢氧化铜可在足量氢氧化钠浓溶液中溶解,溶液呈亮蓝色.
【实验探究】同学们用氢氧化铜粉末(其它试剂可任选)设计如下实验.请填写表中空格.
| 实验序号 | 实验方法与操作 | 实验现象 | 结论 |
| ③ | 将少许Cu(OH)2粉末加到5mL蒸馏水中,充分振荡 | 沉淀不溶解,液体仍为无色 | 猜想一错误 |
| ④ | 将少许Cu(OH)2粉末加入到足量氢氧化钠浓溶液中,充分振荡,固体溶解 | 溶液呈亮蓝色 | 猜想二正确 |
(1)根据实验可知饱和硫酸铜溶液与饱和氢氧化钠溶液的反应是放热反应依据的实验现象是蓝色沉淀逐渐变为黑色.
(2)写出氢氧化铜受热分解生成黑色固体的化学方程式Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O;
【实践与运用】将8.0g氢氧化钠完全溶于水形成溶液,向其中加入一定质量的硫酸铜溶液,恰好完全反应,所得混合物总质量为109.8g.计算:
(1)反应产生沉淀的质量.(写出计算过程)
(2)反应后所得溶液的溶质质量分数.(写出计算过程,结果精确到0.1%)
12.下列我国古代的技术应用不涉及化学变化的是( )
| A. |  粮食酿酒 | B. |  棉纱织布 | C. |  火药应用 | D. |  瓷器烧制 |
9.下列生活用品所使用的主要材料属于有机合成材料的是( )
| A. | 真丝围巾 | B. | 陶瓷餐具 | C. | 塑料保鲜膜 | D. | 红木家具 |
10.下列物质露置于空气中,因发生化学变化而使其质量增加的是( )
| A. | 浓硫酸 | B. | 烧碱溶液 | C. | 浓盐酸 | D. | 过氧化氢溶液 |
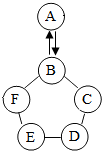 A~F是初中化学常见的物质,如图所示是A~F相互间的关系(“→”表示物质间存在的转化关系,“-”表示两端的物质能发生化学反应).通常情况下A是能参与绿色植物光合作用的气体;B在工业上广泛用于玻璃、造纸、纺织和洗涤剂生产等领域;D的溶液呈蓝色;E是地壳中含量最多金属元素的单质.
A~F是初中化学常见的物质,如图所示是A~F相互间的关系(“→”表示物质间存在的转化关系,“-”表示两端的物质能发生化学反应).通常情况下A是能参与绿色植物光合作用的气体;B在工业上广泛用于玻璃、造纸、纺织和洗涤剂生产等领域;D的溶液呈蓝色;E是地壳中含量最多金属元素的单质. 水是生命之源,人类的生产、生活离不开水.
水是生命之源,人类的生产、生活离不开水.