题目内容
2.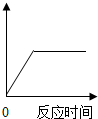 在实验室加热氯酸钾和二氧化锰的混合物制取氧气.若如图中横坐标表示反应时间,纵坐标表示的是( )
在实验室加热氯酸钾和二氧化锰的混合物制取氧气.若如图中横坐标表示反应时间,纵坐标表示的是( )| A. | 氯酸钾的质量 | B. | 钾元素的质量 | C. | 二氧化锰的质量 | D. | 生成氧气的质量 |
分析 氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,据此结合氯酸钾、二氧化锰、氧气的质量变化进行分析判断即可.
解答 解:A、氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,反应后由于氧气逸出,固体物质的质量减少,完全反应后剩余固体的质量不再改变,图象应该是先下降后成一条水平直线,故选项错误.
B、氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,反应前后钾元素的质量不变,故选项错误.
C、此反应中,二氧化锰作催化剂,反应前后质量不变,图象应是成一条水平直线,故选项错误.
D、氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,反应后氧气的质量增加,完全反应后氧气的质量不再改变,图象应该是先上升后成一条水平直线.故选项正确.
答案:D
点评 本题是一道图象坐标与化学知识相结合的综合题,解题的关键是结合所涉及的化学知识,正确分析各变化的过程,注意分析坐标轴表示的意义、曲线的起点、折点及变化趋势,进而确定正确的图象.

练习册系列答案
相关题目
12.下列应用的原理用化学方程式表示正确的是( )
| A. | 用赤铁矿冶炼生铁 Fe2O3+3CO═2Fe+3CO2 | |
| B. | 用氢氧化钠溶液吸收二氧化硫 S02+2NaOH═Na2S03+H20 | |
| C. | 用小苏打治疗胃酸过多 Na2C03+2HCl=2NaCl+H20+C02↑ | |
| D. | 用高锰酸钾制取氧气 2KMnO4═K2MnO4+MnO2+O2↑ |
10.利用分子知识对下列现象的解释合理的是( )
| A. | 气体更易被压缩--构成气体的分子具有弹性 | |
| B. | 液氧为淡蓝色--氧气分子是蓝色的 | |
| C. | 湿衣服变干--水分子在不断地运动 | |
| D. | 碘受热升华--碘分子变大了 |
17.如图是某个化学反应前后的微观模拟图,通过对该图的分析,下列说法正确的是( )
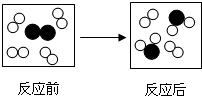

| A. | 该反应中元素的化合价不变 | |
| B. | 在该化学反应中,分子可分,原子不可分 | |
| C. | 参加反应的物质分子个数比为1:4或4:1 | |
| D. | 该反应时置换反应 |
7.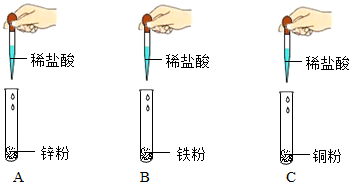 某化学兴趣小组的同学在探究“酸的化学性质”时,做了如图实验.写出实验中的一个化学方程式Fe+2HCl═FeCl2+H2↑.实验结束后,同学们将三支试管中的药品同时倒入同一个洁净的烧杯中,观察到固体表面有气泡冒出,直至不再产生气泡时发现烧杯底部有一些固体,上层为浅绿色的溶液.兴趣小组的同学对上层清液中的溶质成分展开了如下探究.
某化学兴趣小组的同学在探究“酸的化学性质”时,做了如图实验.写出实验中的一个化学方程式Fe+2HCl═FeCl2+H2↑.实验结束后,同学们将三支试管中的药品同时倒入同一个洁净的烧杯中,观察到固体表面有气泡冒出,直至不再产生气泡时发现烧杯底部有一些固体,上层为浅绿色的溶液.兴趣小组的同学对上层清液中的溶质成分展开了如下探究.
【提出问题】溶液中的溶质有哪些呢?
【做出猜想】猜想一:溶质是氯化锌、氯化亚铁;
猜想二:溶质是氯化锌、氯化亚铁、氯化铜;
猜想三:溶质是氯化锌、氯化亚铁、氯化氢.
乐乐同学认为上述有一个猜想不合理,请你指出不合理的猜想,并说明理由猜想二;铜在氢的后面,与酸不反应,不会生成氯化铜.
【进行实验】同学们设计了如下实验验证了其它两种假设.
【实验总结】通过以上探究同学们认为烧杯底部的固体物质是Cu.(写化学用语)
 某化学兴趣小组的同学在探究“酸的化学性质”时,做了如图实验.写出实验中的一个化学方程式Fe+2HCl═FeCl2+H2↑.实验结束后,同学们将三支试管中的药品同时倒入同一个洁净的烧杯中,观察到固体表面有气泡冒出,直至不再产生气泡时发现烧杯底部有一些固体,上层为浅绿色的溶液.兴趣小组的同学对上层清液中的溶质成分展开了如下探究.
某化学兴趣小组的同学在探究“酸的化学性质”时,做了如图实验.写出实验中的一个化学方程式Fe+2HCl═FeCl2+H2↑.实验结束后,同学们将三支试管中的药品同时倒入同一个洁净的烧杯中,观察到固体表面有气泡冒出,直至不再产生气泡时发现烧杯底部有一些固体,上层为浅绿色的溶液.兴趣小组的同学对上层清液中的溶质成分展开了如下探究.【提出问题】溶液中的溶质有哪些呢?
【做出猜想】猜想一:溶质是氯化锌、氯化亚铁;
猜想二:溶质是氯化锌、氯化亚铁、氯化铜;
猜想三:溶质是氯化锌、氯化亚铁、氯化氢.
乐乐同学认为上述有一个猜想不合理,请你指出不合理的猜想,并说明理由猜想二;铜在氢的后面,与酸不反应,不会生成氯化铜.
【进行实验】同学们设计了如下实验验证了其它两种假设.
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,向取中滴加紫色石蕊试液 | 溶液变为红色 | 猜想三正确 |
14.如表为氯化钠和氯化铵在不同温度时的溶解度,回答下列问题:
(1)由表中数据可知,溶解度受温度影响变化较大的物质是NH4Cl.
(2)20℃时lO0g水最多只能溶解NaCl36.0g,氯化钠与氯化铵溶解度相等的温度范围在10~20之间.
(3)向烧杯中加入100g水和50.0g氯化铵配成50℃的溶液,再冷却到20℃,烧杯中析出固体12.8g.
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 |
| NH4Cl溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
| NaCl溶解度/g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
(2)20℃时lO0g水最多只能溶解NaCl36.0g,氯化钠与氯化铵溶解度相等的温度范围在10~20之间.
(3)向烧杯中加入100g水和50.0g氯化铵配成50℃的溶液,再冷却到20℃,烧杯中析出固体12.8g.