题目内容
10.利用分子知识对下列现象的解释合理的是( )| A. | 气体更易被压缩--构成气体的分子具有弹性 | |
| B. | 液氧为淡蓝色--氧气分子是蓝色的 | |
| C. | 湿衣服变干--水分子在不断地运动 | |
| D. | 碘受热升华--碘分子变大了 |
分析 根据分子的基本特征:分子质量和体积都很小;分子之间有间隔;分子是在不断运动的;在化学变化中分子可以再分,在物理变化中,分子本身没有变化.结合事实进行分析判断即可.
解答 解:A、由于分子间有间隔,气体分子的间隔较大,所以气体更易被压缩,不是因为构成气体的分子具有弹性,故A错误;
B、氧气降温加压可以变成淡蓝色的液氧,氧分子间间隔会变小,淡蓝色是大量氧分子聚集体表现出来的性质,而不是液氧分子是淡蓝色的,故B错误;
C、由于分子是不断运动的,湿衣服上水分子通过运动分散到周围的空气中,所以湿衣服变干,故C正确;
D、由于分子间有间隔,碘受热升华是因为分子的间隔变大了,碘分子的大小没有变化,故D错误.
故选C.
点评 熟悉粒子的基本性质,经常考查到的有粒子的运动和粒子的间隔的性质,要求同学们能利用这两条性质解释一些现象.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
20.大气中存在大量的臭氧分子,其化学式是03,其中氧元素的化合价是( )
| A. | 0 | B. | +3 | C. | +2 | D. | -2 |
1.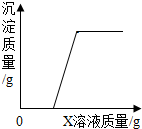 向稀盐酸和硫酸铜的混合溶液中逐滴滴入X溶液至过量,生成沉淀的质量随滴入溶液质量的变化关系如图所示.则X可能是( )
向稀盐酸和硫酸铜的混合溶液中逐滴滴入X溶液至过量,生成沉淀的质量随滴入溶液质量的变化关系如图所示.则X可能是( )
 向稀盐酸和硫酸铜的混合溶液中逐滴滴入X溶液至过量,生成沉淀的质量随滴入溶液质量的变化关系如图所示.则X可能是( )
向稀盐酸和硫酸铜的混合溶液中逐滴滴入X溶液至过量,生成沉淀的质量随滴入溶液质量的变化关系如图所示.则X可能是( )| A. | 硝酸银溶液 | B. | 氯化钡溶液 | C. | 硝酸钾溶液 | D. | 氢氧化钠溶液 |
18.“碱石灰”是指CaO和NaOH固体的混合物,它在空气久置会变质.某实验小组为探究一瓶久置的碱石灰样品的成分,设计了如图所示实验流程,请你参与探究过程:
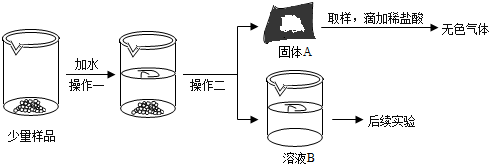
(1)使碱石灰样品充分溶解后再进行操作二,操作二的名称是过滤.
(2)根据实验现象判断固体A中一定含有碳酸钙(CaCO3).
(3)溶液B溶质的探究.
[查阅资料]①Ca(OH)2、Na2CO3溶于水无明显的温度变化;②CaCl2溶液呈中性
[猜想]溶液B中溶质可能为:①NaOH、②Na2CO3、③NaOH和Na2CO3、④Ca(OH)2和NaOH.
[设计方案并进行实验]为了探究哪个猜想正确,同学们设计如下方案步骤并进行实验:
Ⅰ、取少量溶液B于试管中,向其中碳酸钠溶液,溶液不浑浊,证明猜想④不成立.
Ⅱ、另取少量溶液B于试管中,滴加几滴酚酞试液,溶液变成红色,有同学认为溶液B中的溶质一定含有NaOH,但是立即有同学反对,他的理由是碳酸钠溶液呈碱性,也能使无色的酚酞试液变成红色.
为进一步确认溶液B中溶质的成分,他做了如下实验,请填写实验报告:

(1)使碱石灰样品充分溶解后再进行操作二,操作二的名称是过滤.
(2)根据实验现象判断固体A中一定含有碳酸钙(CaCO3).
(3)溶液B溶质的探究.
[查阅资料]①Ca(OH)2、Na2CO3溶于水无明显的温度变化;②CaCl2溶液呈中性
[猜想]溶液B中溶质可能为:①NaOH、②Na2CO3、③NaOH和Na2CO3、④Ca(OH)2和NaOH.
[设计方案并进行实验]为了探究哪个猜想正确,同学们设计如下方案步骤并进行实验:
Ⅰ、取少量溶液B于试管中,向其中碳酸钠溶液,溶液不浑浊,证明猜想④不成立.
Ⅱ、另取少量溶液B于试管中,滴加几滴酚酞试液,溶液变成红色,有同学认为溶液B中的溶质一定含有NaOH,但是立即有同学反对,他的理由是碳酸钠溶液呈碱性,也能使无色的酚酞试液变成红色.
为进一步确认溶液B中溶质的成分,他做了如下实验,请填写实验报告:
| 实验目的 | 实验步骤 | 实验现象 | 实验结论 |
检验溶液B中溶质的存在 | ①取少量溶液B于试管中,加入足量CaCl2溶液; ②过滤,在滤液中滴加酚酞试液 | ①有白色沉淀生成 ②溶液由无色变为红色 | 猜想③ 正确 |
5. 如图所示是甲、乙两种固体物质的溶解度曲线.下列说法中正确的是( )
如图所示是甲、乙两种固体物质的溶解度曲线.下列说法中正确的是( )
 如图所示是甲、乙两种固体物质的溶解度曲线.下列说法中正确的是( )
如图所示是甲、乙两种固体物质的溶解度曲线.下列说法中正确的是( )| A. | 甲物质的溶解度大于乙物质的溶解度 | |
| B. | t2℃时,向甲的饱和溶液中加入少量水,甲的溶解度变小 | |
| C. | 乙物质的饱和溶液从t2℃降到t1℃时,溶液中溶质的质量分数保持不变 | |
| D. | t2℃时,甲、乙两物质各50g,分别充分溶解于100g水中,得到的溶液质量分数相同 |
15.化学实验小组的同学为确定某石灰石中碳酸钙的质量分数,进行了如表所示的实验:
(1)该石灰石中碳酸钙的质量分数为82.5%.
(2)计算实验中所用稀盐酸的溶质质量分数.
| 实验编号 | 石灰石的质量/g | 加入稀盐酸的质量/g | 剩余固体质量/g |
| 实验1 | 20 | 40 | 8.0 |
| 实验2 | 20 | 60 | 3.5 |
| 实验3 | 20 | 80 | 3.5 |
(2)计算实验中所用稀盐酸的溶质质量分数.
2.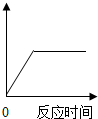 在实验室加热氯酸钾和二氧化锰的混合物制取氧气.若如图中横坐标表示反应时间,纵坐标表示的是( )
在实验室加热氯酸钾和二氧化锰的混合物制取氧气.若如图中横坐标表示反应时间,纵坐标表示的是( )
 在实验室加热氯酸钾和二氧化锰的混合物制取氧气.若如图中横坐标表示反应时间,纵坐标表示的是( )
在实验室加热氯酸钾和二氧化锰的混合物制取氧气.若如图中横坐标表示反应时间,纵坐标表示的是( )| A. | 氯酸钾的质量 | B. | 钾元素的质量 | C. | 二氧化锰的质量 | D. | 生成氧气的质量 |
19.以下物品所用材料中,属于有机合成材料的是( )
| A. | 电脑塑料外壳 | B. | 真丝围巾 | C. | 不锈钢防盜门 | D. | 玻璃茶杯 |
20.皮蛋是我国传统的蛋制品,深受人们喜爱,由少量NaCl、CaO和过量Na2CO3混合得到的粉末状混合物A是腌制皮蛋的配方之一.
(1)某化学兴趣小组从市场获取少量混合物A于烧杯中,缓慢加入足量的蒸馏水,边加边搅拌,静置,过滤得滤液.
①该过程发生反应的化学方程式为CaO+H2O=Ca(OH)2,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
②滤液中除含有Cl-、OH-外,还含有的阴离子是CO32-.
(2)在混合物A中加入少量ZnSO4可改善皮蛋品质,该兴趣小组获得某样品,探究在混合物A中是否添加了少量ZnSO4.
设计实验方案,完成如表表格.
限选用品与试剂:稀盐酸、pH试纸、BaC12溶液、蒸馏水、AgNO3溶液.
(1)某化学兴趣小组从市场获取少量混合物A于烧杯中,缓慢加入足量的蒸馏水,边加边搅拌,静置,过滤得滤液.
①该过程发生反应的化学方程式为CaO+H2O=Ca(OH)2,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
②滤液中除含有Cl-、OH-外,还含有的阴离子是CO32-.
(2)在混合物A中加入少量ZnSO4可改善皮蛋品质,该兴趣小组获得某样品,探究在混合物A中是否添加了少量ZnSO4.
设计实验方案,完成如表表格.
限选用品与试剂:稀盐酸、pH试纸、BaC12溶液、蒸馏水、AgNO3溶液.
| 实验操作 | 预期现象和必要结论 |
| 步骤1:取少量样品于烧杯中,缓慢加入足量蒸馏水,充分搅拌,静置,过滤 | / |
| 步骤2:取少量步骤1所得的滤液于试管中,向其中加入足量的稀盐酸,振荡,观察现象.. | 有气泡生成 |
| 步骤3:向步骤2反应后溶液中滴入少量的BaCl2溶液,观察现. | 若有白色沉淀生成,说明样品中有ZnSO4; 若无明显现象,说明样品中没有ZnSO4. |